Контаминант
Контаминáнт (от лат. contaminant — примесь, также загрязняющий агент) — нежелательный биологический агент (микроорганизмы, включая и вирусы) либо химическое соединение, смесь соединений, обладающие высокой биологической активностью (аллерген, иммуносупрессор, канцероген, мутаген, тератоген, токсин или в общем случае ксенобиотик) либо радиоактивное вещество (радионуклид), присутствие которых в сырье и пищевых продуктах[3] несвойственно и, несомненно, может оказывать негативное воздействие на организм и, как следствие, нести угрозу для здоровья и жизни человека. Процесс, в результате которого происходит загрязнение пищевых продуктов и сырья контаминантами называется контаминацией.
.png.webp)

Термин контаминант употребляется в основном в микробиологии (синоним термина обсеменение), в производстве фармацевтической продукции и в производстве пищевых продуктов[4][5][6]. В большинстве случаев загрязнение пищевого продукта контаминантами является причиной алиментарных расстройств ЖКТ у человека (пищевые интоксикации).
Контаминанты обладают высокой подвижностью и скоростью миграции и, тем самым довольно легко проникают в организм человека из внешней среды[7].
Не следует путать термины контаминант и ксенобиотик. Первый означает любой загрязняющий агент продуктов питания и попадает в организм исключительно алиментарным путём (то есть с пищей), в то время как второй термин означает любое чужеродное вещество, попавшее в организм человека не обязательно алиментарным путём, например, воздушным (респираторным) или через кожу (трансдермально). Любой контаминант — это ксенобиотик, но не каждый ксенобиотик — это контаминант.
Биологические контаминанты


Биологические, также природные или естественные контаминанты — нежелательные микроорганизмы (вирусы, патогенные и условно-патогенные бактерии, микроскопические грибы, простейшие, споры микромицетов итд.), а также их продукты метаболизма (например, ботулотоксин, продуцируемый Clostridium botulinum или охратоксины — группа микотоксинов, вырабатываемые некоторыми видами микроскопических плесневых грибов рода Аспергилл и Пеницилл), присутствующие в пищевых продуктах. Большое количество биологических контаминантов приходится на бактерии и их метаболитов (токсинов, антибиотиков). К этой группе можно отнести токсины морских животных, употребляемых в пищу (например, тетродотоксин из собаки-рыбы или фугу), а также токсины растений или фитотоксины (например, рицин, из ядер клещевины или амигдалин из косточек горького миндаля, абрикоса — ядовитый гликозид) и грибов (аматоксины, фаллотоксины и др.).
 Дезоксиниваленол или вомитоксин (от англ. Vomiting — рвота), наиболее распространённый трихотецен, продуцируется микроскопическими плесневыми грибами рода Fusarium (Fusarium culmorum, Fusarium graminearum). Высокотоксичен, обладает иммуносупрессивным эффектом, вызывает сильнейшее отравление сопровождаемое упорной рвотой, поражением ЖКТ и агранулоцитозом[8][9].
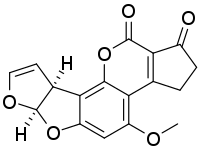
Дезоксиниваленол или вомитоксин (от англ. Vomiting — рвота), наиболее распространённый трихотецен, продуцируется микроскопическими плесневыми грибами рода Fusarium (Fusarium culmorum, Fusarium graminearum). Высокотоксичен, обладает иммуносупрессивным эффектом, вызывает сильнейшее отравление сопровождаемое упорной рвотой, поражением ЖКТ и агранулоцитозом[8][9].-Aflatoxin_B1_Structural_Formulae_V.1.svg.png.webp) Афлатоксин B1 — один из представителей афлатоксинов, смертельно опасный токсин, а также сильнейший гепатоканцероген[10]. Продуцируется микроскопическими плесневыми грибами рода Аспергилл (Aspergillus flavus, Aspergillus parasiticus).
Афлатоксин B1 — один из представителей афлатоксинов, смертельно опасный токсин, а также сильнейший гепатоканцероген[10]. Продуцируется микроскопическими плесневыми грибами рода Аспергилл (Aspergillus flavus, Aspergillus parasiticus).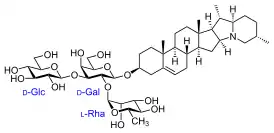 Соланин — стероидный гликозид, фитотоксин вырабатываемый некоторыми видами растений семейства паслёновых или Solanaceae (ягоды чёрного паслёна, клубни картофеля итд.)[11].
Соланин — стероидный гликозид, фитотоксин вырабатываемый некоторыми видами растений семейства паслёновых или Solanaceae (ягоды чёрного паслёна, клубни картофеля итд.)[11].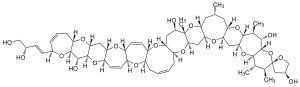 Сигуатоксин 1В — полициклический полиэфир, очень ядовит, продуцируется некоторыми видами динофлагеллятов (Gambierdiscus toxicus). Вместе с планктоном поедается токсин, который накапливается в жировой ткани, внутренностях и коже многих видов морских рыб, тем самым он представляет огромную опасность. Интоксикация сигуатоксином проявляется в виде сигуатеры[12].
Сигуатоксин 1В — полициклический полиэфир, очень ядовит, продуцируется некоторыми видами динофлагеллятов (Gambierdiscus toxicus). Вместе с планктоном поедается токсин, который накапливается в жировой ткани, внутренностях и коже многих видов морских рыб, тем самым он представляет огромную опасность. Интоксикация сигуатоксином проявляется в виде сигуатеры[12].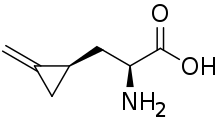 Гипоглицин A — непротеиногенная аминокислота, фитотоксин, содержится в незрелых плодах и семенах Аки (Blighia sapida) и личи (Litchi chinensis)[13]. Высокотоксичен, вызывает специфическое заболевание Ямайскую рвотную болезнь, сопровождаемое сильнейшей интоксикацией и гипогликемией[14].
Гипоглицин A — непротеиногенная аминокислота, фитотоксин, содержится в незрелых плодах и семенах Аки (Blighia sapida) и личи (Litchi chinensis)[13]. Высокотоксичен, вызывает специфическое заболевание Ямайскую рвотную болезнь, сопровождаемое сильнейшей интоксикацией и гипогликемией[14].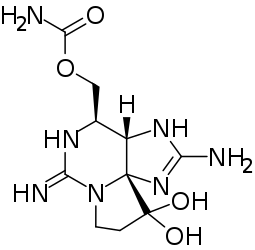 Сакситоксин (STX), накапливается в съедобных морских моллюсках (мидии, морское ушко, устрицы, итд.), которые в свою очередь питаются продуцентами — динофлагеллятами (Gonyaulax catenella, Alexandrium sp., Gymnodinium sp., Pyrodinium sp.) и цианобактериями (Anabaena sp., Aphanizomenon spp., Cylindrospermopsis sp., Lyngbya sp., Planktothrix sp.). Сильнейший яд небелковой природы с ярко выраженным нервно-паралитическим воздейстием, ЛД50 ~5,7 мкг/кг перорально для человека (так, одна мелкая мидия может содержать сакситоксин в дозе, достаточной чтобы убить 50 человек[15]). Селективный блокатор потенциал-зависимых натриевых каналов[16] (сходный по действию с тетродотоксином), тем самым поражает ЦНС.
Сакситоксин (STX), накапливается в съедобных морских моллюсках (мидии, морское ушко, устрицы, итд.), которые в свою очередь питаются продуцентами — динофлагеллятами (Gonyaulax catenella, Alexandrium sp., Gymnodinium sp., Pyrodinium sp.) и цианобактериями (Anabaena sp., Aphanizomenon spp., Cylindrospermopsis sp., Lyngbya sp., Planktothrix sp.). Сильнейший яд небелковой природы с ярко выраженным нервно-паралитическим воздейстием, ЛД50 ~5,7 мкг/кг перорально для человека (так, одна мелкая мидия может содержать сакситоксин в дозе, достаточной чтобы убить 50 человек[15]). Селективный блокатор потенциал-зависимых натриевых каналов[16] (сходный по действию с тетродотоксином), тем самым поражает ЦНС. Аманин — один из представителей аматоксинов, встречается в плодовых телах грибов рода Аманита (Мухомор), Лепиота и Галерина, чрезвычайно токсичен и смертельно опасен, сильнейший гепатотоксин, вызывает лизис и некрозы клеток паренхимы печени, помимо этого он разрушает клетки кишечника и почек (вызывает острую почечную недостаточность)[17].
Аманин — один из представителей аматоксинов, встречается в плодовых телах грибов рода Аманита (Мухомор), Лепиота и Галерина, чрезвычайно токсичен и смертельно опасен, сильнейший гепатотоксин, вызывает лизис и некрозы клеток паренхимы печени, помимо этого он разрушает клетки кишечника и почек (вызывает острую почечную недостаточность)[17]._PDB_1r4q.png.webp) Веротоксин — токсин Коли, вызывает сильнейшее пищевое отравление, сопровождаемое геморрагической лихорадкой, повреждением сосудов внутренних органов, гемолитической анемией.
Веротоксин — токсин Коли, вызывает сильнейшее пищевое отравление, сопровождаемое геморрагической лихорадкой, повреждением сосудов внутренних органов, гемолитической анемией.
Бактериальные токсины
Бактериальные токсины загрязняют пищевые продукты и являются причиной острых пищевых интоксикаций. Рассмотрим наиболее часто регистрируемые интоксикации, связанные с поражением пищевых продуктов некоторыми бактериальными токсинами.
Энтеротоксины S.aureus
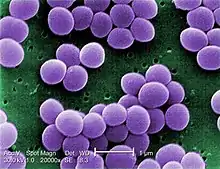
Staphylococcus aureus — грамположительные бактерии, сферической формы, которые являются причиной стафилококкового пищевого отравления. Продуцируют следующие энтеротоксины: А, В, С1, С2, D, E, которые представляют собой полипептиды с молекулярной массой 26 360-28 500 Да. Энтеротоксины S. aureus термостабильны и инактивируются лишь после 2-3-часового кипячения. Бактерицидным действием по отношению к стафилококкам обладают уксусная, лимонная, фосфорная, молочная кислоты при рН до 4,5. Кроме того, жизнедеятельность бактерий прекращается при концентрации соли (NaCl) — 12 %, сахара — 60-70 %, вакуумная упаковка также ингибирует рост бактерий. Всё это необходимо учитывать в различных технологиях консервирования, как в промышленном масштабе, так и в домашних условиях.
Наиболее благоприятной средой для роста и развития стафилококков являются молоко, мясо и продукты их переработки, а также кондитерские кремовые изделия, в которых концентрация сахара составляет менее 50 %. Стафилококковые энтеротоксины являются причиной 27-45 % всех пищевых токсикоинфекций.
Стафилококковые гастроэнтериты вызываются при приёме внутрь пищи, содержащей один или несколько энтеротоксинов, выделяемых некоторыми видами и штаммами стафилококков[18]. Хотя и считается, что выделение энтеротоксинов обычно связано со штаммами S. aureus, продуцирующих коагулазу и термонуклеазу, многие штаммы, не продуцирующие ни коагулазу, ни термонуклеазу, тем не менее выделяют энтеротоксины.
Симптомы стафилококкового пищевого отравления обычно развиваются в течение четырёх часов после приема внутрь заражённых пищевых продуктов, хотя этот интервал, по разным сообщениям, может различаться в пределах от одного до шести часов[19]. Среди симптомов обычно отмечаются такие, как тошнота, рвота, спазмы живота (которые, как правило, бывают очень сильными), диарея, выпотевание, головная боль, упадок сил, истощение, иногда снижение температуры тела — которые обычно продолжаются от 24 до 48 ч. Смертельные исходы достаточно редки или полностью отсутствуют. Как правило, для здоровых людей лечение ограничивается постельным режимом и поддержанием баланса жидкости в организме. После прекращения симптомов у переболевших не сохраняется выраженного иммунитета к повторным заражениям, хотя при неоднократном пероральном введении доз у животных появляется устойчивость к энтеротоксину[20]. Поскольку симптомы были вызваны приёмом внутрь уже сформированного энтеротоксина, понятно, что культуры из фекальных масс не содержат стафилококков, хотя это и случается редко.
Токсины C.perfringens
Clostridium perfringens (ранее известная как C. welchii или Bacillus welchii) представляет собой грамположительную, палочковидную, облигатно (строго) анаэробную, спорообразующую патогенную бактерию рода Клостридиум[21][22]. Является одним из возбудителей газовой гангрены и клостридиальной кишечной токсоинфекции.
Штаммы Clostridium perfringens, вызывающие пищевые отравления, обнаруживаются в почве, воде, пыли, продуктах питания, пряностях и в пищеварительных трактах человека и животных. Многие исследователи сообщали, что распространённость термоустойчивых, негемолитических штаммов в общей популяции оценивается в пределах от 2 до 6 %. В экскрементах от 20 до 30 % здорового персонала больниц и членов их семей были обнаружены эти организмы, а среди заболевших процент носителей этих токсигенных клостридий через две недели равнялся 50 %, а иногда достигал и 88 %. Термочувствительные штаммы являются обычными представителями микрофлоры желудочно-кишечного тракта у всех людей. Бактерии C. perfringens попадают в мясо либо непосредственно после забоя животных, либо в результате последующего заражения мяса животных руками людей или пылью. Поскольку клостридии являются спорообразующими бактериями, они могут противостоять неблагоприятным условиям среды, высушиванию, нагреванию и воздействию различных токсических веществ.
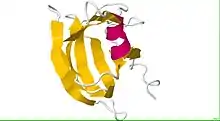
Энтеротоксин является фактором, определяющим пищевые отравления при попадании бактерий C.perfringens в организмы человека и животных. Он имеет молекулярную массу 35,3 кДа и отвечает за распад плотных контактов, образованных между эпителиальными клетками в кишечнике[23]. Необычным является то, что этот белок является споро-специфическим; его выделение происходит параллельно с процессом споруляции. Причиной всех известных случаев пищевых отравлений, вызванных этим видом бактерий, были штаммы, относящиеся к типу A. Другое заболевание, некротический энтерит, вызывается бета-токсином, производимым штаммами типа С. Это заболевание характерно для Новой Гвинеи, и весьма редки сообщения о таком отравлении за её пределами. Несмотря на то что некротический энтерит, вызываемый клостридиями типа С, связан с уровнем смертности в 35-40 %, пищевые отравления, вызываемые клостридиями типа A, являются фатальными только для пожилых и ослабленных людей. Показано, что некоторые штаммы клостридий типа С продуцируют энтеротоксин, но его значение и роль в заболеваниях пока не ясны.
Ботулинистические токсины

В отличие от отравления пищей, содержащей бактерии C. perfringens, при котором большое количество жизнеспособных клеток должны попасть в желудочно-кишечный тракт, симптомы ботулизма вызываются попаданием в организм чрезвычайно токсичного, растворимого энтеротоксина — ботулинистического, продуцируемого бактериями, растущими в продуктах питания.
Ботулизм вызывается некоторыми штаммами бактерий C. botulinum, которые являются грамположительными анаэробными спорообразующими палочками, имеющими форму от овальной до цилиндрической, со спорами, расположенными на конце или почти на конце палочковидной клетки. На основании серологической спецификации их токсинов определены семь типов: A, B, C, D, E, F и G[24][25]. Токсины A, B, E, F и G вызывают заболевания у человека; тип С вызывает ботулизм у домашней птицы и дичи, рогатого скота, норки и других животных; тип D связан с отравлением скота фуражом, в особенности в Южной Африке. Дифференциация типов штаммов осуществляется также на основании их протеолитической активности. Типы A и G являются протеолитическими, также как и некоторые из штаммов, принадлежащих к типам B и F. Тип E непротеолитический, так же как и некоторые из штаммов, принадлежащих к типам B и F. Протеолитическая активность штаммов типа G слабее, чем у штаммов типа A, и для действия их токсина необходимо участие трипсина. Все штаммы, продуцирующие токсин типа G, объединены внутри вида C. argentinense. Штаммы этого вида были выделены из почв Аргентины, Швейцарии и США.
Ботулотоксины, образующиеся в бактериях С.botulinum, высвобождаются в результате автолиза. Они продуцируются клетками, растущими в оптимальных условиях, хотя были сообщения о том, что покоящиеся клетки также образуют токсины. Ботулотоксины являются наиболее токсичными из всех известных природных ядов нервно-паралитического действия. Летальные дозы некоторых типов достигают нескольких десятков пикограмм на килограмм живого веса.
Токсины Сальмонелл и Шигелл
Сальмонеллы являются мелкими, грамотрицательными, неспорообразующими палочковидными бактериями[26], которые практически ничем не отличаются внешне от E. coli под микроскопом или при выращивании на обычных питательных средах. Эти бактерии широко распространены в природе. При этом человек и животные являются их главными резервуарами. Основным механизмом пищевых отравлений сальмонеллами является заглатывание пищевых продуктов, содержащих патогенные штаммы этого рода бактерий в значительных количествах.
Род Shigella принадлежит к семейству Enterobacteriaceae так же, как Salmonella и Escherichia.В этом роду определены только четыре вида: S.dysenteriae, S.flexneri, S.boydii и S.sonnei. Среди них S.dysenteriae является основным патогеном, вызывающим бациллярную форму дизентерии. Установлено, что для возникновения инфекции у чувствительных индивидуумов достаточно попадания в организм всего лишь 10 КОЕ.
Вирусы как биологические контаминанты
По ряду причин о случаях обнаружения в продуктах вирусов известно намного меньше, чем о бактериях и грибах. Во-первых, вирусы — облигатные паразиты, которые не растут на культуральных питательных средах как бактерии и грибы. Обычно для культивирования вирусов применяют культуру ткани или методики, использующие куриный эмбрион. Во-вторых, вирусы не размножаются в продуктах, их число, как предполагают, ниже по сравнению с бактериальным числом, и для их выделения необходимы методы экстракции и концентрирования. Хотя этой методологии было посвящено много исследований, трудно получить больше 50%-го выделения вирусных частиц из таких продуктов, как говядина. В-третьих, лабораторные вирусологические методики неосуществимы во многих микробиологических лабораториях, исследующих пищевые продукты.
Вирус гепатита A
До 1990-х гг. вспышек гепатита А обнаруживаемого в продуктах, было зарегистрировано больше, чем любой другой вирусной инфекции. Вирус принадлежит семейству Picornaviridae так же, как и полиомиелит, ЕСНО-вирус и вирус Коксаки, все они имеют геномы из односпиральной РНК (ssРНК). Инкубационный период при гепатите длится от 15 до 45 дней с пожизненным иммунитетом к повторному заражению. Способ передачи — фекально-оральный, самое обычное средство передачи — сырой или частично приготовленный моллюск из загрязнённых вод.
Прионы как контаминанты
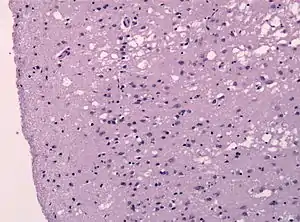
Прионы (англ. prion от protein «белок» + infection «инфекция»; слово было предложено в 1982 году Стенли Прузинером[27]) представляют собой особый класс инфекционных агентов, который не содержит нуклеиновых кислот. Прионы это белки, имеющие аномальную третичную структуру, способные к катализу конформационных превращений гомологичных молекул белка в себе подобные. При этом процесс инфицирования протекает без участия передачи информации, осуществляемых посредством нуклеиновых кислот. Благодаря патологическому фолдингу в здоровых клетках растёт число молекул прионов, происходит замещение нормальных белков на последние, которые способны к образованию плотно упакованных фибриллярных белков — бета-амилоидов. Вызванные патологические процессы являются необратимыми. Прионные заболевания протекают очень медленно, имеют долгий латентный период (некоторые более 15 лет), однако все они неизлечимы и имеют 100%-ую летальность.
Прионы очень устойчивые к агрессивным воздействиям, они не чувствительны к термической обработке, ионизирующему излучению, формалину, протеолизу, некоторых окислителей (перекись водорода, фенолы). Передача прионов к человеку возможна алиментарным путём через инфицированное мясо и мясные продукты, больных животных — овец, коров.
Микотоксины и токсины грибов
Микотоксины (от греч. μύκης, mykes, mukos — «гриб» и τοξικόν, toxikon — «яд») — это вторичные метаболиты микроскопических плесневых грибов, обладающие выраженными токсическими свойствами[28]. Они не являются эссенциальными для роста и развития продуцирующих их микроорганизмов.
С гигиенических позиций — это особо опасные токсические вещества, загрязняющие корма и пищевые продукты. Высокая опасность микотоксинов выражается в том, что они обладают токсическим эффектом в чрезвычайно малых количествах и способны весьма интенсивно диффундировать вглубь продукта.
Афлатоксины

Афлатоксины (AF, сокр. от Aspergillus flavus toxins) — органические соединения, из группы поликетид, представляют собой одну из наиболее опасных групп микотоксинов, обладающих чрезвычайной высокой токсичностью и гепатоканцерогенностью[29].
Афлатоксины, несомненно, наиболее изученные из всех микотоксинов. Первые данные об их существовании относятся к 1960 году, когда внезапно и почти одновременно 100 000 индюшат погибли в Англии (так называемая «болезнь-Х») после употребления арахисовой муки, импортируемой из Африки и Южной Америки[30].
В настоящее время семейство афлатоксинов включает четыре основных представителя (афлатоксины B1, B2, G1, G2)[31] и ещё более 10 соединений, являющихся производными или метаболитами основной группы (M1, M2, B2a, G2a, GM1, афлатоксикол, P1, Q1 и др.)[32].
Продуцентами афлатоксинов являются некоторые штаммы двух видов микроскопических грибов: Aspergillus flavus (Link.) и Aspergillus parasiticus (Speare).
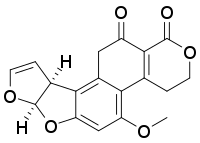 AFG1 | 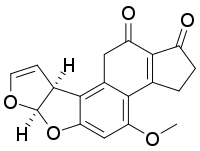 AFM1 | |
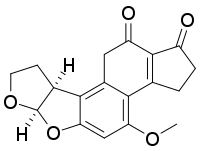 AFB2 | 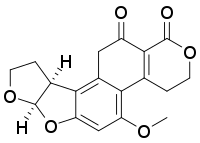 AFG2 | 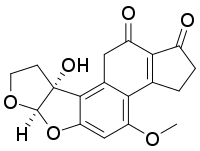 AFM2 |

В природных условиях чаще и в наибольших количествах афлатоксины обнаруживаются в арахисе, кукурузе, семенах хлопчатника. Кроме того, в значительных количествах они могут накапливаться в различных орехах (грецкий орех, миндаль, фундук, кешью и др.), семенах масличных культур, пшенице, ячмене, зёрнах какао и кофе[33].
В кормах, предназначенных для сельскохозяйственных животных, афлатоксины также обнаруживаются достаточно часто и в значительных количествах. Во многих странах с этим связано и обнаружение афлатоксинов в продуктах животного происхождения. Например, в молоке и тканях сельскохозяйственных животных, получавших корма, загрязнённые микотоксинами, обнаружен афлатоксин М1. Причём афлатоксин М1 обнаружен как в цельном, так и в сухом молоке и даже в молочных продуктах, подвергшихся технологической обработке (пастеризация, стерилизация, приготовление творога, йогурта, сыров и т. п.).
Термическая обработка, используемая в кулинарии не способствует уменьшению концентрации афлатоксинов, ввиду того, что они устойчивы к нагреванию, даже в автоклавах при довольно высоких температурах и продолжительности процесса (t > 120° C, более 40 минут). Для разрушения афлатоксинов необходимы дополнительные мероприятия, например, использование окислителей, экстракция с полярными органическими растворителями (хлороформ, ацетон) или азеотропными смесями (оптимальный вариант — смесь воды и метоксиметана), использование раствора или газообразного аммиака, который наиболее эффективно уничтожает организмы продуценты аспергиллы и разрушает до 98 % афлатоксинов.
Токсическое воздействие афлатоксинов
Действие афлатоксинов на организм животных и человека может быть охарактеризовано с двух позиций. Во-первых, с точки зрения острого токсического действия и, во-вторых, с точки зрения оценки опасности отдалённых последствий.
Острое токсическое действие афлатоксинов связано с тем, что они являются одними из наиболее сильных гепатропных ядов, органом-мишенью которых является печень. Отдалённые последствия действия афлатоксинов проявляются в виде канцерогенного, мутагенного и тератогенного и иммунодепрессивного эффектов. Наиболее изучен афлатоксин B1.
| Животные | Способ введения | Токсичность (LD50) в мг/кг |
|---|---|---|
| Утка | п/о | 0,5-2,0 |
| Крысы | п/о, вб | 1,2-17,9 (в зависимости от пола и возраста) |
| Хомяки | п/о | 9,0-10,2 |
| Мыши | п/о | 6,0-9,0 |
| Кролики | п/о | ~0,5 |
| Морские свинки | вб | ~1,0 |
| Собака | п/о | 0,45-0,5 |
| Речная форель | п/о | <0,5 |
Механизм воздействия на гепатоциты имеет сходства с механизмом воздействия ПАУ. Однако продукты гидроксилирования имеют более высокие окислительные свойства и повреждают клетки посредством нарушения структуры целостности биомембран и алкирования нуклеиновых кислот.
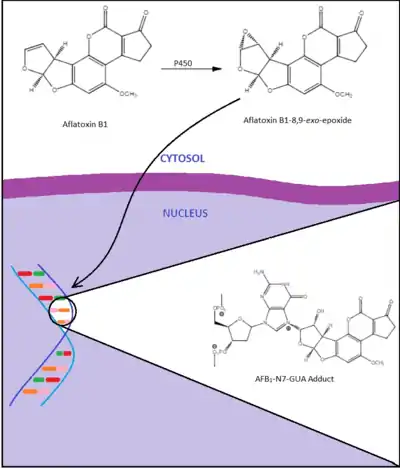
В молекулах афлатоксинов содержится большое количество атомов кислорода, вследствие этого, попадая в клетку печени и подвергаясь эпоксидированию (окислению), посредством цитохрома P450 микросомальной системы молекулы приобретают чрезвычайно реакционноспособные свойства. Молекулы образовавшегося эпоксида легко проникает в ядро, с помощью белка AHR. В ядре они немедленно начинают алкилировать цепи ДНК, образуя с ними прочные аддукты. Происходит торможение и полное подавление синтеза молекул тРНК. В ядре появляются морфологические изменения. Алкилирование ДНК приводит к повреждениям гена-онкосупрессора p53, вплоть до утраты к экспрессии белка[34]. Тем самым лишая гепатоцит апоптоза. Дальнейшее продолжение процесса приводит к трансформации клеток, посредством активации некоторых онкогенов, например, K-ras, вызывая гепатоцеллюлярную карциному[35].
Скорость алкилирования лимитируется концентрацией продуктов гидроксилирования, однако, даже минимальное количество причиняет серьёзные повреждения гепатоцитам. Помимо этого они обладают сильнейшей гепатотоксичностью (в особенности афлатоксин B1 — наиболее токсичный, СДЯВ, минимальная летальная доза для человека составляет менее 2 мг/кг).
Афлатоксины способны вызывать у человека острые и хронические микотоксикозы, названные афлатоксикозами. Возникновению афлатоксикозов способствует отсутствие надлежащего санитарно-эпидемиологического контроля за продуктами питания, особенно в странах с жарким и влажным климатом (страны тропической Африки, Юго-восточной Азии и Индия), где среди местного населения наблюдаются высокие показатели цирроза печени и гепатоцеллюлярной карциномы.
Помимо гепатотропного и канцерогенного эффектов, афлатоксины способны снижать иммунитет, посредством влияния на митохондрии и клеточные мембраны лимфоцитов. Нарушают синтез цитокинов макрофагов и Т-лимфоцитов.
Отравление афлатоксинами требует безотлагательных мер медицинской помощи.
Согласно данным ВОЗ, человек при благоприятной гигиенической ситуации потребляет с суточным рационом до 0,19 мкг афлатоксинов. В России приняты следующие санитарно-гигиенические нормативы по афлатоксинам: № 015/2011 о безопасности зерна и № 021/2011 о безопасности пищевой продукции ПДК афлатоксина В1 для всех пищевых продуктов, кроме молока, составляет 5 мкг/кг, для молока и молочных продуктов — 1 мкг/кг (для афлатоксина М1 — 0,5 мкг/кг). Допустимая суточная доза (ДСД) — 0,005-0,01 мкг/кг массы тела. В ферментных молокосвертывающих препаратах грибного происхождения, продуктах для детей, беременных и кормящих женщин наличие афлатоксина B1 не допускается.
Трихотецены
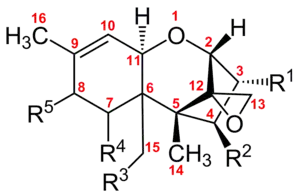
Трихотеценовые микотоксины или просто трихотецены (сокр. ТТМТ) — органические соединения из так называемого семейства сесквитерпеноидов, их отличительной чертой служит трихотеценовое кольцо (трихотекан), которое содержит двойную связь при С-9 и эпоксидную группу в области С-12,13[36]. В настоящее время идентифицировано более 100 трихотеценов, большинство из них являются слаботоксичными, лишь немногие — смертельно опасны. Трихотеценовые микотоксины — вторичные метаболиты, которые продуцируются в основном микроскопическими плесневыми грибами (микромицетами) рода Fusarium, а также в меньшей степени Stahybotrys, Trichoderma, Cephalosporium, Trichothecium и Mizothecium. Биологические контаминанты, являются сильными иммунодепрессантами, поражают органы кроветворения, ЖКТ, повышают риск возникновения геморрагий (кровоизлияний) внутренних органов человека[37].
В зависимости от структуры трихотеценового ядра эти микотоксины подразделяются на 4 группы: А, В, С и D. Структура различных типов трихотеценовых микотоксинов очень сложна и имеет свои характерные особенности.
В качестве природных загрязнителей (контаминантов) пищевых продуктов и кормов к настоящему времени выявлены только четыре: Т-2 токсин и диацетоксискирпенол, относящиеся к типу А, а также ниваленол и дезоксиниваленол (вомитоксин), относящиеся к типу B.

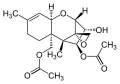 Диацетоксискирпенол
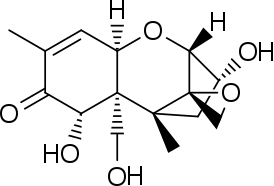
Диацетоксискирпенол Дезоксиниваленол или вомитоксин
Дезоксиниваленол или вомитоксин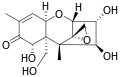 Ниваленол
Ниваленол
Токсическое воздействие трихотеценов
Охратоксины
Охратоксины — органические соединения, группа микотоксинов, производные кумарина, продуцируемые некоторыми видами микроскопических плесневых грибов рода Аспергилл (страны с преимущественно субтропическим и тропическим климатом) и Пеницилл (страны с умеренным климатом). Основной продуцент охратоксинов среди грибов рода Пеницилл — Penicillium verrucosum, среди аспергиллов — Aspergillus ochraceus и некоторые другие виды аспергиллов, включая A.carbonarius и A.niger. Являются биологическими контаминантами. Источниками охратоксинов служат растительные продукты, в особенности зерновые культуры (пшеница, ячмень, кукуруза итд.). По обобщённым статистическим данным, в европейских странах, Канаде, США частота контаминации зерна охратоксином А составляет 5 % и характеризуется диапазоном содержаний токсина от 5 до 360 мкг/кг[38].
Из культуры гриба А. ochraceus выделено четыре охратоксина — А, В, С и D (ТА). Все охратоксины проявляют сильную нефротоксичность. В крови они быстро связываются с белками. Наиболее распространённым и токсичным является охратоксин А. Охратоксины незначительно различаются между собой (имеют сходную структуру молекул). Так, например, охратоксин В в отличие от типа А не содержит атома хлора; охратоксин С — это этилохратоксин А[39].
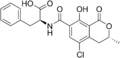
 Охратоксин B
Охратоксин B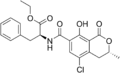 Охратоксин C
Охратоксин C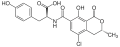 Охратоксин TA
Охратоксин TA
Токсичность охратоксинов Охратоксины входят в группу микотоксинов, преимущественно поражающих почки (нефротоксины). Охратоксин А нефротоксичен для всех изученных до сих пор видов животных даже при воздействии в наименьших из исследованных концентрациях (200 мкг/кг корма у крыс и свиней). Поражение включает атрофию канальцев, интерстициальный фиброз и, в поздних стадиях, гиалинизацию клубочков. При остром токсикозе, вызванном охратоксинами, патологические изменения выявляются и в печени, и в лимфоидной ткани, и в желудочно-кишечном тракте. В настоящее время уже доказано, что охратоксин А обладает сильным тератогенным действием. Вопрос о канцерогенности охратоксинов для человека остается нерешёнными.
Биохимические, молекулярные, клеточные механизмы действия охратоксинов изучены недостаточно. В исследованиях in vitro показано, что они активно связываются с различными белками: альбуминами сыворотки крови, тромбином, альдолазой, каталазой, аргиназой, карбоксипептидазой А. Некоторые моменты подтверждены и в исследованиях in vivo. Результаты изучения влияния охратоксинов на синтез макромолекул свидетельствуют о том, что охратоксин А ингибирует синтез белка и матричной РНК (токсин действует как конкурентный ингибитор), но не действует на синтез ДНК.
Для охратоксина А период полураспада в организме человека определён в 840 часов.
Патулин

Патулин — особо опасное вещество, обладающее канцерогенными и мутагенными свойствами, производное пирана (4-гидроксифуропиранон), трикетид, вторичный метаболит и микотоксин, продуцируемый некоторыми видами микроскопических плесневых грибов рода Aspergillus, Penicillium и реже Byssochlamys. Широко распространён. Является биологическим контаминантом. Высокотоксичен (при пероральном приёме), поражает органы ЖКТ, обладает канцерогенным и генотоксическим воздействием. Помимо этого он проявляет свойства антибиотика, действуя на некоторые виды микроорганизмов[40]. Термостабилен, не разрушается при продолжительном нагревании и пастеризации.
Основными продуцентами патулина являются микроскопические грибы Penicillium patulum и Penicillium expansu. Но и другие виды этого рода микроскопических грибов, а также Byssochlamys fulva и B. nivea способны синтезировать патулин. Максимальное токсинообразование отмечается при температуре 21-30 °С.
Биологическое действие патулина проявляется как в виде острых токсикозов, так и в виде ярко выраженных канцерогенных и мутагенных эффектов. Биохимические механизмы действия патулина изучены недостаточно. Предполагают, что патулин блокирует синтез ДНК, РНК и белков, причём блокирование инициации транскрипции осуществляется за счет ингибирования ДНК-зависимой-РНК-полимеразы. Кроме этого, микотоксин активно взаимодействует с SH-группами белков и подавляет активность тиоловых ферментов.
Продуценты патулина поражают в основном фрукты и некоторые овощи, вызывая их гниение. Патулин обнаружен в яблоках, грушах, абрикосах, персиках, вишне, винограде, бананах, клубнике, голубике, бруснике, облепихе, айве, томатах. Наиболее часто патулином поражаются яблоки[41], где содержание токсина может доходить до 17,5 мг/кг. Патулин концентрируется в основном в подгнившей части яблока, в отличие от томатов, где он распределяется равномерно по всей ткани.
Патулин в высоких концентрациях обнаруживается и в продуктах переработки фруктов и овощей: соках, компотах, пюре и джемах. Особенно часто его находят в яблочном соке (0,02-0,4 мг/л). Содержание патулина в других видах соков: грушевом, айвовом, виноградном, сливовом, манго — колеблется от 0,005 до 4,5 мг/л. Интересным представляется тот факт, что цитрусовые и некоторые овощные культуры, такие как картофель, лук, редис, редька, баклажаны, цветная капуста, тыква и хрен обладают естественной устойчивостью к заражению грибами-продуцентами патулина.
Контроль за загрязнением микотоксинами
В настоящее время вопросы контроля за загрязнением продовольственного сырья, пищевых продуктов и кормов микотоксинами решаются не только в рамках отдельных государств, но и на международном уровне под эгидой ВОЗ и ФАО.
В системе организации контроля за загрязнением продовольственного сырья и пищевых продуктов можно выделить два уровня: инспектирование и мониторинг, которые включают регулярные количественные анализы продовольственного сырья и пищевых продуктов.
Мониторинг позволяет установить уровень загрязнения, оценить степень реальной нагрузки и опасности, выявить пищевые продукты, являющиеся наиболее благоприятным субстратом для микроскопических грибов — продуцентов микотоксинов, а также подтвердить эффективность проводимых мероприятий по снижению загрязнения микотоксинами.
Особое значение имеет контроль за загрязнением микотоксинами при характеристике качества сырья и продуктов, импортируемых из других стран. С целью профилактики алиментарных микотоксикозов основное внимание следует уделять зерновым культурам. В связи с этим необходимо соблюдать следующие меры по предупреждению загрязнения зерновых культур и зернопродуктов:
- Своевременная уборка урожая с полей, его правильная агротехническая обработка и хранение.
- Санитарно-гигиеническая обработка помещений и ёмкостей для хранения.
- Закладка на хранение только кондиционного сырья.
- Определение степени загрязнения сырья и готовых продуктов.
- Выбор способа технологической обработки в зависимости от вида и степени загрязнения сырья.
Токсины грибов
Аматоксины

Аматоксины, также аманитотоксины — группа органических соединений, представляют собой циклические пептиды (октапептиды), состоящие из восьми аминокислотных остатков. Все токсины аманита содержат γ-гидроксилированные аминокислоты, что является условием их токсичности[42]. Чрезвычайно токсичны, сильнейшие гепатотоксины, поражают клетки печени (гепатоциты), вызывая их некроз, и тем самым представляют большую угрозу здоровью и жизни человека при интоксикации.
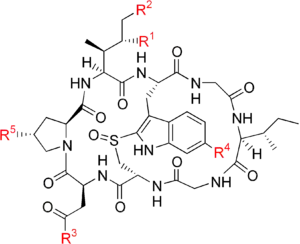
Всего известно десять видов аматоксинов, представленных в виде таблицы[43]:
| Название | R1 | R2 | R3 | R4 | R5 |
|---|---|---|---|---|---|
| α-Аманитин | OH | OH | NH2 | OH | OH |
| β-Аманитин | OH | OH | OH | OH | OH |
| γ-Аманитин | H | OH | NH2 | OH | OH |
| ε-Аманитин | H | OH | OH | OH | OH |
| Амануллин | H | H | NH2 | OH | OH |
| Амануллиновая кислота | H | H | OH | OH | OH |
| Аманинамид | OH | OH | NH2 | H | OH |
| Аманин | OH | OH | OH | H | OH |
| Проамануллин | H | H | NH2 | OH | H |
Источниками аматоксинов являются некоторые виды грибов рода Аманита (бледная поганка, белая поганка, весенняя поганка и др.), Галерина (галерина окаймлённая и др.) и Лепиота или Чешуйница (лепиота коричнево-красная, лепиота каштановая, лепиота розоватая и др.). Наиболее распространённые и смертельно опасные грибы, содержащие аматоксины:
 Лепиота коричнево-красная (Lepiota brunneoincarnata) — один из наиболее смертельно опасных грибов своего рода.
Лепиота коричнево-красная (Lepiota brunneoincarnata) — один из наиболее смертельно опасных грибов своего рода. Галерина окаймлённая (Galerína margináta), смертельно ядовитый гриб.
Галерина окаймлённая (Galerína margináta), смертельно ядовитый гриб. Белая поганка или белый мухомор — один из смертельно опасных видов грибов рода Аманита.
Белая поганка или белый мухомор — один из смертельно опасных видов грибов рода Аманита. Лепиота каштановая, ещё один смертельно опасный гриб, содержащий большое количество аматоксинов.
Лепиота каштановая, ещё один смертельно опасный гриб, содержащий большое количество аматоксинов. Бледная поганка (Amanita phalloides), самый распространённый на Земле смертельно ядовитый гриб рода Аманита (Мухомор)[44][45]. Впервые аматоксины были обнаружены именно в этом грибе, откуда и получили своё название. Один гриб способен накапливать до 10 мг аматоксинов — смертельную дозу для взрослого человека[46].
Бледная поганка (Amanita phalloides), самый распространённый на Земле смертельно ядовитый гриб рода Аманита (Мухомор)[44][45]. Впервые аматоксины были обнаружены именно в этом грибе, откуда и получили своё название. Один гриб способен накапливать до 10 мг аматоксинов — смертельную дозу для взрослого человека[46]. Лепиота розоватая (Lepiota subincarnata) смертельно ядовитый гриб[47].
Лепиота розоватая (Lepiota subincarnata) смертельно ядовитый гриб[47].
Все аматоксины — СДЯВ, с ярко выраженным цитотоксическим воздействием. Вызывают деструкции (разрушения) клеток желудка и особенно энтероцитов кишечника. Наиболее чувствительными к воздействию аматоксинов являются клетки печени и почек. Однако воздействие происходит медленно. Минимальная летальная доза колеблется от 0,1 мг (α-аманитин) до 7 мг/кг тела человека.
Фаллотоксины
Фаллотоксины, также фаллоидины — группа органических соединений, представляют собой циклические гептапептиды, состоящие из 7-ми аминокислотных остатков, соединённые мостиками боковых цепей остатков триптофана и цистеина. За исключением указанных остатков все аминокислоты имеют L-конфигурацию[48]. Фаллотоксины относятся к ингибиторам цитоскелета и блокируют его ремоделирование. Все фаллоидины это чрезвычайно токсичные вещества, которые проявляют гепатотоксическое воздействие, посредством поражения клеток паренхимы печени (некрозы). Отличаются более быстрым периодом токсического воздействия на неё и латентным периодом, а также менее токсичные (ЛД50 фаллоидина ~ 1,9 мг/кг, остальные 9-12 мг/кг), нежели аматоксины. Встречаются вместе с аматоксинами в плодовых телах грибов рода Аманита (Мухомор).

Известные виды фаллотоксинов представлены в виде таблицы:
| Название | R1 | R2 | R3 | R4 |
|---|---|---|---|---|
| Фаллацин | CH2CH(OH)(CH3)2 | CH(CH3)2 | CH(OH)COOH | OH |
| Фаллацидин | CH2C(OH)(CH3)CH2OH | CH(CH3)2 | CH(OH)COOH | OH |
| Фаллизацин | CH2C(OH)(CH2OH)2 | CH(CH3)2 | CH(OH)COOH | OH |
| Фаллизин | CH2C(OH)(CH2OH)2 | CH3 | CH(OH)CH3 | OH |
| Фаллоидин | CH2C(OH)(CH3)CH2OH | CH3 | CH(OH)CH3 | OH |
| Фаллоин | CH2CH(OH)(CH3)2 | CH3 | CH(OH)CH3 | OH |
| Профаллоин | CH2CH(OH)(CH3)2 | CH3 | CH(OH)CH3 | H |
Болесатин

Болесатин представляет собой гликопротеин, с молекулярной массой ~63 кДа, обнаруженный и выделенный из плодовых тел сатанинского гриба (Boletus satanas). Является термолабильным (неустойчивым к нагреванию) ингибитором белкового синтеза[49][50]. Относится к группе рибосомо-инактивирующих белков, токсинов, встречающихся в бактериях и растениях.
Чрезвычайно токсичен, ингибирует синтез белков и ДНК посредством гидролиза нуклеотидов, поражает органы ЖКТ, сильнейший гематический токсин, вызывает обширные тромбозы и гемостаз в печени и почках млекопитающих[51]. ЛД50 = 3,3 мг/кг (мыши, перорально).
Отравление болесатином возникает при употреблении сырых плодовых тел сатанинского гриба. Симптомы отравления наступают в среднем после 6 часов лантентного периода и включают в себя: диспепсию, тошноту, сильную рвоту, повышение температуры, абдоминальную боль, острый гастроэнтерит, геморрагический синдром, понос с кровью, возможно возникновение гепатита с тромботическим поражением сосудов печени и почечной недостаточностью[52][53][54][55].
Гиромитрин

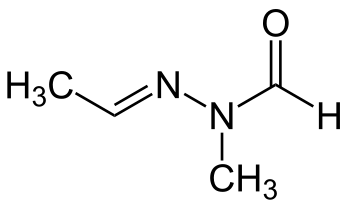
Гиромитрин (N'-этилиден-N-метилформогидразид) — азотсодержащее органическое вещество, производное гидразина, обладает высокой токсичностью и канцерогенностью. Найден в плодовых телах сумчатых грибов рода Строчок (Gyromitra). Гиромитрин нестабилен и легко гидролизуется до чрезвычайно токсичного соединения монометилгидразина. Монометилгидразин (ММН) действует на центральную нервную систему, вызывает гемолиз эритроцитов и нарушает обмен витамина В6. Отравление приводит к тошноте, спазмам желудка и диарее, в то время как тяжёлое отравление может привести к судорогам, желтухе или даже коме или смерти. Было показано, что воздействие монометилгидразина является канцерогенным для мелких млекопитающих. Токсичность гиромитрина сильно варьируется в зависимости от исследуемых видов животных. Средняя летальная доза (LD50) составляет 244 мг/кг для мышей, 50-70 мг/кг для кроликов и 30-50 мг/кг для людей[58]. Токсичность в значительной степени обусловлена образующихся в результате гидролиза молекул ММН; около 35 % проглоченного гиромитрина превращается в MMH. На основании этого преобразования было оценено, что ЛД50 ММН для человека составляет 1,6-4,8 мг/кг (дети) и 4,8-8 мг/кг (взрослые)[58].
Меры предосторожности

Отравления грибами часто возникают ввиду неправильного сбора смертельно ядовитых грибов, приняв последние за съедобные. Наибольшую опасность представляет бледная поганка, её плодовые тела могут накапливать высокие дозы смеси чрезвычайно токсичных соединений (аматоксины и фаллотоксины), которые не разрушаются при термической обработке, интересной особенностью плодовых тел этого гриба является приятный вкус. Помимо этого манифестация отравления (первые симптомы) наступает после продолжительного латентного периода, что приводит к серьёзным последствиям с высокой долей вероятности летального исхода, особенно опасно данное отравление для детей.
Во избежание интоксикаций ядовитыми грибами ни в коем случае не рекомендуется сбор плодовых тел неизвестных видов грибов, осуществление сбора проводить только с опытными грибниками.
Фитотоксины

Фитотоксины (от др.-греч. φυτόν — «растение» и τοξικός — «яд», «ядовитый») — токсины, которые образуются и продуцируются растениями. Обычно такие растения принято называть ядовитыми[59]. Являясь продуктами метаболизма растений, фитотоксины порой выполняют защитные функции, отпугивая от них потенциальных консументов (защищают от поедания). Фитотоксины включают большую группу разнообразных органических соединений, как низко-, так и высокомолекулярные: непротеиногенные аминокислоты, гликозиды, алкалоиды, стероиды, изопреноиды, фенольные соединения, лектины, и т. д. Но наиболее встречаемыми и разнообразными по структуре считают алкалоиды.
Фитотоксины проявляют свойства биологических контаминантов.
Все фитотоксины в какой-то степени представляют опасность для здоровья и жизни человека.
Алкалоиды
Алкалоиды — весьма обширный класс азотсодержащих органических соединений, оказывающих самое различное действие на организм человека. Это и сильнейшие яды, и полезные лекарственные средства (обладают сильными физиологическими воздействиями)[60].
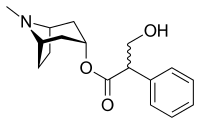 Атропин — алкалоид тропанового ряда, впервые обнаружен в ягодах Красавки обыкновенной или белладонны (от лат. Atrópa belladónna)[61], также встречается в разных частях белены (Hyoscyamus niger) и некоторых видах дурмана (Datura stramonium). Является неселективным м-холинблокатором, вызывает мидриаз (расширение зрачка), снижает слюновыделение (сухость во рту), происходит броноходилатация (расширение просвета бронхов), усиливает сердцебиение (тахикардия), вызывает покраснение кожи лица (т.н. румянец), возбуждает ЦНС (возможны бред, галлюцинации, при сильном отравлении возможны психозы), данные свойства белладоны широко использовали богатые итальянские дамы. Опасным проявлением отравления является паралич дыхания, следствием которого является летальный исход. Отравление происходит при поедании или втирании ягод белладоны. ЛД50 = 300-400 мг/кг.
Атропин — алкалоид тропанового ряда, впервые обнаружен в ягодах Красавки обыкновенной или белладонны (от лат. Atrópa belladónna)[61], также встречается в разных частях белены (Hyoscyamus niger) и некоторых видах дурмана (Datura stramonium). Является неселективным м-холинблокатором, вызывает мидриаз (расширение зрачка), снижает слюновыделение (сухость во рту), происходит броноходилатация (расширение просвета бронхов), усиливает сердцебиение (тахикардия), вызывает покраснение кожи лица (т.н. румянец), возбуждает ЦНС (возможны бред, галлюцинации, при сильном отравлении возможны психозы), данные свойства белладоны широко использовали богатые итальянские дамы. Опасным проявлением отравления является паралич дыхания, следствием которого является летальный исход. Отравление происходит при поедании или втирании ягод белладоны. ЛД50 = 300-400 мг/кг.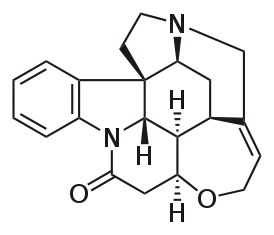 Стрихнин — алкалоид индолового ряда, впервые обнаружен и выделен из рвотных орешков — семян растения чилибу́хи (Strychnos nux-vomica). Чрезвычайно токсичное вещество, нейротоксичной природы, является антагонистом глициновых рецепторов ЦНС. При отравлении симптоматическая картина напоминает столбняк: происходит возбуждение ЦНС, возможны генерализованные судороги мышц — тетания, дыхательный паралич и смерть от остановки дыхания или асфиксии[62]. LD50 ~ 1 мг/кг.
Стрихнин — алкалоид индолового ряда, впервые обнаружен и выделен из рвотных орешков — семян растения чилибу́хи (Strychnos nux-vomica). Чрезвычайно токсичное вещество, нейротоксичной природы, является антагонистом глициновых рецепторов ЦНС. При отравлении симптоматическая картина напоминает столбняк: происходит возбуждение ЦНС, возможны генерализованные судороги мышц — тетания, дыхательный паралич и смерть от остановки дыхания или асфиксии[62]. LD50 ~ 1 мг/кг.
Гликозиды

Гликозиды — представляют собой органические соединения, состоящих из двух компонентов — одного или более углеводного остатка (молекул пиранозного или фуранозного цикла) и неуглеводного компонента или агликона. Гликозиды разнообразны по строению и образуют довольно обширную группу производных углеводов. Многие растительные гликозиды ядовиты, обладают высокой биологической активностью, особенно на мышцы сердца, поэтому некоторые из них, например, ландыша, наперстянки или строфанта (Strophanthus kombe) используют в качестве лекарственных препаратов в очень низких концентрациях (так называемая группа сердечных гликозидов).
Цианогенные гликозиды
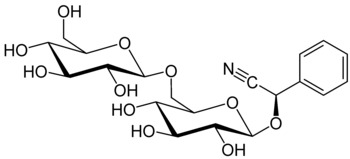
Цианогенные гликозиды — это гликозиды некоторых цианогенных альдегидов и кетонов, которые при ферментативном или кислотном гидролизе выделяют очень ядовитую синильную кислоту HCN, вызывающую общетоксическое и поражение нервной системы.
Из представителей цианогенных гликозидов целесообразно отметить линамарин, содержащийся в белой фасоли, льне и маниоке, и амигдалин, который обнаружен в косточках некоторых растений семейства розовых (Rosaceae) — миндаля (до 8 %), персиков, слив, абрикос (от 4 до 6 %).
Амигдалин представляет собой сочетание дисахарида генциобиозы и агликона, включающего остаток синильной кислоты и бензальдегида.
Линамарин является гликозидом ацетонциангидрина, в качестве углеводной части выступает молекула глюкозы.
Лектины
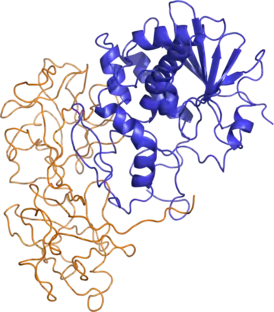
Лектины — группа веществ гликопротеидной природы с молекулярной массой от 60 до 120 тысяч дальтон. Они широко распространены в семенах и других частях растений. Лектины обнаружены в бобовых, арахисе, проростках растений, а также в икре рыб.
Лектины обладают способностью: повышать проницаемость стенок кишечника для чужеродных веществ; нарушать всасывание нутриентов; вызывать агглютинацию (склеивание) эритроцитов крови. С этим связано их негативное действие при высоких концентрациях. Некоторые лектины чрезвычайно токсичны, например, лектин из семян клещевины (Ricinus communis) — рицин[64], а также лектины некоторых животных и микроорганизмов, в частности холерный токсин.
Непротеиногенные аминокислоты
Некоторые непротеиногенные аминокислоты являются токсичными, из-за их способности к имитации структур протеиногенных аминокислот, такие, как тиализин. Другие же подобны структурам аминокислотам-нейромедиаторам, они обладают нейротоксичностью, например, квискваловая кислота, канаванин и азетидин-2-карбоновая кислота[65].
Канаванин
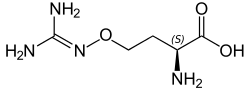
Канаванин — непротеиногенная аминокислота, структурный аналог аргинина. Обнаружен в некоторых растениях семейства бобовых (например, в семенах и ростках люцерны), при употреблении в больших количествах у человека может вызвать симптомы системной красной волчанки[66].
Механизм токсичности канаванина заключается в том, что организмы, потребляющие его, обычно по ошибке включают его в свои собственные белки вместо L-аргинина, тем самым синтезируются структурно аберрантные белки, которые могут не функционировать должным образом.
Меры предосторожности

Ядовитые растения часто путают с неядовитыми, ввиду морфологических сходств некоторых частей. Особенно часто сходства наблюдаются в строении побегов, цветков или плодов. Неопытные сборщики могут легко перепутать несъедобные и ядовитые растения с лекарственными и используемых в пищу, и тем самым подвергнут своё или здоровье близких риску отравления или даже смерти. Например, ягоды очень ядовитого и смертельно опасного вороньего глаза имеют большое сходство с ягодами черники. Часто плоды ядовитых растений имеют прекрасный запах и вполне съедобный вид, однако, такая обманчивость может быть очень опасной, как, например, с плодами манцинеллового дерева[67] или ягодами клещевины. Поэтому не следует собирать ягоды, плоды, семена или другие части растений, для использования в гастрономических целях, если они неизвестны и встречаются впервые.
Зоотоксины и токсины морских беспозвоночных
Зоотоксины от (др.-греч. ζῷον — «животное», «живое существо» и τοξικός — «ядовитый») — токсины, продуцируемые животными, в частности позвоночными (рыбы, земноводные, рептилии, птицы, млекопитающие), такие животные являются ядовитыми по аналогии с растениями. Токсины морских беспозвоночных рассматриваются обычно отдельно. Среди зоотоксинов, наиболее часто встречаемые контаминанты это токсины рыб.
Нейротоксины моллюсков

Отравление нейротоксичными моллюсками связано с употреблением в пищу мидий, устриц, морских гребешков или сердцевидок. Двустворчатые моллюски становятся ядовитыми после питания определёнными динофлагеллятами или цианобактериями. Парализующим токсином моллюска (PSP) является сакситоксин.
Действие сакситоксина проявляется у людей в виде сердечно-сосудистого коллапса и паралича дыхания. Он блокирует распространение нервных импульсов без деполяризации, и нет никакого известного противоядия. Он устойчив к высокой температуре, растворим в воде, не разрушается при варке. Он может быть разрушен кипячением в течение 3-4 ч при pH 3,0.
Признаки синдрома PSP развиваются в течение 2 ч после приема пищи ядовитых моллюсков, они характеризуются парестезией (покалывание, нечувствительность или жжение), которая начинается со рта, губ и языка, которая позднее распространяется по лицу, голове и шее к кончикам пальцев руки ног. Смертность по разным данным колеблется от 1 до 22 %.
Тетродотоксин
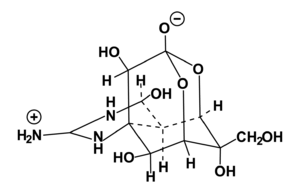
Тетродотоксин представляет собой органическое вещество, небелковый токсин с сильнейшим нервно-паралитическим действием, плохо растворим в воде, хорошо в неполярных органических растворителях. Впервые был обнаружен и выделен в 1909 году японским химиком Ёшизуми Тахара[68] из печени бурой собаки-рыбы (Takifugu rubripes), входящей в отряд четырёхзубообразные (Tetraodontiformes), откуда и происходит название токсина. Смертельная доза для человека составляет менее чем 0,1 мг. Токсин накапливается главным образом в печени, яичниках и икре рыб семейства иглобрюхие, включая и смертоносную собаку-рыбу. Исследования показали, что иглобрюхи не способны вырабатывать нейротоксин, а лишь аккумулируют его в своём организме. Изначально тетродотоксин вырабатывается морскими бактериями, которые затем поедаются разнообразными живыми организмами.
Токсическое воздействие

Тетродотоксин относится к сильнейшим природным нейротоксинам. Его действие обусловлено воздействием на натриевые каналы нейронов, ингибируя их путём изменения структуры (не позволяет проникать ионам натрия внутрь клеток), токсин делает процесс передачи нервного импульса по нервным волокнам невозможным, что приводит к параличу мышц[69]. Токсин легко всасывается в кишечнике в кровь, проникает через практически любые тканевые барьеры, во все внутренние органы, включая головной мозг, может накапливаться в сердце и почках.
Картина отравления сходна с сакситоксином. Сначала развивается онемение, зуд языка, нёба, губ, возникают боли в животе, тошнота, рвота, понос, затем происходит тремор и угнетение мышечного движения, дисфагия, афония и потеря сознания, смерть возникает в результате дыхательной недостаточности, вызванной параличом мышц участвующих в дыхании и поражении блуждающего нерва (n.vagus). Противоядия не существует. Активный антагонист более токсичный батрахотоксин, использовать которого не является целесообразным (минимальная летальная составляет порядка 20 мкг). Лечение при отравлении только симптоматическое, единственная возможность спасти отравившегося человека состоит в искусственном поддержании работы дыхательной и кровеносной систем до тех пор, пока не закончится действие яда. Минимальные концентрации токсина, вызывающие токсические эффекты составляют порядка 0,01-0,02 мг.
Меры предосторожности

Мясо иглобрюхов в Японии и странах Юго-Восточной Азии считается деликатесным, знаменитое блюдо фугу, приготавливают именно из них, особенно вкусным получается из мяса бурого скалозуба. Но несмотря на все необходимые меры безопасности приготовления этого экзотического блюда с эффектом онемения губ и языка, каждый год в Японии регистрируют несколько десятков отравлений. В странах Юго-Восточной Азии (особенно в Таиланде) количество отравлений намного больше (до нескольких сотен) учитывая, что в большинстве случаев рыбы вылавливаются и приготавливаются без должных мер безопасности, имеется высокий риск смертельного отравления. Вследствие этого не рекомендуется приобретать мясо фугу на рыбных рынках.
 Тарелка с fugu sashimi
Тарелка с fugu sashimi Fugu no Shirako
Fugu no Shirako Fugu no ransou nukazuke, Blowfish Ovaries Pickled in Rice-Bran Paste
Fugu no ransou nukazuke, Blowfish Ovaries Pickled in Rice-Bran Paste
Токсоплазма и токсоплазмоз
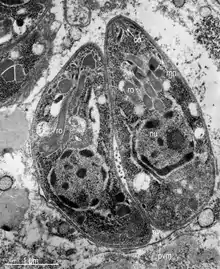
Токсоплазмоз. Эта болезнь вызывается токсоплазмой Toxoplasma gondii, кокцидиозным простейшим, которое является облигатным внутриклеточным паразитом. Родовое название основывается на характерной форме амёбной стадии простейшего (от греч. τόξο — токсо, «дуга»). Впервые он был выделен в 1908 г. от африканского грызуна гонди, откуда и пошло его видовое название. В большинстве случаев попадание ооцист T. gondii в организм человека алиментарным путём не вызывает характерных симптомов, или инфекция является самоизлечивающейся. В этих случаях простейшее инцистируется и становится латентным. Однако когда иммунокомпетентный статус ослаблен, опасный для жизни токсоплазмоз проявляется в результате обострения латентной инфекции. Домашние и дикие кошки — единственные окончательные хозяева (носители) кишечной или половой фазы этого организма, что делает их первичными источниками токсоплазмоза человека. Обычно болезнь передается от кошки к кошке, но фактически все позвоночные животные восприимчивы к ооцистам, распространяющимся кошками. Доза в 100 ооцист может вызвать клинический токсоплазмоз у человека, и ооцисты могут оставаться жизнеспособными более года в тёплой сырой окружающей среде[71]. Свиньи — главный источник токсоплазмоза среди животной пищи для человека.
Химические контаминанты

К химическим или антропогенным контаминантам относят разнообразные химические соединения или их смеси, чужеродного происхождения (являются результатом деятельности человека — ксенобиотиками), обладающие высокой биологической активностью, присутствие которых в пищевых продуктах может серьёзно ухудшить здоровье или даже привести к смерти людей. Подразделяются на две группы: неорганические и органические (составляют большую часть). Примером таких соединений являются метанол, аммиак, формальдегид, неорганические соединения мышьяка, соединения бериллия, некоторые соединения тяжёлых металлов (бария, кадмия, сурьмы, меди, свинца, таллия, ртути итд.), поверхностно-активные вещества (моющие средства или детергенты), пестициды (например, хлорорганические: группы альдрина, гексахлоран, ДДТ; паракват; фосфорорганические: фосдрин, ДФФ, тиофос и др.) и минеральные удобрения (основу, которых составляют нитраты), нефтепродукты (топливо, синтетические масла, бензол и ряд его производных, и другие ароматические соединения), органические растворители, фенолы и их производные (в частности, фенолформальдегидные смолы), эпоксид этилена, пластмассы и некоторые полимеры (ПВХ, поливинилиденхлорид и т. д.), искусственные пищевые и непищевые красители, лаки и краски, продукты сгорания биомассы, диоксины и диоксинподобные соединения, канцерогены антропогенного происхождения (полициклические ароматические углеводороды — бензпирен, бензантрацен, ДМБА, ароматические амины и др.) и многие другие.
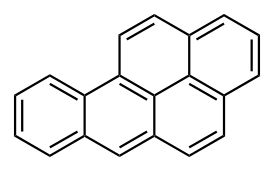 Бензпирен, широко распространённый полициклический ароматический углеводород, канцероген, мутаген. Образуется в результате процессов риформинга, происходящих при сжигании бытовых отходов, нефтепродуктов, табачного дыма, выхлопных газов, а также при термической обработке мяса[72][73].
Бензпирен, широко распространённый полициклический ароматический углеводород, канцероген, мутаген. Образуется в результате процессов риформинга, происходящих при сжигании бытовых отходов, нефтепродуктов, табачного дыма, выхлопных газов, а также при термической обработке мяса[72][73].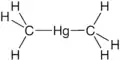 Диметилртуть — ртутьорганическое соединение, чрезвычайно токсична[74], обладает биоаккумуляцией в морских животных, но особенно в рыбе, вызывает тяжёлое поражение ЦНС — болезнь Минамата.
Диметилртуть — ртутьорганическое соединение, чрезвычайно токсична[74], обладает биоаккумуляцией в морских животных, но особенно в рыбе, вызывает тяжёлое поражение ЦНС — болезнь Минамата. Пентахлорфенол — гербицид и десикант. Высокотоксичный. Обладает политропным воздействием на организм человека, в первую очередь поражает нервную систему и клетки миелоидной ткани. Сильный ирритант, при попадании на открытые участки кожи вызывает ожоги и поражения кожи, сходные с хлоракне. ЛД100 для человека составляет 1,5-1,7 г.
Пентахлорфенол — гербицид и десикант. Высокотоксичный. Обладает политропным воздействием на организм человека, в первую очередь поражает нервную систему и клетки миелоидной ткани. Сильный ирритант, при попадании на открытые участки кожи вызывает ожоги и поражения кожи, сходные с хлоракне. ЛД100 для человека составляет 1,5-1,7 г.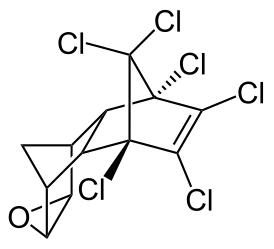 Эндрин — хлорорганическое соединение с необычайно сильным инсектицидным действием, а также чрезвычайно токсичное вещество, вызывает сильнейшую интоксикацию, поражение печени и в особенности ЦНС[75].
Эндрин — хлорорганическое соединение с необычайно сильным инсектицидным действием, а также чрезвычайно токсичное вещество, вызывает сильнейшую интоксикацию, поражение печени и в особенности ЦНС[75]. Бензол — простейший ароматический углеводород, один из самых распространённых ксенобиотиков. Токсичен, сильный канцероген, обладает мутагенными свойствами, миелотоксичен (поражает красный костный мозг)[76][77].
Бензол — простейший ароматический углеводород, один из самых распространённых ксенобиотиков. Токсичен, сильный канцероген, обладает мутагенными свойствами, миелотоксичен (поражает красный костный мозг)[76][77]. Метанол — одноатомный спирт, сильный яд, вызывающий поражение зрения (дегенерацию зрительного нерва) в небольших дозах (5-15 мл), в больших кому и летальный исход (30-50 мл)[78][79].
Метанол — одноатомный спирт, сильный яд, вызывающий поражение зрения (дегенерацию зрительного нерва) в небольших дозах (5-15 мл), в больших кому и летальный исход (30-50 мл)[78][79].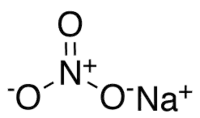 Нитрат натрия, вместе с нитратами калия и аммония, являются наиболее используемыми азотными удобрениями в сельском хозяйстве. Поступают в организм человека с овощами и в меньшей степени с фруктами и ягодами, которые накапливают нитраты в своих плодах. Овощи (особенно корнеплоды), содержащие большие количества нитрата натрия или других нитратов, вследствие окисления в организме человека (фермент нитратредуктаза) до более токсичных нитритов, вызывают серьёзные расстройства и нарушения работы со стороны органов ЖКТ, а также метгемоглобинемию со стороны системы крови[80].
Нитрат натрия, вместе с нитратами калия и аммония, являются наиболее используемыми азотными удобрениями в сельском хозяйстве. Поступают в организм человека с овощами и в меньшей степени с фруктами и ягодами, которые накапливают нитраты в своих плодах. Овощи (особенно корнеплоды), содержащие большие количества нитрата натрия или других нитратов, вследствие окисления в организме человека (фермент нитратредуктаза) до более токсичных нитритов, вызывают серьёзные расстройства и нарушения работы со стороны органов ЖКТ, а также метгемоглобинемию со стороны системы крови[80].(1%252C4)dioxine_200.svg.png.webp) 2,3,7,8-Тетрахлородибензодиоксин, сокр. ТХДД — органическое бифункциональное соединение (хлорорганический циклический эфир), представитель полихлорированных дибензодиоксинов (ПХДД), чрезвычайно токсичен, одно из самых токсичных веществ антропогенного происхождения (ЛД50 = 0,5 мкг/кг морская свинка (перорально)). Сильный мутаген, доказанный канцероген[81], обладает ярко выраженным тератогенным воздействием, снижает деятельность эндокринной и репродуктивной системы.
2,3,7,8-Тетрахлородибензодиоксин, сокр. ТХДД — органическое бифункциональное соединение (хлорорганический циклический эфир), представитель полихлорированных дибензодиоксинов (ПХДД), чрезвычайно токсичен, одно из самых токсичных веществ антропогенного происхождения (ЛД50 = 0,5 мкг/кг морская свинка (перорально)). Сильный мутаген, доказанный канцероген[81], обладает ярко выраженным тератогенным воздействием, снижает деятельность эндокринной и репродуктивной системы.
Тяжёлые металлы, мышьяк и их соединения
В так называемую группу тяжёлых металлов входят металлы с плотностью более 8 г/см3 и атомной массой более 40 а. е. м.. Однако с точки зрения медицины и экотоксикологии тяжёлыми металлами считаются металлы, которые обладают высокой биологической активностью, в частности, токсичностью и способностью внедрения в пищевые цепи. К таким металлам относятся:
- Свинец
- Кадмий
- Ртуть
- Таллий
- Сурьма
- Барий
- Медь
- Хром
- Цинк и их соединения.
Помимо данных элементов в группу входят: Мышьяк, Бериллий и Алюминий. Два последних элемента по плотности и атомной массе нельзя отнести к тяжёлым металлам, однако, бериллий и особенно его растворимые соединения обладают высокой токсичностью.
Ртуть и её соединения

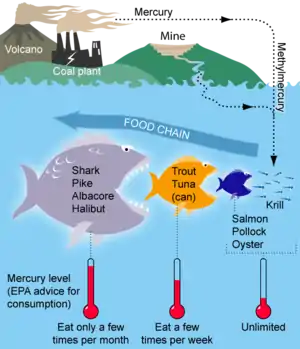
Ртуть — один из самых опасных и высокотоксичных элементов, обладающий способностью накапливаться в растениях и в организме животных и человека, то есть являющийся ядом кумулятивного действия.
В организм человека ртуть поступает в наибольшей степени с рыбопродуктами, в которых её содержание может многократно превышать ПДК.
Токсичность ртути зависит от вида её соединений, которые по-разному всасываются, метаболизируются и выводятся из организма. Наиболее токсичны алкилртутные соединения с короткой углеродной цепью — метилртуть, этилртуть, диметилртуть. Механизм токсического действия ртути связан с её взаимодействием с сульфгидрильными группами белков (SH-группы). Блокируя их, ртуть изменяет свойства или инактивирует ряд жизненно важных ферментов. Неорганические соединения ртути нарушают обмен аскорбиновой кислоты, пиридоксина, кальция, меди, цинка, селена, а органические — обмен белков, цистеина, аскорбиновой кислоты, токоферолов, железа, меди, марганца, селена. Защитным эффектом при воздействии ртути на организм человека обладают цинк и особенно селен. Предполагают, что защитное действие селена обусловлено деметилированием ртути и образованием нетоксичного соединения — селено-ртутного комплекса. Человек получает с суточным рационом около 0,05 мг ртути, что соответствует рекомендациям ФАО/ВОЗ.
Мясо рыбы отличается наибольшей концентрацией ртути и её соединений, поскольку активно аккумулирует их из воды и корма, в который входят различные гидробионты, богатые ртутью. Например, хищные пресноводные рыбы могут содержать от 107 до 509 мкг/кг, нехищные пресноводные рыбы — от 78 до 200 мкг/кг, а океанские нехищные рыбы — от 300 до 600 мкг/кг Hg. Организм рыб способен синтезировать метилртуть, которая накапливается в печени. У некоторых видов рыб в мышцах содержится белок — металлотионеин, который с различными металлами, в том числе и с ртутью, образует комплексные соединения, способствуя тем самым накапливанию ртути в организме и передаче её по пищевым цепям. У таких рыб содержание ртути достигает очень высоких концентраций: рыба-сабля содержит её от 500 до 20 000 мкг/кг, а тихоокеанский марлин — от 5000 до 14 000 мкг/кг. Для других продуктов характерно следующее содержание ртути (в мкг/кг) — в продуктах животноводства: мясо — 6-20, печень — 20-35, почки — 20-70, молоко — 2-12, сливочное масло — 2-5, яйца — 2-15; в съедобных частях сельскохозяйственных растений: овощи — 3-59, фрукты — 10-124, бобовые — 8-16, зерновые — 10-103; в шляпочных грибах — 6-447, в перезрелых — до 2000 мкг/кг, причём, в отличие от растений, в грибах может синтезироваться метилртуть. При варке рыбы и мяса концентрация ртути в них снижается, при аналогичной обработке грибов — остается неизменной. Это различие объясняется тем, что в грибах ртуть связана с аминогруппами азотсодержащих соединений, в рыбе и мясе — с серосодержащими аминокислотами.
Болезнь Минаматы
Наиболее печально известные примеры массового отравления ртутью были вызваны именно метилртутью CH3Hg+. В 1953 году в Японии у 121 жителя побережья в бухте Минамата было зафиксировано заболевание, сопровождавшееся ломотой в суставах, нарушением слуха и зрения. Это заболевание, вошедшее в литературу под названием «болезнь Минаматы», закончилась смертью для почти трети больных.
В дальнейшем в 1959 году удалось установить, что эта болезнь вызывается употреблением в пищу рыбы, отравленной ртутью в форме хлорида CH3HgCl, сбрасываемого химическим предприятием (Chicco corp.) прямо в воды залива. Концентрация ртути была настолько велика, что рыба погибала; поедавшие эту рыбу птицы падали прямо в море, а отведавшие отравленной пищи кошки передвигались, «кружась и подпрыгивая, зигзагами и коллапсируя». К 1954 году популяция кошек в этих местах заметно снизилась. Однако до 1959 года никаких замеров ртутного загрязнения вод залива в этом районе не проводилось (мониторинг отсутствовал).
Интенсивное расследование позволило установить, что на заводе по производству ацетальдегида и уксусной кислоты из ацетилена (по реакции Кучерова) ртутные отходы (в виде отработанного сульфата ртути HgSO4) сбрасывались в реку, впадающую в бухту Минамата. При этом ртуть, о чём первоначально и не подозревали, микробиологическим путём превращалась в метилртуть, которая через планктон, моллюсков и рыб в конце концов попадала в пищу. В этом цикле ртуть постепенно концентрировалась и в конце пищевой цепи, дойдя до человека, достигала токсической концентрации. Загрязнение в устье канала сточными водами было настолько сильным, что измеренные значения концентраций составили 2 кг ртути на тонну отложений.
Свинец и его соединения

Acetate.jpg.webp)
Свинец — один из самых распространённых и опасных экотоксикантов. История его применения очень древняя, что связано с относительной простотой его получения и большой распространённостью в земной коре (1,6·10−3 %). Соединения свинца — Pb3O4 и PbSO4 — основа широко применяемых пигментов: сурика и свинцовых белил. Глазури, которые используются для покрытия керамической посуды, также содержат соединения Pb. Металлический свинец со времён Древнего Рима применяют при прокладке водопроводов. В настоящее время перечень областей его применения очень широк: производство аккумуляторов, электрических кабелей, химическое машиностроение, атомная промышленность, производство эмалей, замазок, лаков, хрусталя, пиротехнических изделий, спичек, пластмасс и т. п. Мировое производство свинца составляет более 11,2 млн тонн в год. В результате производственной деятельности человека в природные воды ежегодно попадает более 1 млн тонн, а в атмосферу в переработанном и мелкодисперсном состоянии выбрасывается около 700 тыс. тонн, подавляющее большинство которого оседает на поверхности Земли.
Токсичность свинца
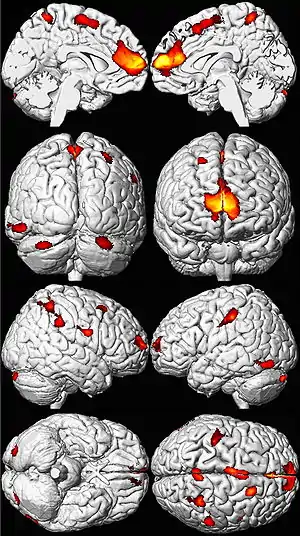
Механизм токсического действия свинца имеет двойную направленность. Во-первых, блокада функциональных SH-групп белков и, как следствие, инактивация ферментов, во-вторых, проникновение свинца в нервные и мышечные клетки, образование лактата свинца, затем фосфата свинца, которые создают клеточный барьер для проникновения ионов Са2+.
Свинцовая интоксикация может приводить к серьёзным нарушениям здоровья, проявляющимся в частых головных болях, головокружениях, повышенной утомляемости, раздражительности, ухудшении сна, мышечной гипотонии, а в наиболее тяжёлых случаях к параличам и парезам, умственной отсталости. Неполноценное питание, дефицит в рационе кальция, фосфора, железа, пектинов, белков (или повышенное поступление кальциферола) увеличивают усвоение свинца, а следовательно, его токсичность. Среднесмертельная доза свинца составляет 500 мг для взрослого человека, и менее 150 мг для детей.
Свинец в пищевых продуктах
Свинец обнаруживается в питьевой воде и некоторых пищевых продуктах.
Ежедневное поступление свинца в организм человека колеблется от 70 до 400 мкг. Основной источник поступления соединений свинца в организм — пища, преимущественно растительная. Поступление свинца в организм человека с питьевой водой составляет лишь несколько процентов от того количества свинца, которое вводится с пищей и воздухом. Основной источник свинца в воде — сплавы, используемые при соединении водопроводных труб. Имеются доказательства того, что содержание свинца в хлорированной водопроводной воде больше, чем в нехлорированной.
Отравления свинцом иногда носит массовый характер, например, в 2019 году в Бангладеш соединения свинца были добавлены в куркуму, чтобы сделать её более жёлтой[85]. Считается, что это началось в 1980-х и продолжается до сих пор.
Мышьяк и его соединения как котаминанты пищевых продуктов
Мышьяк как элемент в чистом виде ядовит только в высоких концентрациях. Он принадлежит к тем микроэлементам, необходимость которых для жизнедеятельности организма человека не доказана, а его соединения, такие как мышьяковистый ангидрид, арсениты и арсенаты, сильно токсичны. Мышьяк содержится во всех объектах биосферы (в земной коре — 2 мг/кг, морской воде — 5 мкг/кг). Известными источниками загрязнения окружающей среды мышьяком являются электростанции, использующие бурый уголь, медеплавильные заводы; он используется при производстве полупроводников, стекла, красителей, инсектицидов, фунгицидов и др.
Нормальный уровень содержания мышьяка в продуктах питания не должен превышать 1 мг /кг. Так, например, фоновое содержание мышьяка (в мг/кг): в овощах и фруктах — 0,01-0,2; в зерновых — 0,006-1,2;
в говядине — 0,005-0,05; в печени — 2,0; яйцах — 0,003-0,03; в коровьем молоке — 0,005-0,01. Повышенное содержание мышьяка отмечается в рыбе и других гидробионтах, в частности в ракообразных и моллюсках.
По данным ФАО/ВОЗ, в организм человека с суточным рационом поступает в среднем 0,05-0,45 мг мышьяка. ДСД — 0,05 мг/кг массы тела.
В зависимости от дозы мышьяк может вызывать острое и хроническое отравление; разовая доза мышьяка 30 мг — смертельна для человека. Механизм токсического действия мышьяка связан с блокированием SH-групп белков и ферментов, выполняющих в организме разнообразные функции.
Пестициды в пищевых продуктах
Пестициды — вещества различной химической природы, применяемые в сельском хозяйстве для защиты культурных растений от сорняков, вредителей и болезней, то есть химические средства защиты растений. Мировое производство пестицидов (в пересчёте на активные вещества) составляет более 2 млн тонн в год, причём эта цифра непрерывно растёт. В настоящее время в мировой практике используют около 10 тыс. наименований пестицидных препаратов на основе 1500 действующих веществ, которые относятся к различным химическим группам. Наиболее распространены следующие: хлорорганические, фосфорорганические, карбаматы (производные карбаминовой кислоты), ртутьорганические, синтетические пиретроиды и медьсодержащие фунгициды. С гигиенических позиций принята следующая классификация пестицидов:
- по токсичности при однократном поступлении через желудочно-кишечный тракт пестициды делятся на сильнодействующие ядовитые вещества (ЛД50 до 50 мг/кг), высокотоксичные (ЛД50 от 50 до 200 мг/кг), среднетоксичные (ЛД50 от 200 до 1000 мг/кг), малотоксичные (ЛД50 более 1000 мг/кг);
- по кумулятивным свойствам пестициды делятся на вещества, обладающие сверхкумуляцией (коэффициент кумуляции меньше 1), выраженной кумуляцией (коэффициент кумуляции от 1 до 3), умеренной кумуляцией (коэффициент кумуляции от 3 до 5), слабовыраженной кумуляцией (коэффициент кумуляции больше 5);
- по стойкости пестициды делятся на очень стойкие (время разложения на нетоксичные компоненты свыше 2 лет), стойкие (от 0,5 до 1 года), умеренно стойкие (от 1 до 6 месяцев), малостойкие (1 месяц).
Нарушения гигиенических норм хранения, транспортировки и применения пестицидов, низкая культура работы с ними приводят к их накоплению в кормах, продовольственном сырье и пищевых продуктах, а способность аккумулироваться и передаваться по пищевым цепям — к их широкому распространению и негативному влиянию на здоровье человека. Применение пестицидов и их роль в борьбе с различными вредителями в повышении урожайности сельскохозяйственных культур, их влиянии на окружающую среду и здоровье человека вызывают неоднозначные оценки различных специалистов.
Пестициды группы альдрина

Пестициды группы альдрина — хлорорганические соединения, полихлорциклодиены, производные альдрина, одни из самых опасных веществ, представляют серьёзную угрозу здоровью человека и окружающей среде. Все производные альдрина — высокотоксичные вещества (для некоторых групп животных чрезвычайно токсичные, например, для холоднокровных — рыб, земноводных, пресмыкающихся, особенно в виде аэрозоля), химические контаминанты, обладающие свойствами биоаккумуляции, отравляя тем самым пищевые цепи и устойчивостью к биохимическому разложению. Несмотря на токсичность, пестициды этой группы обладают необычайно высокой инсектицидной, а также гербицидной активностью[75], превосходя ДДТ и гексахлоран. По решению Стокгольмской конвенции от 23 мая 2001 года альдрин и его производные признаны стойкими органическими загрязнителями и имеют глобальный запрет на производство, использование и реализацию[86]. Несмотря на запрет Стокгольмской конвенции, дильдрин до сих пор производится и применяется в качестве инсектицида в некоторых странах: например, в Малайзии, Венесуэле, Таиланде, некоторых странах Африки.
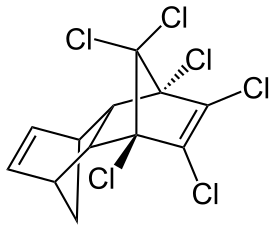 Альдрин
Альдрин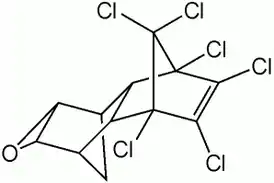 Дильдрин
Дильдрин Эндрин
Эндрин
Токсичность
Все производные альдрина — СДЯВ, нейротоксичной природы, имеются данные о бластомогенном действии альдрина. Имеются ярко выраженные мутагенные эффекты у дильдрина и эндрина. По своей токсичности некоторые производные (эндрин) близки к цианидам.
| ЛД50 мг/кг | Альдрин | Дильдрин | Эндрин |
|---|---|---|---|
| Мыши (перорально) | 50 мг/кг | 20-22,5 мг/кг | 9,5-10 мг/кг |
| Кролики (перорально) | 55-58 мг/кг | 12-15 мг/кг | 7-10 мг/кг. |
| Человек (ЛД100, аэрозоль) | 12 мг/кг | 8 мг/кг | <5 мг/кг |
| Форель (ЛК50) | 0,00005 мг/л | 0,000035 мг/л | 0,00073 мг/л |
Наибольшая токсичность пестицидов группы альдрина проявляется в газообразном или аэрозольном состоянии. Альдрин и его производные возможно использовать в качестве БОВ (в виде аэрозолей). Большинство пестицидов этой группы хорошо проникают через кожу.
Фитотоксичность
Растения, обработанные альдрином или его производными могут накапливать (кумулировать) их в довольно больших концентрациях, особенно это выражено у растений семейства Мятликовых (Poaceae).
Массовые отравления эндрином в Пакистане
С 14 июля по 26 сентября 1984 года длилась вспышка отравлений эндрином в 21 деревне района Талаганг провинции Пенджаб в Пакистане, в результате которой пострадало более 190 человек, 80 % составили дети в возрасте до 15 лет, 19 человек погибли. Отравление сопровождалось сильнейшими судорогами, рвотой, отёками лёгких и гипоксии. У людей, имеющих высокую температуру тела, рвота проявлялась в меньшей степени, чем у имеющих более низкую или нормальную. Большинству пострадавших была оказана медицинская помощь[87].
Причиной отравлений являлось загрязнение эндрином сельскохозяйственной культуры, употребляемой в пищу — сахарного тростника, в то же время наблюдались отравления людей, имеющих дело с хлопчатником. Ряд водителей грузовиков, перевозивших в провинцию Талаганг этот пестицид, утверждают, что скорее всего загрязнение сельскохозяйственных культур произошло при транспортировке[87].
Бензол и его производные как контаминанты

Бензол будучи одним из наиболее синтезируемых органических соединений (более 60 миллионов тонн в год (оценка на 2019)), при этом является и высокоопасным для здоровья человека веществом. Токсичность бензола долгое время была недооценённой. Бензол обладает политропным воздействием, с преимущественно миелотоксичным и мутагенным эффектами. Хроническое воздействие бензолом может увеличить риск возникновения злокачественных новообразований системы крови, клеток паренхимы печени и лимфоидной ткани. Наиболее чувствительны к бензолу клетки активно делящихся тканей — миелоидной и лимфоидной, так как он обладает радиомиметичностью (сходством с ионизирующим излучением). ЛД100 для человека составляет около 55-70 мл, минимальные летальные дозы могут быть намного меньше — 15-17 мл. Бензол в организме человека в большей степени подвергается биотрансформации в печени, где и происходит образование высокореакционных продуктов.
Трансформация бензола в клетках печени и миелоидной ткани
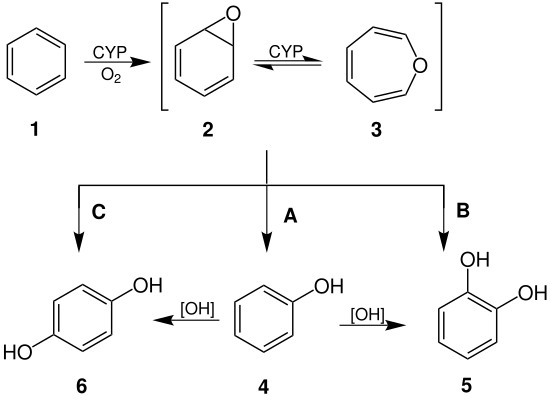
Попав в клетки печени (гепатоциты) или миелоидной ткани бензол претерпевает биотрансформацию, происходящую при участии фермента цитохрома P450, которая приводит к образованию высоко реакционноспособных соединений (эпоксид и оксид бензола) и генерирует свободные радикалы, вследствие активации цитохрома P450 (образуются в первую очередь активные формы кислорода). Конечным продуктом биотрансформации бензола является фенол. Реакция протекает по уравнению:
Цит Р450 + NADPH + H- + O2 → Цит Р450 + NADP+ + HOOH.
HOOH → 2ОH·
C6H6 + 2ОH· → C6H5OH + Н2О.
Образовавшиеся активные формы кислорода способны повреждать клетки миелоидной ткани, которые очень чувствительны к такому роду воздействию (оксидативный стресс). Это приводит к дегенерации и деструкции миелоидной ткани, которые имеют очень серьёзные последствия (миелодисплазии, апластическая анемия и лейкозы)[76]. Повреждения миелоидной ткани ведёт к дисфункциям, сопряжённой с ней иммунной системы.
Таким образом бензол проявляет радиомиметический эффект (эффект сходный с воздействием ионизирующего излучения).
Эпоксид и оксид бензола имеют высокое угловое напряжение связей -С-О-С- и легко превращаются в электрофильные молекулы, посредством разрыва данных связей. Образованные электрофильные молекулы легко образуют прочные ковалентные связи с нуклеофильными центрами аминогрупп в молекулах нуклеиновых кислот (реакция нуклеофильного замещения SN2), в частности, с нуклеотидами ДНК, образовавшиеся продукты носят названия ДНК-аддуктов (например, N7-фенилгуанин). ДНК-аддукты изменяют структуру нативной молекулы ДНК, таким образом, что происходит невозможность протекания нормальных процессов удвоения (репликации) и транскрипции. Это в свою очередь приводит к повреждениям участков ДНК (генотоксичность), образованию мутантных белков, торможению апоптоза, подавлению экспрессии некоторых белков-антионкогенов (вплоть до утраты) и в конечном итоге возможна трансформация клеток (малигнизация) или смерть (некроз). Таким образом, продукты окисления бензола проявляют мутагенные и канцерогенные свойства. К тому же оксид является довольно токсичным веществом.
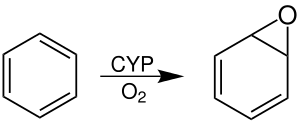
Накопление продуктов окисления бензола, крайне негативно сказывается на целостности клеток. Активные формы кислорода могут начать процесс перекисного окисления липидов и перегрузить антиоксидантную систему. Помимо этого в больших концентрациях бензол может разрушать биомембраны клеток, посредством солюбилизации и растворения липидного бислоя. Хроническое воздействие продуктов окисления бензола увеличивают риск возникновения злокачественных опухолей системы крови и паренхимы печени.
Бензол в пищевых продуктах
Впервые большие дозы бензола были обнаружены в газированных напитках ещё в 1990 г. в США (Perrier).
Фенолы
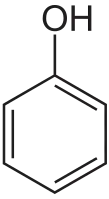 Фенол или гидроксибензол.
Фенол или гидроксибензол. Пирокатехин или 1,2-дигидроксибензол.
Пирокатехин или 1,2-дигидроксибензол.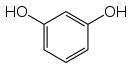 Резорцин или 1,3-дигидроксибензол.
Резорцин или 1,3-дигидроксибензол.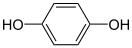 Гидрохинон или 1,4-дигидроксибензол.
Гидрохинон или 1,4-дигидроксибензол. Пара-крезол или 1-метил-4-гидроксибензол.
Пара-крезол или 1-метил-4-гидроксибензол.
Фенолы отличаются от спиртов значительно более сильными кислотными свойствами. В водных растворах едких щелочей образуют соли — феноляты, которые гидролизуются водой и разлагаются кислотами, образуя свободные фенолы. На воздухе фенолы постепенно окисляются. Фенолы отличаются значительным разнообразием — от практически нетоксичных до весьма токсичных. Часть одноатомных фенолов — сильные нейротоксины, поражают печень, почки, проникают через кожу; однако высшие члены ряда в производственных условиях мало опасны. Многоатомные фенолы при длительном поступлении в организм нарушают ферментативные процессы.
Токсичность фенолов зависит от строения, положения и количества радикалов, от растворимости в воде и жирах. В порядке повышения токсичности они располагаются следующим образом: пирогаллол—резорцин—фенол—крезолы—ксиленолы—нитрофенолы—нафтолы—гидрохинон—хлорфенолы.
Фенолы способны накапливаться в рыбах и передаваться по трофической цепи. В наибольшем количестве они обнаруживаются в печени, а затем (в порядке уменьшения) в жабрах, почках, селезёнке, мышцах и кишечнике. При остром отравлении карпов и форели (10 мг/л) содержание фенолов составляло в печени 119 мг/кг, в жабрах 17,7, внутренних органах 7,9; при хроническом отравлении (0,02-0,07 мг/л) — 2,0-3,0 мг/кг. В реках, не загрязненных фенолом, в теле плотвы его содержание составляло 0,3 мг/кг.
Обратимость фенольной интоксикации высокая, так как соединения фенола распадаются или выводятся из организма в течение 1-2 суток, а некоторые соединения сохраняются несколько недель. Рыба приобретает фенольный запах и вкус при содержании в воде смеси фенола и крезолов 0,02-0,03 мг/л, хлорфенолов 0,015-0,001 мг/л, а также после поедания загрязнённых кормовых объектов (тубифацид, хирономид).
Фенольная катастрофа в Уфе Наглядным примером воздействия фенола на окружающую среду стал случай весной 1990 года в Уфе. В результате техногенной аварии на предприятии ПО «Уфахимпром» произошла утечка большого количества фенола в речку Шугуровка, впадающую в более крупную реку Уфу, являющуюся источником хозяйственно-питьевого водоснабжения города Уфы. Загрязнение воды в районе Южного водозабора превышало ПДК более чем в 100 раз. Опасность загрязнения питьевой воды фенолом проявляется в том, что при очистке вод использовался хлор, который, взаимодействуя с фенолом, образовывал хлорпроизводные (смесь хлорфенолов) — более токсичные вещества (некоторые в 100—250 раз превышают токсичность самого фенола). Население Уфы было оповещено об опасности употребления водопроводной воды для питья. Общая численность населения, потреблявшего питьевую воду, загрязненную фенолом из Южного водозабора Уфы, составила 672 876 человек[88].
Диоксины в пищевых продуктах

Диоксины представляют собой бифункциональные органические высокотоксичные соединения (некоторые, как, например, ТХДД — чрезвычайно токсичные), обладающие политропным воздействием, с ярко выраженными мутагенными, канцерогенными, иммунодепрессивными, эмбриотоксическими и тератогенными свойствами. Диоксины — твёрдые вещества, без вкуса и наличия запаха, гидрофобные и нерастворимые в воде (растворимость составляет 10−12−10−13 г/мл), однако хорошая растворимость проявляется в неполярных растворителях и липофильных веществах. Реакционная способность у диоксинов очень низкая, они не взаимодействуют с водой, растворами кислот и щелочей, окислителями. Температуры разложения диоксинов лежат в пределах от 800 до 1100° С. Поэтому они обладают высокой устойчивостью в окружающей среде и могут оставаться неизменными многие годы, особенно в почве (более 10 лет). Особую опасность диоксины как экотоксиканты представляют живым существам, так как они могут накапливаться в организмах животных (в жировой ткани), тем самым способствуют хроническому отравлению и миграции по цепи питания. Ещё большую опасность для здоровья и жизни человека представляет накопление диоксинов в пищевых продуктах, в основном животного происхождения (мясе, печени, рыбе, яйцах, молоке итд.), реже они встречаются в растительном масле, овощных консервах и питьевой воде.
Большой вклад (более 97-98 %) в генерации диоксинов вносит человеческая деятельность, однако и природные процессы, такие, как массовые лесные пожары, способны к генерации диоксинов, но в гораздо меньшей степени. Диоксины образуются в результате производства пестицидов, гербицидов, деятельности мусоросжигающих заводов, функционирования объектов деревообрабатывающей, целлюлозно-бумажной, химической, нефтехимической промышленности, хлорирования воды в бассейнах и др. Особенно опасны аварийные ситуации, связанные с пожарами. По мнению ВОЗ, в более 90 % случаев влияние диоксинов на людей происходит через пищевые продукты.
Примером экстремального роста уровня диоксинов в питьевой воде могут служить события, случившиеся в Уфе в 1989—1990 гг. и потом ставшие известными, как крупнейшая экологическая катастрофа СССР — фенольная катастрофа. Анализ образцов вод, отобранных 21 апреля 1990 года, то есть спустя 3-4 недели после начала событий, был выполнен в Научном центре по разработке и внедрению современных методов молекулярной диагностики (НЦМД, Москва). Были найдены следующие концентрации диоксинов (в нг/л), превышавшие предел обнаружения использованной аппаратуры и потому зафиксированные.
| Место взятия проб | Общее содержание диоксинов (нг/л) | Содержание ТХДД (нг/л) |
|---|---|---|
| Территория ПО «Уфахимпром» | 26,92 | 8 |
| р. Уфа (южный водозабор) | 38,4 | 7,6 |
| Верхняя зона № 2 машинного зала | 17 | 7,4 |
| Водоразборная колонка на ул. Ахметова | 13,78 | ~ 1,15 |
В бывшем СССР на то время действовала лишь одна норма — содержание диоксинов в любых водах не должно было превышать 0,26 пг/л.
Оценки показали, что даже 3-4 недели спустя после начала событий содержание диоксинов в воде в тысячи раз превышало допустимые уровни того времени:
- территория ПО «Химпром» — в > 100000 раз,
- Река Уфа — в > 147000 раз,
- верхняя зона № 2 машинного зала (южный водозабор) — в > 23000 раз,
- водоразборная колонка на ул. Ахметова — в > 53000 раз.
Токсичность и механизмы действия

Диоксины токсичны при любых концентрациях. В малых дозах (менее 100 нг/кг) они вызывают мутагенный эффект, отличаются кумулятивными свойствами, ингибируют различные ферментные системы организма. Опасность кумуляции диоксинов заключается в том, что новые дозы, попавшие в организм извне могут вызвать молниеносные формы отравления в ничтожных количествах (менее 100 нг/кг).
Острые токсические дозы наблюдаются уже при концентрации 100-2000 нг/кг, манифестируют процессы снижения лимфо- и лейкопоэза, снижается процесс деления сперматоцитов, в клетках лимфоидной, миелоидной, а также в гепатоцитах и селезёнки появляется оксидативный стресс, из-за торможения всасывания и метаболизма витаминов A и E, уровни глутатиона имеют довольно низкие значения. В сублетальных дозах (более 10000-50000 нг/кг) наблюдается поражение практически всех внутренних органов (ЖКТ, почек, ЦНС, итд.) и желёз внутренней секреции (тимус, щитовидная железа, гонады), селезёнки, печени, кожи (хлоракне), происходят изменения в составе крови, ликвора, быстро падает уровень лимфоцитов, снижаются обменные процессы, антиоксидантная защита, поражается миелоидная ткань и лимфоидная ткань, появляются морфологические изменения в структуре клеток Лейдига и сперматоцитов итд. Дозы диоксинов в больших концентрациях (более 70000-90000 нг/кг), полученных за относительно короткий промежуток времени смертельно опасны.
Источники, содержание в пищевых продуктах, система менеджмента безопасности
Источниками поступления диоксинов в организм человека являются продукты питания (до 95 %), воздух (3,5 %), почва (1,3 %), вода (0,001 %). Признано недопустимым присутствие диоксинов в продуктах питания, воздухе и питьевой воде. Однако достичь этого практически невозможно. Пороговые дозы и нормы — это условность.
Суммарное суточное поступление диоксинов в организм человека с продуктами питания в Германии составляет 79 пг, в Японии — 63 пг, в Канаде — 92 пг, в США — 119 пг. В основных пищевых продуктах рекомендован допустимый уровень диоксинов — от 0,75 до 4 нг/кг (в пересчёте на жиры). В ряде продуктов их содержание не допускается (в пределах обнаружения существующих методов). Допустимые уровни содержания диоксинов в основных пищевых продуктах в России (СанПиН 2.3.2.2401-08) и ВОЗ представлены в таблице Гигиенические нормативы диоксинов в пищевых продуктах гармонизированы с зарубежными значениями (ВОЗ).
Полициклические ароматические углеводороды


Полициклические ароматические углеводороды (сокр. ПАУ) — особый класс ароматических углеводородов, представляющие серьёзную угрозу пищевой безопасности и здоровью человека. Несмотря на это, большинство ПАУ не обладают высокой токсичностью или канцерогенностью (>65 %), однако, имеются несколько десятков довольно распространённых соединений, которые могут иметь очень мощный канцерогенный эффект, вызывать мутагенез, и при этом являться очень ядовитыми.
ПАУ образуются в результате процессов высокотемпературной деструкции и риформинга биологической массы, особенно при жарке мяса (включая и рыбу) и мясных продуктов (например, барбекю или шашлыка из мяса, с повышенным содержанием жиров или холестерина).
Долговременное потребление продуктов с повышенным содержанием ПАУ может иметь риск развития онкологических заболеваний ЖКТ, в меньшей степени лёгких и половой системы.
Некоторые канцерогенные ПАУ
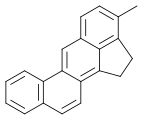
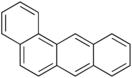

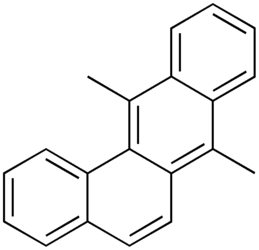
pyrene.svg.png.webp) Дибензо(а,i)пирен
Дибензо(а,i)пирен
Радиоактивные контаминанты

Радиоактивные контаминанты представляют собой особую группу, которая включает природные радиоактивные элементы (уран, торий, радий, полоний, протактиний и многие другие) и их соединения, а также радионуклиды антропогенного происхождения, таких, как например, короткоживущий изотоп 131I (Т1/2 = 8 суток), и более продолжительно живущие 90Sr (Т1/2 ~ 29,15 лет), 137Cs (Т1/2 ~ 30,2 лет).
Основные негативные биологические эффекты радиоактивных контаминантов проявляются в высокой ионизации пищевых продуктов, так как большинство живых клеток высокочувствительны к ней (в особенности это клетки активно делящихся тканей — миелодной, лимфоидной, слизистых оболочек и половых желёз). Радиоактивные соединения, попадают внутрь организма вместе с контаминированными продуктами, где в результате ионизации и избыточного образования токсичных перекисных соединений, возникают цепные реакции сильно перегружающие антиоксидантную систему, что приводит к негативным последствиям, например, к таким, как серьёзные поражения органов ЖКТ (особенно печени, так как в ней происходят процессы депонирования и обезвреживание образовавших токсичных продуктов). Вместе с тем происходят процессы снижения или подавления репродуктивной функции (гипоспермия, азоспермия, бесплодие и др.), мутагенез и тератогенез, снижение функций эндокринной системы (например, в щитовидной железе селективно депонируется радиоизотоп йод-131), накопление в мышцах, костных тканях и дальнейшее усиление дегенерации миелоидной ткани, как следствие — лучевая болезнь, лейкозы и другие злокачественные новообразования системы гемопоэза (кроветворения), соединительных тканей (кости, хрящи, суставы итд.), а также сердечно-сосудистой, эндокринной и половой систем. Особенно опасен в этом отношении остеотропный стронций-90, который легко замещает кальций в костях, тем самым повышается риск возникновения их ломкости (остеомаляция, остеопороз), а также приводит к возникновению радиогенной остеосаркомы (вследствие высокой активности). Бóльшую опасность представляет хроническое (долговременное) воздействие радиоактивных контаминантов.
В последние десятилетия уровень радионуклидов в атмосфере непрерывно повышается, это связано прежде всего с увеличением производства ядерного топлива и возникновением катастроф на АЭС (прежде всего это Чернобыльская катастрофа 1986 года и катастрофа 2011 года японской атомной станции Фукусима-1).
Контаминация пищевых продуктов
Контаминация пищевых продуктов — процесс загрязнения контаминантами, приводящий к нецелесообразности употребления, порчи и изменениям органолептических свойств продуктов (изменение вкуса, внешнего вида, консистенции, запаха, цвета и, как следствие снижение пищевой ценности) и повышения опасности для здоровья и жизни, в случае алиментарного применения данных продуктов.
Существует большое количество путей поступления контаминантов из внешней среды в сырьё и пищевые продукты. Основные из них:
- Почвенный, таким путём в растительное сырьё и сельскохозяйственные продукты проникают нитраты, тяжёлые металлы и их соединения, хлорорганические пестициды, диоксины, радионуклиды.
- Водный, примером служат наличие вируса гепатита в питьевой воде или пресноводные и морские виды рыб, а также морепродукты (крабы, моллюски и др.) которые способные накапливать тяжёлые металлы, пестициды, нефтепродукты, ПАВ, ртутьорганические соединения, и многие другие контаминанты
- Воздушный, характерен для процессов возделывания сельскохозяйственных культур, которые могут поглощать из воздуха многие токсичные вещества — диоксины, нитрозные газы, аммиак, формальдегид и многие другие.
Помимо указанных путей, контаминанты могут проникать в пищевые продукты и во время технологической обработки. Следовательно, контаминация может происходить практически на всех этапах производства, хранения и транспортировки (реализации) пищевых продуктов.
Также возможна преднамерная и диверсионная контаминация, направленные на устранение нежелательных физических лиц (путём отравления пищевых продуктов биологическими агентами, радионуклидами или боевыми отравляющими веществами, например, отравление Литвиненко полонием-210, отравление Ющенко диоксинами) и нанесение серьёзного урона продовольственной безопасности государству (используются также различные биологические, химические или радиоактивные контаминанты).
Действия контаминантов на организм человека


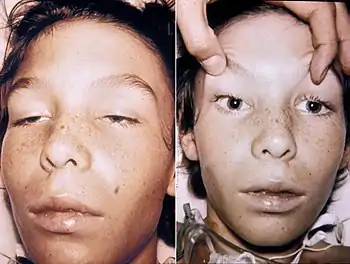

На организм человека, действия оказываемые контаминантами, подразделяются на:
- ближайшие — проявляются в виде острых токсикозов (пищевых отравлений, например, вызванные повышенным содержанием в продуктах питания нитратов или микотоксинов) или инфекционными заболеваниями (сальмонеллёз, ботулизм, амёбиаз, холера итд.), аллергических и специфических иммуннологических реакциях (ангионевротический отёк, бронхоспазм, анафилаксия, агглютинация);
- отдалённые или дистанционные — иммуносупрессивное, канцерогенное, мутагенное, тератогенное или политропное воздействие (множественное) на органы, систему органов или даже на весь организм человека (апластическая анемия, хронический афлатоксикоз, болезнь Минамата, итд.).
Количественной характеристикой токсического воздействия контаминантов является ЛД50. По токсическому воздействию (значения ЛД50 даны в мг/кг) контаминанты делятся на:
- Низкотоксичные (слаботоксичные) (>1500)
- Умеренно-токсичные (1500—150)
- Высокотоксичные (150-15)
- Чрезвычайно токсичные (<15).
Большую опасность представляют высокотоксичные и чрезвычайно токсичные контаминанты, которые могут оказывать негативные воздействия в крайне низких концентрациях (10−2—10−6 кг и менее на кг веса).
Патофизиологические эффекты, оказываемые контаминантами
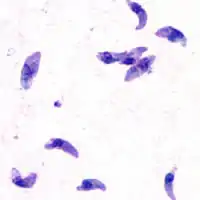 Токсоплазма (Toxoplasma gondii) — самый распространённый паразит-простейшее, который может попадать в организм человека через пищевые продукты (животного происхождения). Вызывает токсоплазмоз, который приводит к тератогенному эффекту (уродства), олигофрении, поражениям нервной системы или гибели плода, у взрослых в острой форме протекает подобно брюшному тифу, с увеличением некоторых внутренних органов (печени, селезёнки), температурой или с поражением нервной системы, может протекать и бессимптомно. Токсоплазмы также обладают свойствами изменять сознания организма носителя.
Токсоплазма (Toxoplasma gondii) — самый распространённый паразит-простейшее, который может попадать в организм человека через пищевые продукты (животного происхождения). Вызывает токсоплазмоз, который приводит к тератогенному эффекту (уродства), олигофрении, поражениям нервной системы или гибели плода, у взрослых в острой форме протекает подобно брюшному тифу, с увеличением некоторых внутренних органов (печени, селезёнки), температурой или с поражением нервной системы, может протекать и бессимптомно. Токсоплазмы также обладают свойствами изменять сознания организма носителя.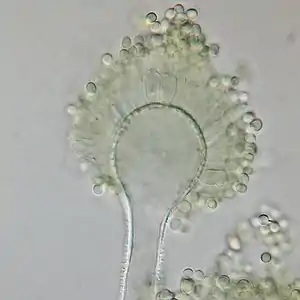 Аспергилл жёлтый (Aspergillus flavus) или просто жёлтая плесень, один из самых распространённых (организм-космополит) токсинообразующих плесневых грибов-микромицетов. Продуцирует сильнейшие гепатоканцерогены и гепатотоксины — афлатоксины, опасен и патогенен для животных и человека[92]. Контаминирует многие пищевые продукты и сырьё, но в основном растительного происхождения (субстратом служат продукты с повышенным содержанием крахмала и растительных масел — зерновые, бобовые, масличные культуры, некоторые виды сухофруктов итд.). Токсинообразование происходит при довольно высоких значениях влажности и температуры[93].
Аспергилл жёлтый (Aspergillus flavus) или просто жёлтая плесень, один из самых распространённых (организм-космополит) токсинообразующих плесневых грибов-микромицетов. Продуцирует сильнейшие гепатоканцерогены и гепатотоксины — афлатоксины, опасен и патогенен для животных и человека[92]. Контаминирует многие пищевые продукты и сырьё, но в основном растительного происхождения (субстратом служат продукты с повышенным содержанием крахмала и растительных масел — зерновые, бобовые, масличные культуры, некоторые виды сухофруктов итд.). Токсинообразование происходит при довольно высоких значениях влажности и температуры[93]. Нераскрывшийся плод Аки (Blighia sapida) содержит гипоглицин[94] — высокотоксичное вещество, которое может привести к сильному отравлению, к т.н. Ямайской рвотной болезни.
Нераскрывшийся плод Аки (Blighia sapida) содержит гипоглицин[94] — высокотоксичное вещество, которое может привести к сильному отравлению, к т.н. Ямайской рвотной болезни. Бледная поганка (Amanita phalloides) может быть очень похожа на некоторые виды съедобных грибов (например, на шампиньоны или сыроежки), для неё характерен приятный вкус. Однако гриб содержит в себе токсины, которые не разрушаются при термической обработке и обладают сильнейшей гепатотоксичностью, вызывают дегенерацию, разрушение и некролитическую смерть клеток печени. Опасностью отравления является долгий период бессимптомного протекания (более 10 часов). Летальный исход при отравлении бледной поганкой довольно высок.
Бледная поганка (Amanita phalloides) может быть очень похожа на некоторые виды съедобных грибов (например, на шампиньоны или сыроежки), для неё характерен приятный вкус. Однако гриб содержит в себе токсины, которые не разрушаются при термической обработке и обладают сильнейшей гепатотоксичностью, вызывают дегенерацию, разрушение и некролитическую смерть клеток печени. Опасностью отравления является долгий период бессимптомного протекания (более 10 часов). Летальный исход при отравлении бледной поганкой довольно высок. Тихоокеанские устрицы (Magallana gigas) могут накапливать в себе смертельно опасные дозы нейротоксичных соединений (от 400 мкг до 15000-25000 мкг), главным из которых является сакситоксин. Помимо этого, у некоторых групп людей, при поедании мяса устриц (оно содержит специфические антигены), провоцируется сильная и скоротечная аллергенная реакция — анафилаксия, которая может стать причиной летального исхода.
Тихоокеанские устрицы (Magallana gigas) могут накапливать в себе смертельно опасные дозы нейротоксичных соединений (от 400 мкг до 15000-25000 мкг), главным из которых является сакситоксин. Помимо этого, у некоторых групп людей, при поедании мяса устриц (оно содержит специфические антигены), провоцируется сильная и скоротечная аллергенная реакция — анафилаксия, которая может стать причиной летального исхода.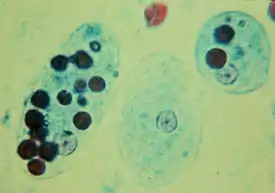 На микрофотографии представлена одна из форм дизентерийной амёбы — трофозоиты, которые поглощают эритроциты крови. Дизентерийная амёба (Entamoeba histolytica) — опасный биологический контаминант, попав во внутрь толстого кишечника она, приступает к разрушению слизистой оболочки кишечника, вызывая кровотечения, диарею, деструкцию (разрушение) слизистой и некролитические процессы (язвы, отторжения слизистой, гнойное поражение, некрозы).
На микрофотографии представлена одна из форм дизентерийной амёбы — трофозоиты, которые поглощают эритроциты крови. Дизентерийная амёба (Entamoeba histolytica) — опасный биологический контаминант, попав во внутрь толстого кишечника она, приступает к разрушению слизистой оболочки кишечника, вызывая кровотечения, диарею, деструкцию (разрушение) слизистой и некролитические процессы (язвы, отторжения слизистой, гнойное поражение, некрозы). Спорынья (Claviceps purpurea), паразитирующая на колосе ржи. Хлеб, выпеченный из муки, контаминированной алкалоидами спорыньи (лизергиновая кислота, эрготамин, эргин (лизергамид), эргометрин и др.)[95][96] вызывает сильнейшее отравление — эрготизм.
Спорынья (Claviceps purpurea), паразитирующая на колосе ржи. Хлеб, выпеченный из муки, контаминированной алкалоидами спорыньи (лизергиновая кислота, эрготамин, эргин (лизергамид), эргометрин и др.)[95][96] вызывает сильнейшее отравление — эрготизм. Клещевина обыкновенная (Ricinus communis), красивое декоративное растение, однако, её семена содержат сильнейший белковый фитотоксин — рицин. При поедании семян возникает сильнейшая интоксикация с гемолитическим и геморрагическим синдромом, поражается кишечник и сосуды (нарушается целостность стенок, образуются тромбы, снижается кровоток итд.), как следствие гемолитическая анемия, угнетается деятельность ЦНС, возникает тотальное падение артериального давления, летальный исход происходит почти в 100% случаев интоксикаций. Сырьё или жмых, контаминированный рицином также смертельно опасен и для домашних животных (крупный и мелкий рогатый скот, лошади).
Клещевина обыкновенная (Ricinus communis), красивое декоративное растение, однако, её семена содержат сильнейший белковый фитотоксин — рицин. При поедании семян возникает сильнейшая интоксикация с гемолитическим и геморрагическим синдромом, поражается кишечник и сосуды (нарушается целостность стенок, образуются тромбы, снижается кровоток итд.), как следствие гемолитическая анемия, угнетается деятельность ЦНС, возникает тотальное падение артериального давления, летальный исход происходит почти в 100% случаев интоксикаций. Сырьё или жмых, контаминированный рицином также смертельно опасен и для домашних животных (крупный и мелкий рогатый скот, лошади). Смертоносная бурая собака-рыба (Takifugu rubripes) или просто фугу. Её некоторые внутренние органы чрезвычайно токсичны из-за высокого содержания в них тетродотоксина (TDX), сильнейшего нейротоксина. Блюда, которые готовят из фугу в Японии являются деликатесом. Неправильно приготовленное фугу, мясо которого содержит небольшие количества ТDX каждый год вызывает сильнейшие отравления и уносит десятки жизни людей[97].
Смертоносная бурая собака-рыба (Takifugu rubripes) или просто фугу. Её некоторые внутренние органы чрезвычайно токсичны из-за высокого содержания в них тетродотоксина (TDX), сильнейшего нейротоксина. Блюда, которые готовят из фугу в Японии являются деликатесом. Неправильно приготовленное фугу, мясо которого содержит небольшие количества ТDX каждый год вызывает сильнейшие отравления и уносит десятки жизни людей[97].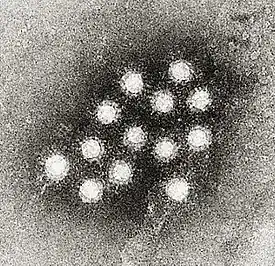 Вирус гепатита А (НVA), возбудитель вирусного гепатита А (болезнь Боткина), РНК-содержащий вирус относится к семейству Picornaviridae[98]. Данный вирус высококонтагиозный (опасен для человека, так как может вызвать гепатит в большинстве случаев заражения), обладает высокой устойчивостью к действию хлора, поэтому способен проникать в водопроводную воду через барьеры водоочистных сооружений[99].
Вирус гепатита А (НVA), возбудитель вирусного гепатита А (болезнь Боткина), РНК-содержащий вирус относится к семейству Picornaviridae[98]. Данный вирус высококонтагиозный (опасен для человека, так как может вызвать гепатит в большинстве случаев заражения), обладает высокой устойчивостью к действию хлора, поэтому способен проникать в водопроводную воду через барьеры водоочистных сооружений[99]. Тихоокеанский голубой тунец (Thunnus orientalis) — один из основных источников ртутьорганических соединений. Мясо тунца, как и многих морских хищных рыб может накапливать большие дозы метилртути (от 1500 до 20000 мкг/кг).
Тихоокеанский голубой тунец (Thunnus orientalis) — один из основных источников ртутьорганических соединений. Мясо тунца, как и многих морских хищных рыб может накапливать большие дозы метилртути (от 1500 до 20000 мкг/кг).
Наиболее частые патофизиологические эффекты, оказываемые контаминантами:
- Токсичность — свойство негативно влиять на физиологические и биохимические процессы, протекающих в нормальных клетках, результатом которого является обратимые или необратимые изменения, нарушения или даже ингибирование (подавление) данных процессов, и как следствие смерть клеток и организма в целом. Многие, если не большинство контаминантов обладают токсичностью. Токсичность зависит от целого ряда физиологических и токсико-химических факторов, главные из которых, возраст, пол, количество токсичных веществ поступивших в организм, период действия, период выведения, тропность, комплексообразование, способность к гидролизу, биоаккумуляция, тканевая или органная специфичность и другие.
- Альтеративный воспалительный процесс — нарушения целостности структуры клеток т.е их повреждения, возникающие в результате воздействия биологических агентов и/или химических соединений (включая радиоактивные) и, последующие за ними некролитический путь смерти, деструктивных клеток. Многие контаминанты обладают альтеративным эффектом.
- Канцерогенное воздействие или канцерогенность — свойство химических и радиоактивных соединений или их смесей, а также биологических агентов, включая вирусы вызывать злокачественные заболевания организма человека. К этой группе относятся ПАУ, которые образуются в результате термической обработки (при жарке) мяса и продуктов из неё (копчённости), нитрозамины[100](образуются из нитратов и нитритов), ароматические амины, диоксины и диоксибензофураны (в частности 2,3,7,8-ТХДД), соединения мышьяка, кадмия и шестивалентного хрома, афлатоксины, бензол, стронций-90.
- Мутагенное воздействие или мутагенность — свойство негативного воздействия химических соединений, физических факторов или биологических агентов на генетический аппарат клеток, следствием которого являются мутации. Генотоксичность — предельная форма мутагенности, при которой происходят нарушения целостности структуры молекул ДНК (вследствие встраивания ксенобиотических молекул в молекулу ДНК — ковалентного или интеркаляции), вплоть до утраты генов или деструкции (разрушения). Часто мутагены могут быть канцерогенами и/или тератогенами. Многие диоксины, и в особенности ТХДД являются сильными мутагенами, такими же свойствами обладают многие ароматические углеводороды и их производные (бензол, ДМБА, метилхолантрен) и органические перекисные соединения.
- Иммуносупрессия или иммунодепрессивный эффект выражается в частичном (вторичные иммунодефицитные состояния или ВИДС) или полном подавлении функций иммунной системы[101][102] (например, иммунодефицитный микотоксикоз). Данным эффектом обладают многие микотоксины, диоксины, некоторые виды вирусов.
- Тератогенное воздействие — негативный эффект воздействия тератогенов на генетический аппарат плода, результатом, которого являются мутации и аномальные морфологические изменения тела (врождённые уродства). Диоксины обладают высоким тератогенным и эмбриотоксичным воздействием, также этим воздействием обладают охратоксины, многие канцерогены, например, метилхолантрен.
- Аллергическое воздействие — происходит при действии специфических антигенов, вызывающих аллергическую реакцию. Некоторые аллергические реакции могут быть очень быстрыми и опасными для жизни, как, например, анафилаксия. Примером могут служить антигены некоторых видов двустворчатых моллюсков (мидии, устрицы и др.), морских рыб, молока, арахиса, употребляемых в пищу.
- Гепатотоксичность — негативный эффект воздействия некоторых биологических агентов, физических факторов и химических соединений на клетки паренхимы печени — гепатоциты. Выражается в дегенерации и некролитическом процессе гибели клеток паренхимы печени, как следствие гепатиты и цирроз. Гепатотоксичностью обладает некоторые микотоксины (афлатоксины, Т-2 токсин, патулин), токсины бледной поганки, этанол, вирусы гепатита.
- Нейротоксичность — свойство химических соединений негативно влиять (вплоть до летального исхода) на процессы и функции клеток (нейроны) центральной и периферической нервной системы[103]. Одними из следствий такого влияния являются повреждения нервной ткани, судороги, парезы и параличи. Например, метанол обладает нейродегенеративным воздействием на зрительный нерв и необратимо поражает его, также этим воздействием обладают пестициды (группы альдрина, фосфорорганические соединения), некоторые токсины бактерий (ботулотоксин) и беспозвоночных (тетродотоксин, октопотоксины, сакситоксин итд.), ртутьорганические соединения.
- Нефротоксичность — негативный эффект воздействия химических соединений или биологических агентов на структурно-функциональные единицы почки (нефроны), следствием которого являются повреждения нефронов и/или их смерть. Охратоксины, тяжёлые металлы, соединения мышьяка (арсин и др.), аматоксины проявляют нефротоксические свойства.
- Гематотоксичность — негативный эффект от воздействия различных химических соединений (включая радиоактивные) и/или биологических агентов (включая их продукты метаболизма) на функции клеток крови, их качественные характеристики и состав. Например, нитраты и особенно нитриты, а также органические нитросоединения (нитробензол) обладают гематотоксичностью, вызывают резкое падение уровня гемоглобина (метгемоглобинемия) в эритроцитах, переводя его в неактивную для переноса кислорода форму, бензол вызывает лейкопении и гемолитическую анемию, такими же свойствами обладает и анилин, но действует гораздо медленнее. Миелотоксичность является частным случаем гематотоксичности и выражается в негативном эффекте воздействия химических соединений, радионуклидов или биологических агентов на клетки миелоидной ткани красного костного мозга, повреждая их вплоть до полной деструкции (разрушения структур) или трансформации в опухолевые.
- Антибиотическое действие — негативный эффект воздействия на микрофлору кишечника биологически активных соединений, следствием которого является снижение числа бактерий кишечника вплоть до полной стерилизации. Многие антибиотики обладают низкой селективностью, и могут существенно влиять на количество бактериальной микрофлоры, данное свойство крайне негативно сказывается на функционировании ЖКТ (дисбактериоз, диарея, нарушения электролитного баланса, итд.). Помимо антибиотиков, данным эффектов обладают сульфаниламидные препараты, препараты нитрофурана и другие.
- Цитотоксичность — свойство химических соединений, физических факторов и/или биологических агентов негативно воздействовать на определённые виды клеток (например на клетки энтероцитов), вызывая их повреждения или смерть. Таким свойством обладают токсины Коли и токсины бледной поганки.
- Политропия или политропное воздействие, также эффект комбинированного воздействия — негативный эффект воздействия токсичных соединений или биологических агентов на многие органы, систему органов или на весь организм. Включает в себя совокупность разнообразных патофизиологических процессов и поэтому является наиболее опасным для здоровья или жизни человека. Таким свойством обладают некоторые радиоактивные элементы, диоксины, тяжёлые металлы и их соединения (ртуть, свинец, таллий, радий, полоний итд.), некоторые радионуклиды.
Причины контаминации пищевых продуктов
Основные причины, из-за которых возникает контаминация пищевых продуктов это не соблюдение или нарушения, а также отсутствие систем менеджмента безопасности и стандартов качества пищевых продуктов (HACCP, ISO 22000:2005 итд.), ГОСТов, санитарно-гигиенических норм и правил (СанПиН) или иных нормативно-правовых актов, установленных и контролируемых действующим законодательством государства, происходящих при обработке сырья или производстве пищевых продуктов.

Гигиенический аспект контаминации пищевых продуктов непосредственно сопряжён с экономическим. Обеспечение большинства населения стран Африки, Латинской Америки, некоторых стран Азии (Индия, Бангладеш, Индонезия итд.) чистой питьевой водой и продовольственными продуктами является одной из самых сложных проблем. Во многих регионах Африки и Азии, нерациональное использование водных ресурсов (загрязнение воды продуктами жизнедеятельности и/или нефтепродуктами, сложность процесса очистки или вовсе её отсутствие), частое применение пестицидов в сельском хозяйстве, отражается на качестве продуктов питания (низкая пищевая ценность, большое количество контаминантов, как следствие частые интоксикации и высокий уровень смертности), происходят частые инфекционные заболевания (холера, амёбиаз, тиф, кишечные токсоинфекции, итд.), наблюдается низкая осведомлённость населения об использовании чистой питьевой воды (в некоторых регионах Африки она отсутствует) и использовании воды в процессах кулинарной обработки (вода обычно неочищенная (не проходит процессы очистки) и практически не пригодна для употребления, так как содержит большое количество контаминантов различного происхождения).
Экономический аспект также играет важную роль в обеспечении безопасности пищевой продукции и сырья. Наглядный пример демонстрирует корреляция между уровнем потребления контаминированных продуктов афлатоксинами (арахис, зерновые итд.) и заболеваемостью афлатоксикозом, в некоторых странах Африки (где у населения почти в 100 % случаев выявляются циррозное поражение печени и/или рак печени) и западной Европы (единичные случаи)[104]. Данная корреляция показывает на сколько может быть различными уровни продовольственной безопасности и медицины в государствах.
Проблема контаминации пищевых продуктов по мнению Всемирной организации продовольствия (ФАО) является одной из главнейших проблем человечества.
Безопасность пищевых продуктов
Под безопасностью пищевых продуктов понимается отсутствие опасности для здоровья и жизни человека при употреблении их, как с точки зрения опасности острого патофизиологического воздействия (пищевые интоксикации или токсоинфекции), так и с точки зрения опасности последствий отдалённого, хронического или долговременного воздействия (канцерогенность, мутагенное воздействие, иммунодепрессивный эффект, миелотоксичность итд.).
Пищевые продукты и сырьё являются источниками контаминантов, что влечёт за собой множественные риски для здоровья или жизни потребителя, вследствие этого необходимо проводить комплекс мер по обеспечению безопасности данной категории продуктов, к которым относят деконтаминацию. Деконтаминация как технологический процесс, направлена на удаление или полную инактивацию контаминантов в пищевых продуктах или сырье, осуществляемую при помощи механических, физических, химических и/или комбинированных (смешанных) методов.
Механические методы деконтаминации
Механические методы деконтаминации наиболее простые и доступные, представляют собой использование механических процессов очистки, таких, как фильтрование или баромембранные процессы. Фильтрование позволяет очистить пищевые продукты от твёрдых частиц химических контаминантов. Баромембранные процессы служат для более глубокой очистки продукта, посредством обратного осмоса и ультрафильтрации.
Физические методы деконтаминации
Физические методы деконтаминации — использование теплового и волнового излучения. Тепловые или термические методы основываются на нагревании пищевых продуктов до определённой температуры, как правило кратковременно в специальных устройствах — пастеризаторах, стерилизаторах или автоклавах, при этом, процесс нагрева происходит с увеличением давления. Также к этому методу относят криоконсервацию, в результате которой происходит глубокая заморозка пищевых продуктов (производится жидким азотом).
Волновые методы основываются на применении электромагнитного излучения с высокой энергией, как правило, такие виды излучения имеют короткие длины волн, к ним относятся: УФ-лучи, рентгеновское или гамма-излучение. Большинство биологических агентов (бактерии, простейшие, микроскопические грибы) очень чувствительны к подобному роду воздействиям (УФ-лучи), что делает волновые процессы эффективными. Однако применение в процессе деконтаминации пищевых продуктов рентгеновского или более агрессивного гамма-излучения во многих странах запрещено. Нежелательные изменения, которые происходят в некоторых облученных продуктах, могут быть вызваны непосредственно облучением или косвенно в результате пострадиационных реакций. Вода подвергается радиолизу при облучении следующим образом:
3Н2О → Н• + ОН• + Н2О2 + Н2.
Кроме того, свободные радикалы, образованные на всём протяжении пути первичного электрона, реагируют друг с другом, как в случае диффузии. Некоторые из продуктов, образованные вдоль линии прохождения электрона, могут реагировать со свободными молекулами. Облучение в анаэробных условиях несколько снижает образование неприятных запахов и привкусов из-за нехватки кислорода, участвующего в образовании пероксидов. Один из лучших способов минимизировать образование нежелательных ароматов — облучение при температурах подмораживания. Действие температур подмораживания должно уменьшить или остановить радиолиз и образование сопутствующих ему реагентов. Другие способы снижения побочных эффектов в продуктах представлены в таблице 1.
Кроме воды белки и другие азотсодержащие компоненты — самые чувствительные к действию облучения в продуктах. Продукты облучения аминокислот, пептидов и белков зависят от дозы радиации, температуры, количества кислорода, количества влаги и других факторов.
| Метод | Аргументация |
|---|---|
| Снижение температуры | Связывание свободных радикалов |
| Снижение давления кислорода | Сокращение числа окислительных свободных радикалов, активизирующих молекулы |
| Добавление поглотителей свободных радикалов | Конкуренция поглотителей за свободные радикалы |
| Дистилляция | Удаление летучих предшественников неприятных аромата и вкуса |
| Сокращение дозы | Очевидно[105] |
Химические методы деконтаминации

Химические методы деконтаминации — применение химических соединений, предотвращающих контаминацию пищевых продуктов биологическими агентами (условно-патогенные, патогенные бактерии, микроскопические плесневые грибы, биологически-активные продукты их метаболизма итд.). К таким соединениям относятся широко используемые консерванты, как, например, некоторые органические кислоты (уксусная, пропионовая, бензойная[106], сорбиновая итд.) и/или их соли (бензоат натрия, сорбат калия[107] итд.), а также поваренная соль (хлорид натрия), этиловый спирт, мёд или сахар (в высоких концентрациях 65—80 %). Консерванты создают неблагоприятную среду, подавляя рост, развитие и размножение биологических агентов (обладают бактериостатическим и фунгистатическим действиями)[108].
| Консервант | Бактерии | Дрожжи | Плесневые микромицеты |
|---|---|---|---|
| Нитриты | ++ | - | - |
| Неорганические сульфиты | ++ | ++ | + |
| Муравьиная кислота | + | ++ | ++ |
| Пропионовая кислота | + | ++ | ++ |
| Сорбиновая кислота | ++ | +++ | +++ |
| Бензойная кислота | ++ | +++ | +++ |
| Гидроксибензоаты | ++ | +++ | +++ |
| Дифенил | - | ++ | ++ |
| Примечание: — неэффективен; + малая эффективность; ++ средняя эффективность;
+++ высокая эффективность[109]. |
Использование агрессивных химических соединений, таких, как аммиак, формальдегид, гипохлорит натрия. Формальдегидом обрабатывают зёрна злаковых культур, используют в качестве фунгицида, однако, его наличие даже остаточного количества в зёрнах не допустимо. Гипохлорит натрия NaOCl, ввиду своих сильных окислительных свойств в нейтральной среде (молекула неустойчивая и выделяет сильнейший окислитель и биоцидное соединение — синглетный кислород[110]), также применяют в качестве деконтаминанта зерна, защищая его от опасных микромицетов (рода аспергилл, пеницилл, фузариум и т. д.). При этом гипохлорит натрия отлично инактивирует множественные токсины — ботулинистический, токсины морских животных, микотоксины и др[111].
Комбинированные методы деконтаминации
Комбинированные или смешанные методы деконтаминации представляют собой одновременное применение нескольких методов, например, физических совместно с химическими, тем самым повышая эффективность процесса. Являются наиболее оптимальными, приоритетными и действенными в производстве пищевых продуктов или сырья. В настоящее время использование комбинированных методов деконтаминации, позволяют снизить потенциальные риски, которые могут привести ущерб здоровью человека, в случае контаминации или порчи пищевых продуктов или сырья во много раз, тем самым, обеспечивая безопасность и контроль качества.
Обеспечение качества и безопасности пищевых продуктов
Обеспечение качества и безопасности пищевых продуктов является основной целью сохранения полноценного здоровья человека. Представляет собой комплекс мер, направленных на соответствие пищевых продуктов международным стандартам сертификации, включая этапы производства, транспортировки и хранения. Одним из таких стандартов является система ХАССП, внедрение которой на пищевом производстве позволяет максимально снизить все угрозы и риски, возникающие непосредственно во время процесса производства, повысить качество продукта и сохранить пищевую ценность[112].
Примечания
- Yong Zhang, Cao Chen, Shuangli Zhu, Chang Shu, Dongyan Wang. Isolation of 2019-nCoV from a Stool Specimen of a Laboratory-Confirmed Case of the Coronavirus Disease 2019 (COVID-19) (англ.) // China CDC Weekly. — 2020-02-01. — Vol. 2, iss. 8. — P. 123—124. — ISSN 2096-7071.
- Светлана Евгеньевна Траубенберг, А.А. Кочеткова; Нечаев, Алексей Петрович. Пищевая химия. — 2-е. — Санкт-Петербург: ГИОРД, 2003. — С. 524. — 640 с. — 3000 экз. — ISBN 5-901065-38-0.
- Preface: Food—A necessity and a threat // Microbial Food Contamination / Wilson, C.L.. — CRC Press, 2008. — С. xi–xvi. — ISBN 9781420008470.
- Bohrer, D. Preface // Sources of Contamination in Medicinal Products and Medical Devices (англ.). — John Wiley & Sons, 2012. — ISBN 9781118449059.
- Rose, M. Environmental Contaminants // Encyclopedia of Meat Sciences / Dikeman, M.; Devine, C.. — 2nd. — Elsevier, 2014. — Т. 1. — С. 497—501. — ISBN 9780123847348.
- Midcalf, B. Pharmaceutical Isolators: A Guide to Their Application, Design and Control (англ.). — Pharmaceutical Press, 2004. — P. 88—89. — ISBN 9780853695738.
- Роева Н.Н. Безопасность продовольственных продуктов. — М.: МГУТУ, 2009.
- Type I host resistance and Trichothecene Accumulation in Fusarium-infected Wheat Heads // American Journal of Agricultural and Biological Sciences. — 2011. — 1 февраля (т. 6, № 2). — С. 231—241. — ISSN 1557-4989. — doi:10.3844/ajabssp.2011.231.241.
- Beyer M., Klix M. B., Klink H., Verreet J.-A. Quantifying the effects of previous crop, tillage, cultivar and triazole fungicides on the deoxynivalenol content of wheat grain — a review // Journal of Plant Diseases and Protection. — 2006. — Декабрь (т. 113, № 6). — С. 241—246. — ISSN 1861-3829. — doi:10.1007/BF03356188.
- Ilic Z., Crawford D., Vakharia D., Egner P. A., Sell S. Glutathione-S-transferase A3 knockout mice are sensitive to acute cytotoxic and genotoxic effects of aflatoxin B1. (англ.) // Toxicology and applied pharmacology. — 2010. — Vol. 242, no. 3. — P. 241—246. — doi:10.1016/j.taap.2009.10.008. — PMID 19850059.
- Соланин // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Food Poisoning from Marine Toxins - Chapter 2 - 2018 Yellow Book (англ.) ?. CDC (2017). Дата обращения: 1 июня 2018.
 Эта статья включает текст из этого источника, который находится в общественном достоянии.
Эта статья включает текст из этого источника, который находится в общественном достоянии. - Association of acute toxic encephalopathy with litchi consumption in an outbreak in Muzaffarpur, India, 2014: a case-control study. The Lancet.
- Нельсон Д., Кокс М. Основы биохимии Ленинджера. — М.: БИНОМ, 2011. — Т. II.
- Страйер Л. Биохимия. — М.: Мир, 1985. — Т. 3. — С. З24. — 400 с.
- Huot, R. I.; Armstrong, D. L.; Chanh, T. C. Protection against nerve toxicity by monoclonal antibodies to the sodium channel blocker tetrodotoxin (англ.) // Journal of Clinical Investigation : journal. — 1989. — June (vol. 83, no. 6). — P. 1821–1826. — doi:10.1172/JCI114087. — PMID 2542373.
- M. Cochet-Meillhac; Chambon P. Animal DNA-dependent RNA polymerases. 11. Mechanism of the inhibition of RNA polymerases B by amatoxins (англ.) // Biochim Biophys Acta : journal. — 1974. — Vol. 353, no. 2. — P. 160–184. — doi:10.1016/0005-2787(74)90182-8. — PMID 4601749.
- Staphylococcal Food Poisoning. cdc.gov. hhs.gov (4 октября 2016). Дата обращения: 23 октября 2016.
- «Staphylococcus.» Foodsafety.gov, U.S. Department of Health and Human Services, https://www.foodsafety.gov/poisoning/causes/bacteriaviruses/staphylococcus/.
- Bergdoll, M.S. 1972. The enterotoxins. In The Staphylococci, ed. J.O. Cohen, 301—331. New York: Wiley-Interscience.
- Ryan, Kenneth J.; Ray, C. George. Sherris Medical Microbiology : an Introduction to Infectious Diseases (англ.). — 4th. — New York: McGraw-Hill Education, 2004. — P. 310. — ISBN 978-0-8385-8529-0.
- Kiu, R; Hall, L. J. An update on the human and animal enteric pathogen Clostridium perfringens (англ.) // Emerging Microbes and Infections : journal. — 2018. — Vol. 7, no. 141. — P. 141. — doi:10.1038/s41426-018-0144-8. — PMID 30082713.
- Katahira J., Inoue N., Horiguchi Y., Matsuda M., Sugimoto N. Molecular cloning and functional characterization of the receptor for Clostridium perfringens enterotoxin (англ.) // J. Cell Biol. : journal. — 1997. — Vol. 136, no. 6. — P. 1239—1247. — doi:10.1083/jcb.136.6.1239. — PMID 9087440.
- Janes L.E., Connor L.M., Moradi A., Alghoul M. Current Use of Cosmetic Toxins to Improve Facial Aesthetics. Plast. Reconstr. Surg.. 2021;:644E-657E. doi:10.1097/PRS.0000000000007762
- Rosales RL, Bigalke H, Dressler D. Pharmacology of botuli- num toxin: Differences between type A preparations. Eur J Neurol. 2006;13(Suppl 1):2-10.
- Сальмонеллы / А. А. Имшенецкий // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
- Stanley B. Prusiner — Autobiography. NobelPrize.org. Дата обращения: 18 июня 2013. Архивировано 14 июня 2013 года.
- А. Котик, Труфанов О. В., Труфанова В. А. Словарь токсикологических терминов, Харьков: НТМТ, 2006.— 100 с.
- Hudler, George W. Magical Mushrooms, Mischievous Molds: The Remarkable Story of the Fungus Kingdom and Its Impact on Human Affairs (англ.). — Princeton University Press, 1998. — ISBN 978-0-691-07016-2.
- Грачева И.М. Теоретические основы биотехнологии. Биохимические основы синтеза биологически активных веществ. — М.: Элевар, 2003. — С. 379. — 554 с.
- Geiser D. M., Dorner J. W., Horn B. W., Taylor J. W. The phylogenetics of mycotoxin and sclerotium production in Aspergillus flavus and Aspergillus oryzae (англ.) // Fungal Genetics and Biology : journal. — 2000. — December (vol. 31, no. 3). — P. 169—179. — doi:10.1006/fgbi.2000.1215. — PMID 11273679.
- Neal, G.E.; Eaton, D.L.; Judah, D.J.; Verma, A. Metabolism and Toxicity of Aflatoxins M1and B1in Human-Derivedin VitroSystems (англ.) // Toxicology and Applied Pharmacology : journal. — 1998. — July (vol. 151, no. 1). — P. 152—158. — doi:10.1006/taap.1998.8440.
- Galvano F., Ritieni A., Piva G., Pietri A. Mycotoxins in the human food chain. In: Diaz D.E., editor. The Mycotoxin Blue Book. Nottingham University Press; Nottingham, UK: 2005. pp. 187—224.
- Wogan GN, Hecht SS, Felton JS, Conney AH, Loeb LA. Environmental and chemical carcinogenesis. Seminars in Cancer Biology (2004). 14: 473—486.
- Ricordy R, Gensabella G, Cacci E, Augusti-Tocco G. Impairment of cell cycle progression of aflatoxin B1 in human cell lines. Mutagenesis (2002). 17: 241—249.
- Cole R.J., Cox R.H. The trichothecenes.// In: Cole R.J., Cox R.H. Handbook of Toxic Fungal Metabolites. New York, NY Academic Press, 1981. —P. 152—263.
- Wannemacher R.W. Jr. Bunner D.L., Neufeld H.A. Toxicity of trichothecenes and other related mycotoxins in laboratory animals. // In: Smith J.E., Henderson R.S., eds. Mycotoxins and Aimal Foods. Boca Raton, Fla: CRC Press, 1991. —Р. 499—552.
- Кононенко Г. П., Буркин А. А., Зотова Е. В. и др. Охратоксин А: исследование контаминации зерна // Прикладная биохимия и микробиология. 2000. Т. 36. № 2. С. 209—213.
- Елинов Н.П. Химическая микробиология. — М.: Высшая школа, 1989. — С. 360—361. — 448 с. — 19 000 экз. — ISBN 5-06-000089-3.
- Merck Index, 11th Edition, 7002
- Keblys M., Bernhoft A., Höfer C.C., Morrison E., Jørgen H., Larsen S., Flåøyen A. (2004). The effects of the Penicillium mycotoxins citrinin, cyclopiazonic acid, ochratoxin A, patulin, penicillic acid, and roquefortine C on in vitro proliferation of porcine lymphocytes. Mycopathologia (158) 317—324.
- Бартон Д., Оллис У. Д. Общая органическая химия. — М.: Химия, 1986. — С. 317. — 704 с.
- K. Baumann K. Muenter H. Faulstich. Identification of structural features involved in binding of α-amanitin to a monoclonal antibody (англ.) // Biochemistry : journal. — 1993. — Vol. 32, no. 15. — P. 4043—4050. — doi:10.1021/bi00066a027. — PMID 8471612.
- Benjamin, p.200.
- Death Cap Mushroom Soup Claims Fourth Victim
- Benjamin, p.211
- Hall IR. Edible and Poisonous Mushrooms of the World. — Portland, Oregon : Timber Press, 2003. — P. 107. — ISBN 0-88192-586-1.
- Бартон Д., Оллис У.Д. Общая органическая химия. — М.: Химия, 1986. — С. 317. — 704 с.
- М. В. Вишневский //Ядовитые грибы России. «Проспект», 2016 // УДК 630.283 // ББК 28.591я2
- Kretz O., Creppy E.E., Dirheimer G. Characterization of bolesatine, a toxic protein from the mushroom Boletus satanas Lenz and its effects on kidney cells (англ.) // Toxicology : journal. — 1991. — Vol. 66, no. 2. — P. 213—224. — doi:10.1016/0300-483X(91)90220-U. — PMID 1707561.
- Ennamany R., Bingen A., Creppy E.E., Kretz O., Gut J.P., Dubuisson L., Balabaud C., Sage P.B., Kirn A. Aspirin (R) and heparin prevent hepatic blood stasis and thrombosis induced by the toxic glycoprotein Bolesatine in mice (англ.) // Human & Experimental Toxicology : journal. — 1998. — Vol. 17, no. 11. — P. 620—624. — doi:10.1191/096032798678908017.
- North, Pamela. Poisonous Plants and Fungi in colour. — Blandford Press & Pharmacological Society of Great Britain, 1967.
- Brensinsky A, Besl H. (1990). A colour atlas of poisonous fungi. Wolfe Publishing Ltd, London. 295 p.
- Spoerke DG, Rumack BH (eds). (1994). Handbook of mushroom poisoning: diagnosis and treatment. CRC Press, Boca Raton.
- Berger KJ, Guss DA. (2005). Mycotoxins revisited: Part I. J Emerg Med 28:53.
- Описание строчка обыкновенного в интернет-журнале «Декоративный сад». Дата обращения: 22 декабря 2015.
- М.В.Вишневский. Строчки съедобные и ядовитые. Дата обращения: 22 декабря 2015.
- Andary C., Privat G. Variations of monomethylhydrazine content in Gyromitra esculenta (англ.) // Mycologia : journal. — Taylor & Francis, 1985. — Vol. 77, no. 2. — P. 259—264. — doi:10.2307/3793077. — .
- Алтухов Н.М., Афанасьев В.И., Башкиров Б.А. Краткий справочник ветеринарного врача. — М.: Агропромиздат, 1990. — 574 с. — 200 000 экз. — ISBN 5-10-001366-4.
- Manfred Hesse. Alkaloids. Nature’s Curse or Blessing. — Wiley-VCH, 2002. — p. 4.
- Тарханов И. Р.,. Яды сердечные // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Sharma, R. K., Consice textbook of forensic medicine & toxicology, Elsevier, 2008
- http://toxnet.nlm.nih.gov/cgi-bin/sis/search/a?dbs+hsdb:@term+@DOCNO+3559 «For 100 grams of moistened seed; the peach pit contains approximately 88 mg of hydrocyanic acid, cultivated apricot pit 8.9 mg, wild apricot pit 217 mg. The ingestion of 500 mg of amygdalin may release as much as 30 mg of cyanide.»
- Chan, Charles KF; Ransom, Ryan C; Longaker, Michael T. Lectins bring benefits to bones (англ.) // eLife : journal. — 2016. — 13 December (vol. 5). — doi:10.7554/eLife.22926. — PMID 27960074.
- Dasuri K., Ebenezer P. J., Uranga R. M., Gavilán E., Zhang L., Fernandez-Kim S. O. K., Bruce-Keller A. J., Keller J. N. Amino acid analog toxicity in primary rat neuronal and astrocyte cultures: implications for protein misfolding and TDP-43 regulation // Journal of Neuroscience Research. — 2011. — Vol. 89, № 9. — P. 1471—1477. — doi:10.1002/jnr.22677. — PMID 21608013.
- Montanaro, A; Bardana Jr, E. J. (1991). “Dietary amino acid-induced systemic lupus erythematosus”. Rheumatic Diseases Clinics of North America. 17 (2): 323—32. DOI:10.1016/S0889-857X(21)00573-1. PMID 1862241.
- Bygbjerg, I.C.; Johansen, H.K. (1991). “Manchineel poisoning complicated by streptococcal pharyngitis and impetigo”. Ugeskr. Laeger. 154 (1): 27—28. PMID 1781062.
- Suehiro, M (1994). “[Historical review on chemical and medical studies of globefish toxin before World War II]”. Yakushigaku Zasshi. 29 (3): 428—34. PMID 11613509.
- Леонид Завальский. Нейротоксины: яды или противоядия?. ОАО «Известия». Дата обращения: 27 января 2009.
- Rigoulet J., Hennache A., Lagourette P., George C., Longeart L., Le Net J. L., Dubey J. P. Toxoplasmosis in a bar-shouldered dove (Geopelia humeralis) from the Zoo of Clères, France (англ.) // Parasite : journal. — 2014. — Vol. 21. — P. 62. — doi:10.1051/parasite/2014062. — PMID 25407506.

- Fayer, R., and J.P. Dubey. 1985. Methods for controlling transmission of protozoan parasites from meat to man. Food Technol. 39(3):57-60.
- Polynuclear Aromatic Hydrocarbons. In: Guidelines for Drinking-water Quality, 2nd ed. Vol. 2. Health Criteria and other Supporting Information. Geneva, World Health Organization, pp. 123—152.: (page 11) «For ambient air, residential heating and vehicle traffic appear to be the main sources of exposure. In the direct vicinity of an emission source, a maximum intake of 1 µg of BaP per day may be reached (WHO, 1987; LAI, 1992).»
- Polynuclear Aromatic Hydrocarbons. In: Guidelines for Drinking-water Quality, 2nd ed. Vol. 2. Health Criteria and other Supporting Information: «The main contributors of PAHs to the total dietary intake appear to be cereals, oils, and fats. The oil and fat group has high individual PAH levels, whereas the cereal group, although never containing high individual PAH concentrations, is a main contributor by weight to total intake in the diet. Smoked meat and fish products, although containing the highest PAH levels, appear to be low to modest contributors, as they are minor components of the usual diet»
- Hazard Information Bulletin — Dimethylmercury. OSHA Safety and Health Information Bulletins (SHIBs), 1997—1998
- Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей. Изд. 7-е, пер. и доп. В трех томах. Том I. Органические вещества. Под ред. засл. деят. науки проф. Н. В. Лазарева и докт. мед. наук Э. Н. Левиной. Л., «Химия», 1976. 592 стр., 27 табл., библиография —1850 названий.
- Kasper, Dennis L.et al. (2004) Harrison’s Principles of Internal Medicine, 16th ed., McGraw-Hill Professional, p. 618, ISBN 0071402357.
- Smith, Martyn T. Advances in understanding benzene health effects and susceptibility (англ.) // Ann Rev Pub Health : journal. — 2010. — Vol. 31. — P. 133–48. — doi:10.1146/annurev.publhealth.012809.103646.
- Vale A. Methanol (неопр.) // Medicine. — 2007. — Т. 35, № 12. — С. 633–4. — doi:10.1016/j.mpmed.2007.09.014.
- http://www.epa.gov/chemfact/s_methan.txt «Humans — Ingestion of 80 to 150 mL of methanol is usually fatal to humans (HSDB 1994).»
- Светлана Евгеньевна Траубенберг, А.А. Кочеткова; Нечаев, Алексей Петрович. Пищевая химия. — Санкт-Петербург: ГИОРД, 2003. — С. 516. — 630 с. — 3000 экз. — ISBN 5-901065-38-0.
- International Agency for Research on Cancer. Polychlorinated dibenzo-para-dioxins and polychlorinated dibenzofurans. — Lyon : IARC, 1997. — Vol. 69. — ISBN 92-832-1269-X.
- The mercury levels in the table, unless otherwise indicated, are taken from: Mercury Levels in Commercial Fish and Shellfish (1990—2010) Архивировано 3 мая 2015 года. U.S. Food and Drug Administration. Accessed 8 January 2012.
- Первый искусственный подсластитель был на основе свинца и убивал древних римлян. Фактрум. Дата обращения: 31 октября 2015.
- Cecil, KM; Brubaker, CJ; Adler, CM; Dietrich, KN; Altaye, M; Egelhoff, JC; Wessel, S; Elangovan, I; Hornung, R. Decreased Brain Volume in Adults with Childhood Lead Exposure (англ.) // PLOS Medicine : journal / Balmes, John. — 2008. — Vol. 5, no. 5. — P. e112. — doi:10.1371/journal.pmed.0050112. — PMID 18507499.
- Lead found in turmeric (англ.), Stanford News (24 September 2019). Дата обращения 25 сентября 2019.
- Список 12 изначальных соединений
- International Notes Acute Convulsions Associated with Endrin Poisoning -- Pakistan. Morbidity and Mortality Weekly Report (MMWR). Center for Disease Control (14 December 1984). Дата обращения: 1 марта 2015.
- 1990 год — загрязнение питьевой воды г. Уфы фенолом Архивировано 15 января 2005 года.
- Aygün SF, Kabadayi F. Determination of benzo[a]pyrene in charcoal grilled meat samples by HPLC with fluorescence detection. International Journal of Food Sciences and Nutrition. 2005 Dec;56(8):581-5. PMID 16638662
- Polynuclear Aromatic Hydrocarbons. In: Guidelines for Drinking-water Quality, 2nd ed. Vol. 2. Health Criteria and other Supporting Information: There are a few studies on daily intake of individual PAHs from food from western Europe… The maximum/median intake levels for the PAHs selected in this guideline, in µg/day per person, have been estimated to be as follows: … BaP (0.36/0.05);. (Pfannhauser, 1991).
- Bernstein, JA; Cremonesi, P; Hoffmann, TK; Hollingsworth, J. Angioedema in the emergency department: a practical guide to differential diagnosis and management (англ.) // International Journal of Emergency Medicine : journal. — 2017. — December (vol. 10, no. 1). — P. 15. — doi:10.1186/s12245-017-0141-z. — PMID 28405953.
- Agrios, George N. Plant Pathology: Fifth Edition. — Elsevier Academic Press, 2005. — P. 922. — ISBN 0-12-044565-4.
- Светлана Евгеньевна Траубенберг, А.А. Кочеткова; Нечаев, Алексей Петрович. Пищевая химия. — 2. — Санкт-Петербург: ГИОРД, 2003. — С. 526. — 640 с. — 3000 экз. — ISBN 5-901065-38-0.
- Oxford, 2014, p. 214.
- Paul M Dewick. Medicinal Natural Products. A Biosynthetic Approach. Second Edition. — Wiley, 2002. — С. 370—372. — 515 с. — ISBN 0471496405.
- Орехов А. П. Химия алкалоидов. — Изд.2. — М.: АН СССР, 1955. — С. 627. — 859 с.
- Davidson, Alan. The Oxford Companion to Food. — Oxford University Press, 2006. — P. 324. — ISBN 978-0-19-280681-9.
- Cristina J., Costa-Mattioli M. Genetic variability and molecular evolution of hepatitis A virus (англ.) // Virus Res. : journal. — 2007. — August (vol. 127, no. 2). — P. 151—157. — doi:10.1016/j.virusres.2007.01.005. — PMID 17328982.
- Коротяев А. И., Бабичев С. А. Медицинская микробиология, иммунология и вирусология. — СПб.: СпецЛит, 2010. — С. 1062—1064. — 1992 с. — ISBN 978-5-299-00425-0.
- Advances in Agronomy. — Academic Press, 2013. — С. 159—. — ISBN 978-0-12-407798-0.
- Immunodeficiency disorders: MedlinePlus Medical Encyclopedia (англ.). medlineplus.gov. Дата обращения: 6 мая 2017.
- NCI Dictionary of Cancer Terms (англ.). National Cancer Institute. Дата обращения: 6 мая 2017.
- Cunha-Oliveira T., Rego A. C., Oliveira C. R. Cellular and molecular mechanisms involved in the neurotoxicity of opioid and psychostimulant drugs (англ.) // Brain Research Reviews : journal. — 2008. — June (vol. 58, no. 1). — P. 192—208. — doi:10.1016/j.brainresrev.2008.03.002. — PMID 18440072.. — «The Interagency Committee on Neurotoxicology defined neurotoxicity as a broad concept, including any adverse effect on the structure or function of the central and/or peripheral nervous system by a biological, chemical or physical agent. In this definition, neurotoxic effects may be permanent or reversible and result from direct or indirect actions on the nervous system (Erinoff, 1995).».
- География раковых заболеваний — Популярные статьи — Онкология — Энциклопедия — MedPortal.ru
- Goldblith, S. A. 1963. Radiation preservation of foods — Two decades of research and development. In Ra-diationResearch,155-167.Washington,DC:U.S.DepartmentofCommerce,OfficeofTechnicalServices.
- A D Warth. Mechanism of action of benzoic acid on Zygosaccharomyces bailii: effects on glycolytic metabolite levels, energy production, and intracellular pH (англ.) // Appl Environ Microbiol : journal. — 1991. — 1 December (vol. 57, no. 12). — P. 3410—3414. — PMID 1785916.
- Nordic Food Additive Database Архивная копия от 2 мая 2008 на Wayback Machine Nordic Working Group on Food Toxicology and Risk Assessment.
- Светлана Евгеньевна Траубенберг, А.А. Кочеткова; Нечаев, Алексей Петрович. Пищевая химия. — 2-е. — Санкт-Петербург: ГИОРД, 2003. — С. 440—441. — 640 с. — 3000 экз. — ISBN 5-901065-38-0.
- Светлана Евгеньевна Траубенберг, А.А. Кочеткова; Нечаев, Алексей Петрович. Пищевая химия. — 2-е. — Санкт-Петербург: ГИОРД, 2003. — С. 442. — 640 с. — 3000 экз. — ISBN 5-901065-38-0.
- Швецов А. Б., Козырева А. В., Седунов С. Г., Тараскин К. А. Хлорные дезинфектанты и их применение в современной водоподготовке // Молекулярные технологии. — 2009. — № 3. — С. 98—121.
- Biological Safety: Principles and Practices / Edited by Fleming D. O., Hunt D. L.. — Third edition. — Washington: ASM Press, 200o. — P. 269. — ISBN 1-55581-180-9.
- Система управления безопасностью пищевых продуктов — In.Business World
Литература
- The Oxford Companion to Food / Alan Davidson, Tom Jaine. — Oxford University Press, 2014. — ISBN 978-0-19-104072-6.