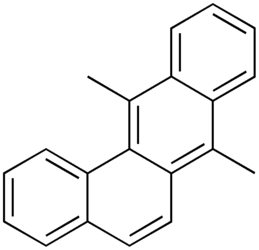
Диметилбензантрацен
ДМБА, сокр. от диметилбензантрацéн — органическое соединение, полициклический ароматический углеводород, производное бензантрацена, один из распространённых и сильнейших канцерогенов[1]. Образуется в результате неполного сгорания нефтепродуктов, бытового мусора, входит в состав выхлопных газов, смога и сигаретного дыма. Синтезируется из каменноугольной смолы.
| Диметилбензантрацен | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
7,12-диметил-5,6-бензо[а]зантрацен |
| Сокращения | ДМБА |
| Традиционные названия | диметилбензантрацен, 5,10-диметил-1,2-бензо[а]зантрацен |
| Хим. формула | С20H16 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 256,34104 (±0,004) г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 123 °C |
| • кипения | 480 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,055 г/100 мл |
| Классификация | |
| Рег. номер CAS | 57-97-6 |
| PubChem | 6001 |
| Рег. номер EINECS | 200-359-5 |
| SMILES | |
| InChI | |
| ChEBI | 254496 |
| ChemSpider | 5779 |
| Безопасность | |
| Предельная концентрация | 0,005 мг/м3 |
| ЛД50 |
0,115 мг/кг (мыши, перорально), 0,250 мг/кг (мыши, накожно) |
| Токсичность | чрезвычайно токсичен для многих млекопитающих, сильный кожный ирритант, сильнейший канцероген |
| Пиктограммы ECB |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
История
Впервые был синтезирован в 1938 году В. Бахманом и Й. Хемердом, в том же году Бахманом и его коллегами из Мичиганского университета был обнаружен канцерогенный потенциал[2]. Опыты проводились на мышах, в результате чего они обнаружили, что ДМБА индуцирует опухоли в 2 раза быстрее, чем 3-метилхолантрен[2]. Благодаря положению метильной группы (положение С7,С12), ДМБА считается высококанцерогенным веществом[3][4].
Физические свойства
Представляет собой твёрдое вещество, от желтовато-серого до жёлтого цвета, практически нерастворимое в воде (0,055 мг/1 л, при t = 24° С)[5], хорошо в органических растворителях: бензоле[6], толуоле, ацетоне[6] и ксилолах, слабо в спирте и эфире имеет высокую температуру плавления (122,5° С)[6] и кипения. Горит сильно коптящим пламенем, часто не полностью сгорая образует угарный газ.
Токсикология и биологическая роль
Чрезвычайно токсичен, при попадании даже в незначительных количествах (15 мкг) на кожу (особенно повреждённую), может вызывать предраковые состояния. Является генотоксическим канцерогеном. В организм попадает через лёгкие, кровь или кожу. Гидроксилируется в печени микросомальной системой окисления. Часто накапливаясь в ней образует более токсичные и канцерогенные промежуточные эпоксиды, которые легко алкилируют ДНК — образуя с ней ковалентно (зачастую прочно) связанные ДНК-аддукты, тем самым вызывая мутации. Помимо канцерогенной активности характеризуется сильной токсичностью — вызывает сильнейшую дегенерацию и некроз близлежащих тканей печени. В небольших количествах может задерживаться в лёгких.
Помимо сильного гепатоканцерогенного действия, ДМБА вызывает часто и быстро опухоли молочной железы и лёгких, меланому и лейкемию, поэтому его широко используют во многих исследовательских лабораториях по изучению рака. ДМБА выступает в качестве инициатора опухолей (в количестве 10-50 мкг), создающий необходимые для исследования геномные мутации[7]. У мышей, подвергавшихся действию ДМБА, наблюдалось значительное повышение частоты мертворождений, уродств, потомство хилое и нежизнеспособное. Может вызывать бесплодие.
Экология
Сильно загрязняет атмосферу, имеет свойства биоаккумуляции. Будучи химически сравнительно устойчивым, ДМБА может долго циркулировать в экосистемах, в результате многие объекты окружающей среды становятся его вторичными источниками. Вместе с бензантраценом и другими ПАУ образуют смог[8]. В больших количествах обнаруживается в воздухе рядом с промышленными зонами и ТЭС, мусоросжигательными заводами. Среднее содержание составляет 150—200 нг/м3.
Из-за своей токсичности и канцерогенности (токсичнее бензола приблизительно в 20 раз), ДМБА не имеет промышленного значения. ПДК в рабочей зоне = 0,00015 мг/м3[8], для атмосферного воздуха 0,005-0,01 мкг/м3[8]. Сильно раздражает кожу, является ирритантом. LD50 для мыши (перорально) составляет 0,115 мг/кг, 0,2-0,25 мг/кг — подкожно[9].
Примечания
- M. M. Coombs und T. S. Bhatt: Cyclopenta(a)phenanthrenes. CUP Archive, 1987, S. 8. ISBN 0-521-30123-8.
- W. E. Bachmann und J. M. Chemerda: The synthesis of 9,10-dimethyl-1:2-benzanthracene, 9,10-diethyl-1:2-benzanthracene and 5,9,10-trimethyl-1:2-benzanthracene. In: JACS. 60, 1938, S. 1023.
- W. E. Bachmann u. a.: The rapid production of tumours by two new hydrocarbons. In: Yale J Biol Med. 11, 1938, S. 97-102, PMC 2601969
- W. E. Bachmann u. a.: The rapid production of tumors by two new hydrocarbons. In: Yale J Biol Med. 73, 1939, S. 259—263, PMID 11765945
- S. H. Yalkowsky und R. M. Dannenfelser: The AQUASOL dATAbASE of Aqueous Solubility. 5. Auflage, College of Pharmacy, 1992.
- CRC Handbook of Chemistry and Physics. 90. Auflage, CRC Press Inc., 2009, S. 3-192.
- История изучения канцерогенеза. Двухстадийный канцерогенез кожи
- Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей. Изд. 7-е, пер. и доп. В трех томах. Том I. Органические вещества. Под ред. засл. деят. науки проф. Н. В. Лазарева и докт. мед. наук Э. Н. Левиной. Л., «Химия», 1976, 592 стр., 27 табл.
- Канцерогенные вещества — справочник: материалы Международного агентства по изучению рака. — М. : Медицина, 1987. — 334 с. — 2.30 р.
Ссылки
- ДМБА вызывает рак кожи
- Молекулярная онкология (недоступная ссылка)