Оксид титана(IV)
Оксид титана(IV) (диоксид титана, двуокись титана, титановые белила, пищевой краситель E171) TiO2 — амфотерный оксид четырёхвалентного титана. Является основным продуктом титановой индустрии (на производство чистого титана идёт лишь около 5 % титановой руды)[2].
| Оксид титана(IV) | |
|---|---|
_oxide.jpg.webp) | |
| Общие | |
| Систематическое наименование |
Диоксид титана |
| Хим. формула | TiO2 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 79,866 г/моль |
| Плотность |
(Р) 4,235 г/см³ (А) 4,05 г/см³ (Б) 4,1 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1843 °C |
| • кипения | 2972 °C |
| • разложения | 2900 °C |
| Давление пара | 0 ± 1 мм рт.ст.[1] |
| Классификация | |
| Рег. номер CAS | 13463-67-7 |
| PubChem | 26042 |
| Рег. номер EINECS | 236-675-5 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E171 |
| RTECS | XR2775000 |
| ChEBI | 32234 |
| ChemSpider | 24256 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Строение
Оксид титана существует в виде нескольких модификаций. В природе встречаются кристаллы с тетрагональной сингонией (анатаз, рутил) и ромбической сингонией (брукит). Искусственно получены ещё две модификации высокого давления — ромбическая IV и гексагональная V.
| Модификация/Параметр | Рутил | Анатаз | Брукит | Ромбическая IV | Гексагональная V | |
|---|---|---|---|---|---|---|
| Параметры элементарной решётки, нм | a | 0,45929 | 0,3785 | 0,51447 | 0,4531 | 0,922 |
| b | — | — | 0,9184 | 0,5498 | — | |
| c | 0,29591 | 0,9486 | 0,5145 | 0,4900 | 0,5685 | |
| Число формульных единиц в ячейке | 2 | 4 | 8 | |||
| Пространственная группа | P4/mnm | I4/amd | Pbca | Pbcn | ||
При нагревании и анатаз, и брукит необратимо превращаются в рутил (температуры перехода соответственно 400—1000 °C и около 750 °C). Основой структур этих модификаций являются октаэдры TiO6, то есть каждый ион Ti4+ окружён шестью ионами O2−, а каждый ион O2− окружён тремя ионами Ti4+.
Октаэдры расположены таким образом, что каждый ион кислорода принадлежит трём октаэдрам. В анатазе на один октаэдр приходятся 4 общих ребра, в рутиле — 2.
Нахождение в природе
В чистом виде в природе встречается в виде минералов рутила, анатаза и брукита (по строению первые два имеют тетрагональную, а последний — ромбическую сингонию), причём основную часть составляет рутил.
Третье в мире по запасам рутила месторождение находится в Рассказовском районе Тамбовской области. Крупные месторождения находятся также в Чили (Cerro Bianco), канадской провинции Квебек, Сьерра-Леоне.
Свойства
Физические, термодинамические свойства

Чистый диоксид титана — бесцветные кристаллы (желтеют при нагревании). Для технических целей применяется в раздробленном состоянии, представляя собой белый порошок. Не растворяется в воде и разбавленных минеральных кислотах (за исключением плавиковой).
- Температура плавления для рутила — 1870 °C (по другим данным — 1850 °C, 1855 °C)
- Температура кипения для рутила — 2500 °C.
- Плотность при 20 °C:
- Температура разложения для рутила 2900 °C[4]
Температура плавления, кипения и разложения для других модификаций не указана, так как они переходят в рутильную форму при нагревании (см. выше).
| Модификация | Интервал температуры, K | |||||
|---|---|---|---|---|---|---|
| 298—500 | 298—600 | 298—700 | 298—800 | 298—900 | 298—1000 | |
| рутил | 60,71 | 62,39 | 63,76 | 64,92 | 65,95 | 66,89 |
| анатаз | 63,21 | 65,18 | 66,59 | 67,64 | 68,47 | 69,12 |
| Модификация | ΔH°f, 298, кДж/моль[7] | S°298, Дж/моль/K[8] | ΔG°f, 298, кДж/моль[9] | C°p, 298, Дж/моль/K[10] | ΔHпл., кДж/моль[11] |
|---|---|---|---|---|---|
| рутил | -944,75 (-943,9[4]) | 50,33 | -889,49 (-888,6[4]) | 55,04 (55,02[4]) | 67 |
| анатаз | -933,03 (938,6[4]) | 49,92 | -877,65 (-888,3[4]) | 55,21 (55,48[4]) | 58 |
Вследствие более плотной упаковки ионов в кристалле рутила увеличивается их взаимное притяжение, снижается фотохимическая активность, увеличиваются твёрдость (абразивность), показатель преломления (2,55 — у анатаза и 2,7 — у рутила), диэлектрическая постоянная.
Химические свойства
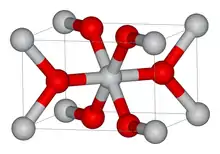
Серым цветом обозначены атомы титана, красным — кислорода
Диоксид титана амфотерен, то есть проявляет как осно́вные, так и кислотные свойства (хотя реагирует главным образом с концентрированными кислотами).
Медленно растворяется в концентрированной серной кислоте, образуя соответствующие соли четырёхвалентного титана:
При сплавлении с оксидами, гидроксидами, карбонатами образуются титанаты — соли титановой кислоты (амфотерного гидроксида титана TiO(OH)2)
C пероксидом водорода даёт ортотитановую кислоту:
При нагревании с аммиаком даёт нитрид титана:
При нагревании восстанавливается углеродом и активными металлами (Mg, Ca, Na) до низших оксидов.
При нагревании с хлором в присутствии восстановителей (углерода) образует тетрахлорид титана.
Нагревание до 2200 °C приводит сначала к отщеплению кислорода с образованием синего Ti3O5 (то есть TiO2Ti2O3), а затем и тёмно-фиолетового Ti2O3.
Гидратированный диоксид TiO2nH2O [гидроксид титана(IV), оксо-гидрат титана, оксогидроксид титана] в зависимости от условий получения может содержать переменные количества связанных с Ti групп ОН, структурную воду, кислотные остатки и адсорбированные катионы. Полученный на холоде свежеосаждённый TiO2nH2O хорошо растворяется в разбавленных минеральных и сильных органических кислотах, но почти не растворяется в растворах щелочей. Легко пептизируется с образованием устойчивых коллоидных растворов.
При высушивании на воздухе образует объёмистый белый порошок плотностью 2,6 г/см³, приближающийся по составу к формуле TiO22H2O (ортотитановая кислота). При нагревании и длительной сушке в вакууме постепенно обезвоживается, приближаясь по составу к формуле TiO2H2O (метатитановая кислота). Осадки такого состава получаются при осаждении из горячих растворов, при взаимодействии металлического титана с HNO3 и т. п. Их плотность ~ 3,2 г/см³ и выше. Они практически не растворяются в разбавленных кислотах, не способны пептизироваться.
При старении осадки TiO2nH2O постепенно превращается в безводный диоксид, удерживающий в связанном состоянии адсорбированные катионы и анионы. Старение ускоряется кипячением суспензии с водой. Структура образующегося при старении TiO2 определяется условиями осаждения. При осаждении аммиаком из солянокислых растворов при рН < 2 получаются образцы со структурой рутила, при рН 2—5 — со структурой анатаза, из щелочной среды — рентгеноаморфные. Из сульфатных растворов продукты со структурой рутила не образуются.
Кроме того, под воздействием ультрафиолетовых лучей способен разлагать воду и органические соединения.
Токсические свойства, физиологическое действие, опасные свойства
Регистрационный номер ООН — UN2546
При вдыхании
TLV (предельная допустимая концентрация): как TWA (средневзвешенная во времени концентрация, США) — 10 мг/м³ A4 (ACGIH 2001).
ПДК в воздухе рабочей зоны — 10 мг/м³ (1998)
IARC (МАИР) относит оксид титана к группе 2B (потенциально канцерогенный) в случае вдыхания наночастиц[12].
В качестве пищевой добавки E171
Оценки безопасности пищевой добавки E171 (Оксид титана) со стороны EFSA (European Food Safety Authority): был разрешён к пищевому применению до 2022 года директивой 94/36/EEC (в отдельных формах)[13], ADI не установлен, MoS 2250 мг/кг[14].
В конце 2010-х появилось несколько публикаций INRA об исследовании оксида титана на мышах или на малом числе пациентов. Агентство EFSA направило авторам статей ряд вопросов[15] и не нашло причин для переоценки рисков на основании данных публикаций, остаётся в силе мнение 2016 года[16][17].
В США по данным FDA допускается использование красителя — пищевой добавки E171 (Оксид титана) в пищевых продуктах (на уровне не более 1 % по массе), в косметике, в составе лекарственных препаратов[18], что подтверждается CFR Title 21 (Food and Drugs) Chapter I Subchapter A Part 73 (LISTING OF COLOR ADDITIVES EXEMPT FROM CERTIFICATION) — § 73.575 Titanium dioxide.[19]
C 2020 года запрещена во Франции[20]. В 2021 году Европейское агентство по безопасности продуктов питания постановило, что в связи с новыми данными о наночастицах диоксид титана «более не может рассматриваться в качестве безопасной пищевой добавки», его генотоксичность, которая может вести к канцерогенным эффектам, не может сбрасываться со счетов, а «безопасный уровень дневного потребления этой пищевой добавки невозможно установить». Европейский комиссар по здравоохранению анонсировал планы по запрету его использования на территории Европейского Союза[21]
По данным Роспотребнадзора пищевая добавка E171 разрешена для применения на территории России[22]
Добыча и производство
Мировое производство диоксида титана на конец 2004 года достигло приблизительно 5 миллионов тонн[23].
Основные производители и экспортёры диоксида титана:
- Sachtleben Chemie (Пори, Финляндия, Дуйсбург и Крефельд, Германия)
- «Крымский Титан» (Армянск, север Крыма)
- «Сумыхимпром» (Сумы, Украина)
- KRONOS Titan (Норденхам, Германия)
- Tronox (Оклахома-Сити, США)
- DuPont (Де-Лайл, штат Миссисипи, Нью-Джонсонвилл, штат Теннесси, Эджмур, штат Делавэр, США; Альтамира, Мексика; Гуаньинь, Тайвань; Убераба, Бразилия)
В последние годы чрезвычайно быстро растёт производство диоксида титана в Китае.
Сумской государственный институт минеральных удобрений и пигментов (МИНДИП) в своих научно-исследовательских работах особое место уделяет технологиям получения оксида титана (IV) сульфатным способом: исследование, разработка новых марок, модернизация технологии и аппаратурного оформления процесса.
Существуют два основных промышленных метода получения TiO2: из ильменитового (FeTiO3) концентрата и из тетрахлорида титана. Поскольку запасов ильменита для удовлетворения нужд промышленности явно недостаточно, значительная часть TiO2 производится именно из тетрахлорида титана.
Производство диоксида титана из ильменитового концентрата
Первый завод по производству титановых белил из природного титанового минерала ильменита FeTiO3 был построен в Норвегии в 1918 г., однако первые промышленные партии белил имели жёлтый цвет из-за примесей соединений железа и плохо подходили для живописи, так что фактически белые титановые белила стали использоваться художниками лишь в 1922—1925 гг. При этом следует указать, что до 1925 г. были доступны лишь композитные титановые пигменты на базе барита или кальцита.
До 1940-х гг. двуокись титана выпускалась в кристаллической модификации — анатаз (β-TiO2) тетрагональной сингонии с показателем преломления ~2,5
Технология производства состоит из трёх этапов:
- получение растворов сульфата титана (путём обработки ильменитовых концентратов серной кислотой). В результате получают смесь сульфата титана и сульфатов железа (II) и (III), последний восстанавливают металлическим железом до степени окисления железа +2. После восстановления на барабанных вакуум-фильтрах отделяют растворов сульфатов от шлама. Сульфат железа(II) отделяют в вакуум-кристаллизаторе.
- гидролиз раствора сульфатных солей титана. Гидролиз проводят методом введения зародышей (их готовят, осаждая Ti(OH)4 из растворов сульфата титана гидроксидом натрия). На этапе гидролиза образующиеся частицы гидролизата (гидратов диоксида титана) обладают высокой адсорбционной способностью, особенно по отношению к солям Fe3+, именно по этой причине на предыдущей стадии трёхвалентное железо восстанавливается до двухвалентного. Варьируя условия проведения гидролиза (концентрацию, длительность стадий, количество зародышей, кислотность и т. п.), можно добиться выхода частиц гидролизата с заданными свойствами, в зависимости от предполагаемого применения.
- термообработка гидратов диоксида титана. На этом этапе, варьируя температуру сушки и используя добавки (такие, как оксид цинка, хлорид титана) и используя другие методы, можно провести рутилизацию (то есть перестройку оксида титана в рутильную модификацию). Для термообработки используют вращающиеся барабанные печи длиной 40—60 м. При термообработке испаряется вода (гидроксид титана и гидраты оксида титана переходят в форму диоксида титана), а также диоксид серы.
Производство диоксида титана из тетрахлорида титана
В 1938—1939 гг. способ производства изменился — появился так называемый хлорный метод производства белил из тетрахлорида титана, благодаря чему титановые белила стали выпускаться в кристаллической модификации рутил (α-TiO2) — также тетрагональной сингонии, но с другими параметрами решётки и несколько бо́льшим по сравнению с анатазом показателем преломления 2,61.
Существуют три основных метода получения диоксида титана из его тетрахлорида:
- гидролиз водных растворов тетрахлорида титана (с последующей термообработкой осадка)
- парофазный гидролиз тетрахлорида титана (основан на взаимодействии паров тетрахлорида титана с парами воды) при 400°C.
- термообработка тетрахлорида (сжигание в токе кислорода). Процесс обычно ведётся при температуре 900—1000°C
Применение
Основные применения диоксида титана:
- производство лакокрасочных материалов, в частности, титановых белил — 57 % от всего потребления[23] (диоксид титана рутильной модификации обладает более высокими пигментными свойствами — светостойкостью, разбеливающей способностью и др.);
- производство пластмасс — 21 %[23];
- производство ламинированной бумаги — 14 %[23];
- производство декоративной косметики;
- производство огнеупорной бумаги[24];
- фотокаталитические бетоны.
| 2001 г. | 2002 г. | 2003 г. | 2004 г. | |
|---|---|---|---|---|
| Америка | 1730 | 1730 | 1730 | 1680 |
| Запад. Европа | 1440 | 1470 | 1480 | 1480 |
| Япония | 340 | 340 | 320 | 320 |
| Австралия | 180 | 200 | 200 | 200 |
| Прочие страны | 690 | 740 | 1200 | 1400 |
| Всего | 4380 | 4480 | 4930 | 5080 |
Другие применения — в производстве резиновых изделий, стекольном производстве (термостойкое и оптическое стекло), как огнеупор (обмазка сварочных электродов и покрытий литейных форм), в косметических средствах (мыло и т. д.), в фармакологической промышленности в качестве пигмента и наполнителя некоторых лекарственных форм (таблетки и т.д.), в пищевой промышленности (пищевая добавка E171)[26].
Используется в процессах очистки воздуха методом фотокатализа.
Ведутся исследования по использованию диоксида титана в фотохимических батареях — ячейках Гретцеля, в которых диоксид титана, являющийся полупроводником с широкой запрещённой зоной 3-3,2 эВ (в зависимости от кристаллической фазы) и развитой поверхностью, сенсибилизируется органическими красителями[27].
Запрет ЕС
7 февраля 2022 года в ЕС вступил запрет на использовании диоксида титана (E171) в пищевой промышленности. Переходный период продлится 6 месяцев. Применение диоксида титана в фармацевтической промышленности пока сохранится в связи с отсутствием альтернативных веществ.[28]
Цены и рынок
Цены на диоксид титана отличаются в зависимости от степени чистоты и марки. Так, особо чистый (99,999 %) диоксид титана в рутильной и анатазной форме стоил в сентябре 2006 года 0,5—1 доллара за грамм (в зависимости от размера покупки), а технический диоксид титана — 2,2—4,8 доллара за килограмм в зависимости от марки и объёма покупки.
Примечания
- http://www.cdc.gov/niosh/npg/npgd0617.html
- А. Е. Рикошинский. Мировой рынок пигментного диоксида титана. Состояние, тенденции, прогнозы // Лакокрасочные материалы 2002-2003. Справочник. — М.: Редакция еженедельника «Снабженец», 2003. — С. 53-61. — 832 с. — 3000 экз.
- Химическая энциклопедия
- Рабинович. В. А., Хавин З. Я. Краткий химический справочник Л.:Химия, 1977 с. 105
- Краткий справочник физико-химических величин. Изд. 8-е, перераб./Под ред. А. А. Равделя и А. М. Пономаревой. — Л.: Химия, 1983. С.60
- Кроме изменения стандартной энтальпии плавления там же с. 82
- изменение стандартной энтальпии (теплоты образования) при образовании из простых веществ, термодинамически устойчивых при 101,325 кПа (1 атм) и температуре 298 K
- стандартная энтропия при температуре 298 K
- изменение стандартной энергии Гиббса (теплоты образования) при образовании из простых веществ, термодинамически устойчивых при 101,325 кПа (1 атм) и температуре 298 K
- стандартная изобарная теплоёмкость при температуре 298 K
- Изменение энтальпии плавления. Данные по Химической энциклопедии с. 593
- https://monographs.iarc.fr/wp-content/uploads/2018/06/TR42-4.pdf
- Архивированная копия (недоступная ссылка). Дата обращения: 27 января 2017. Архивировано 2 февраля 2017 года.
- Re-evaluation of titanium dioxide (E 171) as a food additive |
- https://efsa.onlinelibrary.wiley.com/doi/10.2903/j.efsa.2018.5366 https://www.efsa.europa.eu/en/efsajournal/pub/5366
- EFSA closes the door on titanium dioxide re-evaluation
- https://www.efsa.europa.eu/en/efsajournal/pub/4545 https://efsa.onlinelibrary.wiley.com/doi/pdf/10.2903/j.efsa.2016.4545 Архивная копия от 30 мая 2021 на Wayback Machine EFSA ANS Panel (EFSA Panel on Food Additives and Nutrient Sources added to Food), 2016. Scientific Opinion on the re-evaluation of titanium dioxide (E 171) as a food additive. EFSA Journal 2016;14(9):4545, 83 pp. doi:10.2903/j.efsa.2016.4545
- Summary of Color Additives for Use in the United States in Foods, Drugs, Cosmetics, and Medical Devices
- e-CFR Title 21 (Food and Drugs) Chapter I Subchapter A Part 73 (LISTING OF COLOR ADDITIVES EXEMPT FROM CERTIFICATION) — § 73.575 Titanium dioxide. (недоступная ссылка). Дата обращения: 7 октября 2018. Архивировано 7 октября 2018 года.
- Во Франции запретили опасную пищевую добавку Е171 (рус.) ?. rosng.ru. Дата обращения: 16 октября 2020.
- Boffey, Daniel E171: EU watchdog says food colouring widely used in UK is unsafe (англ.). the Guardian (6 мая 2021).
- http://49.rospotrebnadzor.ru/rss_all/-/asset_publisher/Kq6J/content/id/444267 Архивная копия от 7 октября 2018 на Wayback Machine — Список Д, Список К
- TiO2 — Двуокись Титана — Диоксид титана, новости, цены, обзоры
- Ученые изобрели бумагу, которая не горит (рус.), Yoki.Ru (27 сентября 2006). Дата обращения 23 ноября 2017.
- На мировом рынке диоксида титана (недоступная ссылка). Новости. Titanmet.ru (16 декабря 2005). Дата обращения: 22 августа 2014. Архивировано 28 сентября 2007 года.
- В странах Евросоюза вступает в силу запрет на использование в производстве продуктов питания диоксида титана E171 // Sputnik, 6.02.2022
- Grätzel, M. Dye-sensitized solar cells (англ.) // Journal of Photochemistry and Photobiology C: Photochemistry Reviews : journal. — 2003. — Vol. 4, no. 2. — P. 145—153.
- COMMISSION REGULATION (EU) 2022/63 // Europa.eu, 18.01.2022
Литература
- Ахметов Т. Г., Порфирьева Р. Т., Гайсин Л. Г. и др. Химическая технология неорганических веществ: в 2 кн. Кн. 1. — Под ред. Т. Г. Ахметова. — М.: Высшая школа, 2002. — ISBN 5-06-004244-8. С. 369—402.
- Некрасов Б. В. Основы общей химии. Т. I. — Изд. 3-е, испр. и доп. М.: Химия, 1973. — С. 644, 648.
- Химическая энциклопедия (электронная версия). — С. 593, 594
- Химия: Справ. изд. / В. Шретер, К.-Х. Лаутеншлегер, Х. Бибрак и др.: Пер. с нем. 2-е изд., стереотип. — М.: Химия, 2000. С. 411.
- Юрьев Ю. Н. Свойства тонких плёнок оксида титана (TiO[2) и аморфного углерода (а-С), осаждённых с помощью дуальной магнетронной распылительной системы: автореферат диссертации на соискание ученой степени кандидата технических наук: спец. 01.04.07]. — Томск, 2016. — 22 с.
Ссылки
- А. Е. Рикошинский. Мировой рынок пигментного диоксида титана. Состояние, тенденции, прогнозы // Лакокрасочные материалы 2002-2003. Справочник. — М.: Редакция еженедельника «Снабженец», 2003. — С. 53-61. — 832 с. — 3000 экз.
- TiO2 — Titanium Dioxide | Двуокись титана (диоксид титана) - Свойства, область применения, производители диоксида титана
- Международная карта химической безопасности для диоксида титана
- Titanium dioxide - Информация из Химической базы данных Акронского университета
