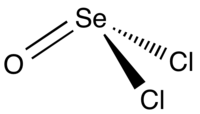
Оксихлорид селена
Оксихлорид селена — неорганическое соединение селена, кислорода и хлора (оксохлорид) с формулой SeOCl2, желтоватая или бесцветная жидкость, разлагается в воде.
| Оксихлорид селена | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Оксихлорид селена |
| Традиционные названия | Оксид-дихлорид селена; хлористый селенил; оксохлорид селена |
| Хим. формула | SeOCl2 |
| Рац. формула | SeCl2O |
| Физические свойства | |
| Состояние | желтоватая или бесцветная жидкость |
| Молярная масса | 165,87 г/моль |
| Плотность | 2,445 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 8,5; 10,8; 11 °C |
| • кипения | 168; 177; 179; 179,4 °C |
| Энтальпия | |
| • образования | -128 [1] кДж/моль |
| Классификация | |
| Рег. номер CAS | 7791-23-3 |
| PubChem | 24647 |
| Рег. номер EINECS | 232-244-0 |
| SMILES | |
| InChI | |
| RTECS | VS7000000 |
| ChemSpider | 23049 |
| Безопасность | |
| Предельная концентрация | 0,1 мг/м³ |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Физические свойства
Оксихлорид селена образует желтоватую или бесцветную гигроскопичную жидкость, которая дымит во влажном воздухе.
Растворяется в сероуглероде, хлороформе, тетрахлорметане, бензине.
Химические свойства
- Реагирует с водой:
При 180 °C разлагается:
- Реагирует с щелочью:
Применение
- Хлорирующий агент.
- Растворитель и компонент растворителей для жидкостных лазеров.
- Пластификатор для полимеров (в химической промышленности).
- Промежуточный продукт для получения высокочистого селена.
Взрыво- и пожароопасность
Вещество негорюче, но многие реакции могут привести к взрыву.
Физиологическое действие
Вещество токсично. ПДК 0,01 мг/л. При попадании на кожу и в глаза оксихлорид селена вызывает раздражение. Взрыво- и пожаробезопасен.
Как и другие соединения селена, на животных хлористый селенил оказывает общетоксическое действие. ЛД50 на крысах — 30 мг/кг.
Примечания
- Chemical Thermodynamics of Selenium. — Elsevier, 2005. — С. 176. — 894 с. — ISBN 9780080457512.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4. — 639 с. — ISBN 5-85270-092-4.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Химический энциклопедический словарь / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1983. — 792 с.
- CRC Handbook of Chemistry and Physics. — 89th Edition. — Taylor and Francis Group, LLC, 2008—2009.
- Руководство по неорганическому синтезу: В 6-ти т. / Ред. Брауэр Г.. — М.: Мир, 1985. — Т. 2. — 338 с.
- Химический энциклопедический словарь / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1983. — 792 с.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.

