Оксид марганца(VII)
Оксид марганца(VII) Mn2O7 — зеленовато-бурая или красная маслянистая жидкость с металлическим блеском, неустойчив при комнатной температуре; сильный окислитель, при соприкосновении с горючими веществами воспламеняет их, возможно со взрывом. Высокотоксичен, сильнейший окислитель.
_%D0%B2_%D1%81%D0%B5%D1%80%D0%BD%D0%BE%D0%B9_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B5.jpg.webp)
| Оксид марганца(VII) | |||
|---|---|---|---|
| |||
| Общие | |||
| Хим. формула | Mn2O7 | ||
| Классификация | |||
| Рег. номер CAS | 12057-92-0 | ||
| PubChem | 13879826 | ||
| Рег. номер EINECS | 235-025-8 | ||
| SMILES | |||
| InChI | |||
| Безопасность | |||
| Токсичность | токсичен | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Физические свойства
Температура плавления — 5,9 °C. Разлагается со взрывом выше 55 °C или при контакте с органическими веществами.
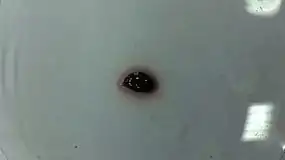
В проходящем свете имеет красную окраску, в отражённом — зелёную. Образует кристаллы тёмно-зелёного цвета.
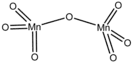
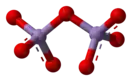
Молекулы состоят из пары тетраэдров с атомами кислорода в вершинах и атомами марганца в центрах. Сходная структура наблюдается у оксида хлора(VII), оксида технеция(VII) и оксида рения(VII).
Химические свойства
Оксид марганца(VII) — соединение кислорода и марганца, ангидрид марганцовой кислоты.
Получение
Получить оксид марганца(VII) Mn2O7 можно действием холодной концентрированной серной кислоты на перманганат калия:
Полученный оксид марганца(VII) неустойчив и разлагается на оксид марганца(IV) и кислород:

Одновременно выделяется озон:
Разложение оксида марганца(VII) сопровождается взрывом:

Взаимодействие с кислотами
Растворяется в серной кислоте, образуя гидросульфат триоксимарганца, более устойчивый при комнатной температуре:
Взаимодействие с органическими веществами
При контакте воспламеняет этиловый спирт, ацетон.