Терпены
Терпе́ны — класс углеводородов — продуктов биосинтеза общей формулы (C5H8)n, с углеродным скелетом, формально являющимся производным изопрена СН2=С(СН3)−СН=СН2[1].

В больших количествах терпены содержатся в хвойных растениях, во многих эфирных маслах. Терпены — основной компонент смол и бальзамов, так, скипидар (эфирное терпентинное масло) получают из живицы (бальзама терпентина). Название «терпены» происходит от лат. oleum terebinthinae — скипидар.
Классификация
Терпены классифицируют по числу изопреновых звеньев, образующих углеродный скелет молекулы:
- Гемитерпены — C5H8,
- Монотерпены (терпены) — C10H16,
- Сесквитерпены (полуторатерпены) — C15H24,
- Дитерпены — C20H32, (C10H16)2,
Терпены с большим количеством конденсированных молекул (звеньев) образуют смолы и каучук.
- Тритерпены — C30H48, (C10H16)3,
- Тетратерпены — C40H64, (C10H16)4,
- Политерпены — (C5H8)n, где n > 8.
Примеры монотерпенов: как углеводороды мирцен и оцимен, а уже как их производные альдегиды и кетоны встречаются в составе многих эфирных масел. Это — цитронеллол, цитраль, лимонен, α-пинен, ментол, миртенол, борнеол, камфора, вербенон и пиперитон. Сесквитерпены есть в сандаловом дереве (β-санталин), в эвкалиптовом масле — кадинол и эвдесмол. Дитерпены встречаются довольно редко, известны α-камфорен, фитол (входит в состав хлорофилла), абиетиновая кислота.
 |
 |
 |
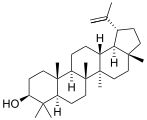 |
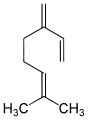
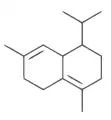
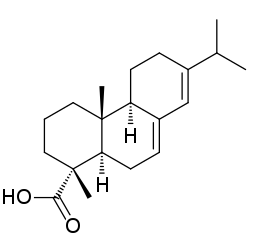
| Монотерпен мирцен | Сесквитерпен кадинен | Дитерпен абиетиновая кислота | Тритерпен лупеол |
Значение и применение
Важные растительные пигменты — каротин и ликопин являются тетратерпенами.
Пример политерпена — каучук из натурального латекса, и его производное — резина.
Эфирные масла растений в значительной степени состоят из моно-, сескви- и дитерпенов и их производных, в том числе:
- альфа-пинен — основной компонент скипидара (соснового масла);
- бета-пинен и дельта-3-карен — содержатся в некоторых видах эфирных масел, во многих маслах являются минорными компонентами;
- лимонен — компонент цитрусовых эфирных масел.
Терпены обычно рассматриваются как углеводороды, не содержащие гетероатомов — в отличие от своих кислородзамещенных производных, так называемых терпеноидов (например, ментол, карвон, туйон), хотя нередко в литературе терпенами называют и терпеноиды.
Примеры
Пинен
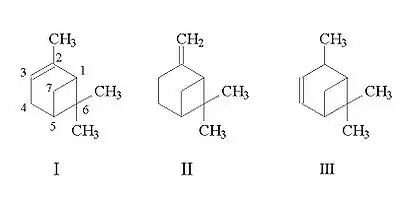
Пинен — бициклический терпен (монотерпен). Известны 3 изомера, отличающихся положением двойной связи. Название пиненов происходит от слова Pinus — сосна (лат.) — это важный компонент смолы хвойных деревьев, скипидара; эфирные масла многих растений содержат пинены. Пинены хорошо распознаются насекомыми и являются важным регулятором их химической коммуникации (см. хеморецепция). Пинены — важный компонент для синтеза камфоры и многих других веществ, часто трансформация пиненов производится с помощью окисления с применением селективных катализаторов. Скипидар, а реже α- и β-пинены применяются как растворители лаков и красок, сырьё для получения соснового масла, политерпеновых смол, терпинеола и душистых веществ. β-Пинен используется для синтеза мирцена.
Изомеры пинена
- 2,6,6-триметилбицикло[3.1.1]гепт-2-ен (2-пинен, α-пинен) (формула I)
- 2-метилен-6,6-диметилбицикло[3.1.1]гептан (нопинен, β-пинен) (формула II)
- 2,6,6-триметилбицикло[3.1.1]гепт-3-ен (δ-пинен) (формула III)
Карены
Карены — бициклические терпены (монотерпены). Известны 4 изомера, отличающихся положением двойной связи. Представляют собой подвижные бесцветные жидкости с запахом, напоминающим аромат сосновой древесины.
Растворимы в органических растворителях, слабо растворимы в этаноле, нерастворимы в воде. 2- и 3-карены получают фракционированием из скипидаров и эфирных масел. Карены быстро окисляются кислородом воздуха и другими окислителями, легко изомеризуются при действии кислотных агентов с раскрытием трехчленного цикла. При действии TiO2, CH3COOH и H2SO4 3-карен изомеризуется в 2-карен. При гидрировании в мягких условиях все карены превращаются в смесь цис- и транс-каранов. 3-карен содержится в скипидарах, получаемых из Pinus roxburghill Sarg. (55—65 %), сосны жёлтой (Pinus ponderosa Dough.) (20—25 %), сосны обыкновенной (Pinus silvestris L.) (20—40 %) и других видов сосен. 2-карен содержится в эфирном масле Andropogon iwarancusa L.. 3-карен применяют для получения душистых веществ, в частности ментола, вальтерилацетата и ряда других веществ.
Лимонен
-Limonen.svg.png.webp)
Лимонен — 1-метил-4-изопропенилциклогексен-1, углеводород группы терпенов. Существует в виде двух оптически активных форм — энантиомеров и в виде рацемической смеси, которую раньше считали одним веществом (дипентен). При нагревании до 300 °C оптически активные формы лимонена рацемизуются в дипентен, при высоких температурах (пропускание паров над раскалённой металлической поверхностью) разлагается с образованием изопрена.
Лимонен окисляется по аллильному положению циклогексенового ядра до карвона, однако в промышленности карвон синтезируют из лимонена нитрозированием нитрозилхлоридом с последующим гидролизом образовавшегося оксима карвона. Дегидрирование лимонена в присутствии серы ведёт к образованию цимола. Лимонен образуется из геранилфосфата через циклизацию промежуточно образующегося карбокатиона. Содержится во многих эфирных маслах (в эфирных маслах цитрусовых до 90 % D-лимонена) и в скипидаре (4—6 % дипентена в скипидаре из живицы сосны обыкновенной Pinus silvestris). D-лимонен ((R)-энантиомер) обладает выраженным цитрусовым запахом и используется в качестве отдушки в парфюмерии и в производстве ароматизаторов. Запах L-лимонена ((S)-энантиомер) напоминает запах хвои, этот энантиомер также используется в качестве отдушки. Обсуждаются его возможные канцерогенные свойства.
Каротин
Каротин (от лат. carota — морковь) — жёлто-оранжевый пигмент, непредельный углеводород из группы каротиноидов. Эмпирическая формула С40H56. Нерастворим в воде, но растворяется в органических растворителях. Содержится в листьях всех растений, а также в корне моркови, плодах шиповника и др. Является провитамином витамина А. Зарегистрирован в качестве пищевой добавки Е160a. Возможны следующие варианты пространственного расположения частей молекулы, определяющие структуру изомера:
- α-каротин β,ε-каротин;
- β-каротин β,β-каротин;
- γ-каротин (с одним β-кольцом и одним нециклизованным концом, что обозначается буквой пси) — β,ψ-каротин;
- δ-каротин (с одним ε-кольцом и одним нециклизованным концом) — ε,ψ-каротин;
- ε-каротин ε,ε-каротин
Свойства
Низшие терпены — прозрачные летучие жидкости, обладающие индивидуальными запахами, липофильные и малорастворимые в воде.
Терпены — лабильные вещества, склонны к изомерии и окислению, в том числе кислородом воздуха.
Примечания
Литература
- Актуальность на конец XIX - начало XX века:. Терпены и их производные // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Пигулевский Г. В. Химия терпенов / Проф. Г. В. Пигулевский; Ленингр. гос. ордена Ленина ун-т им. А. А. Жданова. — Л.: Изд-во ЛГУ, 1949. — 288 с.