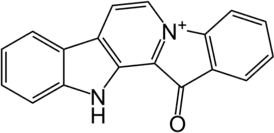
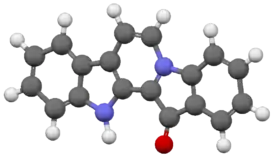
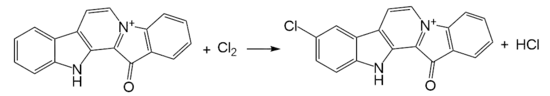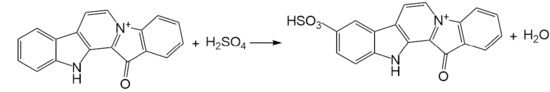Фаскаплизин
Фаскаплизин — бисиндольный алкалоид, родоначальник фаскаплизиновых алкалоидов, впервые выделенный в 1988 году из губки рода Fascaplysinopsis. Обладает широкой биологической активностью, в том числе противоопухолевой и противомикробной[1].
| Фаскаплизин | |
|---|---|
   | |
 | |
| Общие | |
| Систематическое наименование |
12H-пиридо[1,2-a:3,4-b']дииндол |
| Хим. формула | C18H11N2O+ |
| Физические свойства | |
| Состояние | кристаллы кроваво-красного[1] или кирпично-красного[2] цвета |
| Молярная масса | 271,087138±0 г/моль |
| Термические свойства | |
| Температура | |
| • разложения | 232-235[1] °C |
| Химические свойства | |
| Растворимость | |
| • в воде | менее 2 мг/мл[2] |
| • в ДМСО | 20 мг/мл |
| Классификация | |
| Рег. номер CAS | 114719-57-2 |
| PubChem | 73293 |
| SMILES | |
| InChI | |
| ChEBI | 93765 |
| ChemSpider | 66033 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нахождение в природе
В природе встречается в губках рода Fascaplysinopsis, Hyrtios, Thorectandra и оболочниках рода Didemnum[3].
Полный синтез
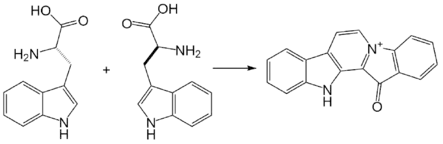
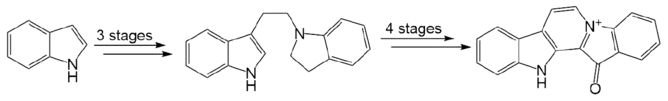
Известно более 10 полных синтезов фаскаплизина[3]. Первый был осуществлён в 1990 году в семь стадий из индола с суммарным выходом в 65%[6]. Ключевой полупродукт — дииндол был получен в три стадии, а затем циклизован и окислен до фаскаплизина[3].
Физико-химические свойства
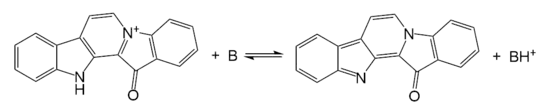
Фаскаплизин образует кристаллы красного цвета с температурой разложения 232-235 °С[1]. Вступает в реакции электрофильного замещения с галогенами и концентрированной серной кислотой по девятому положению. Не образует продукты нитрования при взаимодействии со смесью конценрированных азотной и серной кислот, а также не образует продуктов алкилирования и ацилирования по Фриделю-Крафтсу в классических условиях[7]. Обладает кислотными свойствами, при взаимодействии с основаниями теряет протон образуя незаряженную структуру[8]:
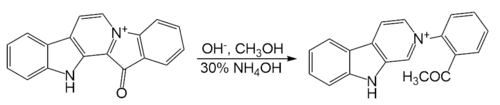
При обработке основаниями в метаноле или гидроксиде аммония образует структуру соответствующую алкалоиду ретикулатину[8]:
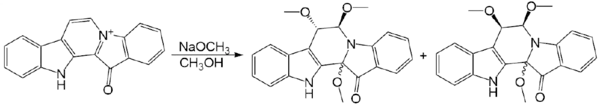
При обработке метилатом натрия в метаноле образует смесь продуктов содержащих три метоксильные группы[8]:
При обработке гидрохлоридом гидроксиламина в пиридине, а затем соляной кислотой в метаноле образуется оксим[8]:
При обработке реактивами Гриньяра и алкиллитиевыми реагентами образуются третичные спирты[8]:
При взаимодействии с хлором в уксусной кислоте при 70 °С образуется 9-хлорфаскаплизин[7]:
При взаимодействии с NBS в уксусной кислоте при 65 °С образуется 9-бромфаскаплизин[7]:
При сульфировании концентрированной серной кислотой образуется цвиттер-ион 9-сульфофаскаплизина[7]:
Биологическая активность
Фаскаплизин проявляет широкий спектр биологической активности. Является селективным ингибитором циклин-зависимой киназы CDK-4, блокирует рост раковых клеток на фазе G0/G1 клеточного цикла. Показывает антипролиферативный эффект в отношении клеток HeLa рака шейки матки и супрессию пролиферации клеток мышиной лейкемии. Обладает анти-ангиогенезной активностью за счет блокирования фактора роста эндотелия сосудов (VEGF). Показывает противомикробное действие против Staphylococcus aureus, Escherichia coli, Candida albicans, Saccharomyces cerevisae[3].
Примечания
- Roll, 1988-07.
- Fascaplysin chloride hydrate (англ.). Дата обращения: 9 апреля 2019.
- Bharate, 2012-12.
- Jimenez, 1991-05.
- Segaraves, 2004-05.
- Pelcman, 1990-01.
- Fretz, 2000-11.
- Fretz, 2001-04.
Источники
- Deborah M. Roll, Chris M. Ireland, Helen S. M. Lu, Jon Clardy. Fascaplysin, an unusual antimicrobial pigment from the marine sponge Fascaplysinopsis sp (англ.) // The Journal of Organic Chemistry. — 1988-07. — Vol. 53, iss. 14. — P. 3276–3278. — ISSN 1520-6904 0022-3263, 1520-6904. — doi:10.1021/jo00249a025.
- S. B. Bharate, S. Manda, N. Mupparapu, N. Battini, R. A. Vishwakarma. Chemistry and Biology of Fascaplysin, a Potent Marine-Derived CDK-4 Inhibitor (англ.) // Mini-Reviews in Medicinal Chemistry. — 2012-12. — Vol. 12, iss. 7. — P. 650-664. — ISSN 13895575. — doi:10.2174/138955712800626719.
- Benjamin Pelcman, Gordon W Gribble. Total synthesis of the marine sponge pigment fascaplysin (англ.) // Tetrahedron Letters. — 1990-01. — Vol. 31, iss. 17. — P. 2381–2384. — doi:10.1016/S0040-4039(00)97367-2.
- Heinz Fretz, Katharina Ucci-Stoll, Paul Hug, Joseph Schoepfer, Marc Lang. Investigations on the Reactivity of Fascaplysin, Part I, Aromatic Electrophilic Substitutions Occur at Position 9 (англ.) // Helvetica Chimica Acta. — 2000-11. — Vol. 83, iss. 11. — P. 3064-3068. — doi:10.1002/1522-2675(20001108)83:11<3064::AID-HLCA3064>3.0.CO;2-P.
- Heinz Fretz, Katharina Ucci-Stoll, Paul Hug, Joseph Schoepfer, Marc Lang. Investigations on the Reactivity of Fascaplysin, Part II, General Stability Considerations and Products Formed with Nucleophiles (англ.) // Helvetica Chimica Acta. — 2001-04. — Vol. 84, iss. 4. — P. 867-873. — doi:10.1002/1522-2675(20010418)84:4<867::AID-HLCA867>3.0.CO;2-A.
- Carlos Jimenez, Emilio Quinoa, Madeline Adamczeski, Lisa M. Hunter, Phillip Crews. Novel sponge-derived amino acids. 12. Tryptophan-derived pigments and accompanying sesterterpenes from Fascaplysinopsis reticulata // The Journal of Organic Chemistry. — 1991-05. — Т. 56, вып. 10. — С. 3403–3410. — ISSN 1520-6904 0022-3263, 1520-6904. — doi:10.1021/jo00010a041.
- Nathaniel L. Segraves, Sarah J. Robinson, Daniel Garcia, Sadri A. Said, Xiong Fu. Comparison of Fascaplysin and Related Alkaloids: A Study of Structures, Cytotoxicities, and Sources // Journal of Natural Products. — 2004-05. — Т. 67, вып. 5. — С. 783–792. — ISSN 1520-6025 0163-3864, 1520-6025. — doi:10.1021/np049935+.