Пурин
Пури́н — простейший представитель имидазо[4,5-d]пиримидинов. При нормальных условиях — бесцветные кристаллы, хорошо растворимые в воде, горячем этаноле и бензоле, плохо растворимые в диэтиловом эфире, ацетоне и хлороформе.
| Пурин | |||
|---|---|---|---|
 | |||
| Общие | |||
| Систематическое наименование |
имидазо[4,5-d]пиримидин | ||
| Традиционные названия | пурин | ||
| Хим. формула | C5N4H4 | ||
| Физические свойства | |||
| Состояние | твёрдое, бесцветные кристаллы | ||
| Молярная масса | 120,1121 ± 0,0051 г/моль | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 214 °C | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 50 г/100 мл | ||
| Классификация | |||
| Рег. номер CAS | 120-73-0 | ||
| PubChem | 1044 | ||
| Рег. номер EINECS | 204-421-2 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 35584 | ||
| ChemSpider | 1015 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Реакционная способность
Пурин проявляет амфотерные свойства (рКа 2,39 и 9,93), образуя соли с сильными минеральными кислотами и металлами (замещается водород имидазольного цикла).
Для пурина характерна прототропная таутомерия по имидазольному атому водорода, в водных растворах в таутомерном равновесии присутствует смесь 7H- и 9H-таутомеров:
Ацилирование и алкилирование пурина идет по имидазольным атомам азота. Так, при ацилировании уксусным ангидридом образуется смесь 7- и 9-ацетилпуринов, при алкилировании метилйодидом серебряной соли пурина либо диметилсульфатом в щелочных условиях образуется 9-метилпурин, действие избытка йодистого метила в диметилформамиде ведет к кватернизации с образованием йодида 7,9-диметилпуриния.
Пурин — электрондефицитная гетероциклическая система, поэтому реакции электрофильного замещения для него нехарактерны. При действии пероксида водорода, подобно пиридину, образует N-оксиды (смесь 1- и 3-оксидов при действии H2O2 в уксусном ангидриде).
При сплавлении с серой при 245 °С тионируется по имидазольному циклу с образованием 8-меркаптопурина.
Синтез
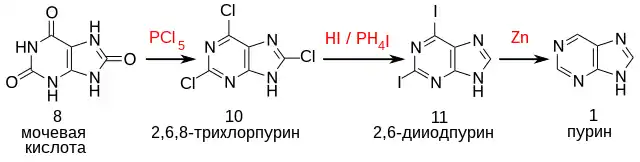
Впервые пурин был синтезирован Эмилем Фишером из мочевой кислоты 8 замещением кислорода на хлор действием пентахлорида фосфора и дальнейшим восстановлением образовавшегося 2,6,8-трихлорпурина 10:
Благодаря доступности мочевой кислоты метод Фишера сохранил некоторое значение и до настоящего времени, восстановление 2,6,8-трихлорпурина проводится цинковой пылью.
Другим исторически значимым методом является конденсация 4,5-диаминапиримидина с безводной муравьиной кислотой в инертной атмосфере (вариант синтеза пуринов по Траубе)[1]
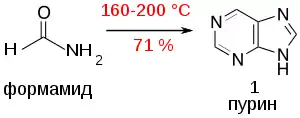
На сегодняшний день, вероятно, наиболее простым и доступным лабораторным методом синтеза пурина является нагревание формамида при 170-190 °C в течение ~30 часов; в этих условиях в реакцию вступает ~30% формамида, выход по израсходованному формамиду составляет 71%[2]:
Биологическое значение

Производные пурина играют важную роль в химии природных соединений (пуриновые основания ДНК и РНК; является коферментом никотинамидадениндинуклеотида (NAD); входит в состав алкалоидов: кофеина, теофиллина и теобромина; в состав токсинов, сакситоксин и родственные к пурину соединения: мочевая кислота) и, благодаря этому, используется в фармацевтике.
Некоторые биохимические производные пурина приведены на рисунке.
Нарушения метаболизма пуриновых оснований в организме могут вызывать заболевание подагрой[3].
Примечания
- Isay, Oskar (1906-01). “Eine Synthese des Purins”. Berichte der deutschen chemischen Gesellschaft. 39 (1): 250—265. DOI:10.1002/cber.19060390149. eISSN 1099-0682. ISSN 0365-9496. Дата обращения 2020-09-22. Проверьте дату в
|date=(справка на английском) - Yamada, Hiroshi; Okamoto, Toshihiko (1972). “A One-step Synthesis of Purine Ring from Formamide”. CHEMICAL & PHARMACEUTICAL BULLETIN. 20 (3): 623—624. DOI:10.1248/cpb.20.623. eISSN 1347-5223. ISSN 0009-2363. Дата обращения 2020-09-22.
- Schlesinger N (March 2010). “Diagnosing and treating gout: a review to aid primary care physicians”. Postgrad Med. 122 (2): 157—61. DOI:10.3810/pgm.2010.03.2133. PMID 20203467.