Тенофовир алафенамид
Тенофовира алафенамид фумарат (МНН, ранее GS-7340) — нуклеотидный ингибитор обратной транскриптазы и пролекарство тенофовира. Он находится в стадии разработки компанией Gilead. Предназначен для лечения ВИЧ-инфекции и хронического гепатита В, применяется в виде Тенофовир алафенамид фумарат (ТАФ). Тесно связан с широко используемым ингибитором обратной транскриптазы Тенофовир дизопроксил, ТАФ обладает большей противовирусной активностью и лучше распределяется в лимфоидных тканях[1][2].
| Тенофовир алафенамид | |
|---|---|
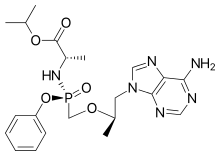 | |
| Химическое соединение | |
| ИЮПАК | изопропил (2S)-2-[[[(1R)-2-(6-аминопурин-9-ил)-1-метил-этокси]метил-фенокси-фосфорил]амино]пропаноат |
| Брутто-формула | C21H29N6O5P |
| Молярная масса | 476,466 |
| CAS | 379270-37-8 |
| PubChem | 9574768 |
| DrugBank | 09299 |
| Состав | |
| Классификация | |
| АТХ | J05AR18 J05AR19 |
| Фармакокинетика | |
| Период полувывед. | 0,51 час |
| Экскреция | Кал (31,7 %), моча (<1 %) |
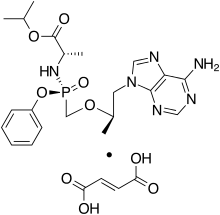
История
В ноябре 2015 года FDA одобрило схемы лечения ВИЧ-1, основанные на применении Тенофовир алафенамида.[3] Gilead оказалась первой фармкомпанией, получившей одобрение FDA на применение препаратов на основе Тенофовир алафенамида[3]. В январе 2017 года индийский фармацевтический производитель Hetero начинает серийное производство Тенофовир алафенамид/эмтрицитабин под торговой маркой Tafero-EM.
Компания Gilead объявила о разработке вариантов препарата с кобицистатом, эмтрицитабином и ингибитором протеазы дарунавиром.[4][5][6] В 48-недельном исследовании проходило сравнение элвитегравир/кобицистат/эмтрицитабин/тенофовир дизопроксил с элвитегравир/кобицистат/эмтрицитабин/тенофовир алафенамид (торговое название Genvoya). Результаты показали, что новый препарат не уступает предыдущему, требуются гораздо меньшие дозы, частотой побочных эффектов значительно ниже, особенно таких как нарушение функции почек[7][8][9].
Также компания Gilead в 2018 году объявила об успешном окончании клинических испытаний в Китае комбинированного препарата Тенофовир алафенамид с кобицистатом, эмтрицитабином и элвитегравиром[10], фаза 3 испытаний проводится в США с 2013г[11]).
Примечания
- Eisenberg, E. J.; He, G. X.; Lee, W. A. Metabolism of Gs-7340, A Novel Phenyl Monophosphoramidate Intracellular Prodrug of Pmpa, in Blood (англ.) // Nucleosides, Nucleotides and Nucleic Acids : journal. — 2001. — Vol. 20, no. 4—7. — P. 1091—1098. — doi:10.1081/NCN-100002496. — PMID 11562963.
- M Markowitz, A Zolopa, et al.
- U.S. Food and Drug Administration Approves Gilead's Single Tablet Regimen Genvoya (Elvitegravir, Cobicistat, Emtricitabine and Tenofovir Alafenamide) for Treatment of HIV-1 Infection, Gilead (5 ноября 2015). Архивировано 24 января 2016 года. Дата обращения 30 января 2016.
- McQueen, Courtney. Gilead And Tibotec To Develop Single-Pill Protease Inhibitor-Based Combination Regimen (недоступная ссылка). The AIDS Beacon (16 ноября 2011). Дата обращения: 30 января 2016. Архивировано 6 марта 2016 года.
- GS-7340 Packs Greater HIV Punch, Potentially Better Safety, Versus Viread Архивная копия от 8 сентября 2015 на Wayback Machine Horn, Tim. 15 Mar 2012.
- Pharmacokinetics of a Novel EVG/COBI/FTC/GS-7340 Single Tablet Regimen. 13th International Workshop on Clinical Pharmacology of HIV Therapy.
- Once-Daily Tenofovir Prodrug Combo Pill as Effective as Stribild Архивная копия от 20 сентября 2015 на Wayback Machine.
- CROI 2013: New Pro-drug Tenofovir Alafenamide Appears Equally Effective but Better Tolerated.
- Horn, T. et al.
- China National Medical Products Administration Approves Descovy® (Emtricitabine, Tenofovir Alafenamide) for the Treatment of HIV-1 Infection (8 декабря 2018).
- Gilead (January 2013). Gilead Initiates Phase 3 Clinical Program for Tenofovir Alafenamide. Пресс-релиз. Архивировано из первоисточника 7 февраля 2013.
Ссылки
- Federally approved HIV/AIDS medical practice guidelines. (англ.). A service of the U.S. Department of Health and Human Services (HHS). Дата обращения: 30 января 2016.rm link