Атазанавир
Атазанавир, продаваемый под торговой маркой Reyataz, представляет собой антиретровирусный препарат (АРТ), используемый для лечения ВИЧ/СПИДа. Обычно его рекомендуется использовать с другими антиретровирусными препаратами. Его можно использовать для профилактики после укола иглой или другого потенциального контакта (постконтактная профилактика (PEP)). Его принимают внутрь один раз в день.
| Атазанавир | |
|---|---|
 | |
 | |
| Химическое соединение | |
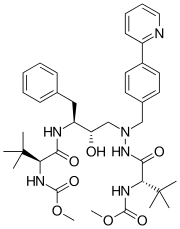
| ИЮПАК | methyl N-[(1S)-1-{[(2S,3S)-3-hydroxy-4-[(2S)-2-[(methoxycarbonyl)amino]-3,3-dimethyl-N'-{[4-(pyridin-2-yl)phenyl]methyl}butanehydrazido]-1-phenylbutan-2-yl]carbamoyl}-2,2-dimethylpropyl]carbamate |
| Брутто-формула | C38H52N6O7 |
| CAS | 198904-31-3 |
| PubChem | 148192 |
| DrugBank | DB01072 |
| Состав | |
| Классификация | |
| АТХ | J05AE08 |
| Фармакокинетика | |
| Биодоступн. | 60-68% |
| Связывание с белками плазмы | 86% |
| Метаболизм | Печень (CYP3A4) |
| Период полувывед. | 6.5 часов |
| Экскреция | Кал и почки |
| Способы введения | |
| Перорально | |
Общие побочные эффекты включают головную боль, тошноту, желтуху, боль в животе, проблемы со сном и лихорадку. К серьезным побочным эффектам относятся сыпь, например, многоформная эритема и высокий уровень сахара в крови. Атазанавир безопасен для использования во время беременности. Он относится к классу ингибиторов протеазы (ИП) и действует путем блокирования протеазы ВИЧ.
Атазанавир был одобрен для медицинского применения в США в 2003 г.. Препарат включен в Примерный перечень ВОЗ основных лекарственных средств[2]. В Соединенных Штатах он недоступен в качестве дженерика[3].
Медицинское использование
Атазанавир используется для лечения ВИЧ. Эффективность атазанавира оценивалась в ряде хорошо спланированных испытаний у взрослых, не получавших АРТ и получавших АРТ.
Атазанавир отличается от других ингибиторов протеаз тем, что он меньше влияет на липидный профиль и, по-видимому, с меньшей вероятностью вызывает липодистрофию. Может быть некоторая перекрестная резистентность с другими ингибиторами протеаз.
Беременность
Никаких доказательств вреда среди беременных пациентов, принимавших атазанавир, обнаружено не было. Это одно из предпочтительных лекарств от ВИЧ для беременных женщин, которые раньше не принимали лекарства от ВИЧ[5].
Противопоказания
Атазанавир противопоказан пациентам с гиперчувствительностью в анамнезе (например, с синдромом Стивенса-Джонсона, мультиформной эритемой или токсическими кожными высыпаниями). Кроме того, атазанавир не следует назначать с альфузозином, рифампином, иринотеканом, луразидоном, пимозидом, триазоламом, пероральным введением мидазолама, производных спорыньи, цизаприда, зверобоем, ловастатином, симвастатином, силденафилом, индинавиром или невирапином[6].
Побочные эффекты
Общие побочные эффекты включают: тошноту, желтуху, сыпь, головную боль, боль в животе, рвоту, бессонницу, периферические неврологические симптомы, головокружение, мышечную боль, диарею, депрессию и лихорадку[6]. Уровень билирубина в крови обычно бессимптомно повышается при приеме атазанавира, но иногда может привести к желтухе.
Механизм действия
Атазанавир связывается с протеазой ВИЧ активного центра и предотвращает расщепление проформы вирусных белков рабочими механизмами вируса[7]. Если фермент протеазы ВИЧ не работает, вирус не заразен и зрелые вирионы не образуются[8][9]. Лекарственное средство азапептид было разработано как аналог субстрата пептидной цепи, который протеаза ВИЧ обычно расщепляет на активные вирусные белки. В частности, атазанавир является структурным аналогом переходного состояния, во время которого разрывается связь между фенилаланином и пролином[10][11].
Состав
Атазанавир выпускается в виде капсулы 150/200/300 мг и пакета перорального порошка 50 мг.[6]. Капсула 300 мг должна уменьшить количество таблеток, так как одна капсула 300 мг может заменить две капсулы по 150 мг.[12].
Примечания
- World Health Organization model list of essential medicines: 21st list 2019. — Geneva : World Health Organization, 2019. — ISBN WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- Richard J. Hamilton, 2015, с. 67.
- "What's New in the Guidelines? Adult and Adolescent ARV Guidelines". AIDSinfo. Дата обращения: 4 мая 2021. Архивировано 15 ноября 2016 года.
- "Reyataz Package Insert" (PDF). Food and Drug Administration (September 2016). Дата обращения: 4 мая 2021.
- "Atazanavir". DrugBank (12 October, 2018). Дата обращения: 4 мая 2021. Архивировано 9 ноября 2016 года.
- Kohl, NE; Emini, EA; Schleif, WA; Davis, LJ; Heimbach, JC; Dixon, RA; Scolnick, EM; Sigal, IS (1 July 1988). “Active human immunodeficiency virus protease is required for viral infectivity”. Proceedings of the National Academy of Sciences of the United States of America. 85 (13): 4686—4690. Bibcode:1988PNAS...85.4686K. DOI:10.1073/pnas.85.13.4686. ISSN 0027-8424. PMC 280500. PMID 3290901.
- Lv, Z; Chu, Y; Wang, Y (2015). “HIV protease inhibitors: a review of molecular selectivity and toxicity”. HIV/AIDS – Research and Palliative Care. 7: 95—104. DOI:10.2147/HIV.S79956. PMC 4396582. PMID 25897264.
- Graziani, Amy L (June 17, 2014). "HIV protease inhibitors". UpToDate.
- Bold, G; Fässler, A; Capraro, HG; Cozens, R; Klimkait, T; Lazdins, J; Mestan, J; Poncioni, B; Rösel, J; Stover, D; Tintelnot-Blomley, M; Acemoglu, F; Beck, W; Boss, E; Eschbach, M; Hürlimann, T; Masso, E; Roussel, S; Ucci-Stoll, K; Wyss, D; Lang, M (August 1998). “New Aza-Dipeptide Analogues as Potent and Orally Absorbed HIV-1 Protease Inhibitors: Candidates for Clinical Development”. Journal of Medicinal Chemistry. 41 (18): 3387—3401. DOI:10.1021/jm970873c. PMID 9719591.
- Perazzolo S, Shireman LM, McConnachie LA, Koehn J, Shen DD, Ho RJ (Dec 2018). “Three HIV drugs, atazanavir, ritonavir, and tenofovir, co-formulated in drug-combination nanoparticles exhibit long-acting and lymphocyte-targeting properties in nonhuman primates”. Journal Pharmaceutical Sciences. 107 (12): 3153—3162. DOI:10.1016/j.xphs.2018.07.032. PMC 6553477. PMID 30121315.
Литература
- Richard J. Hamilton. Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. — Jones and Bartlett Publishers, 2015. — 510 с. — ISBN 978-1284057560.
