Тенофовир/эмтрицитабин
Тенофовир/эмтрицитабин, известный под торговой маркой Truvada — комбинация двух антиретровирусных препаратов, используемая для лечения и профилактики ВИЧ-инфекции. Препарат включает 300 мг тенофовира (в виде пролекарства тенофовира дизопроксила фумарата) и 200 мг эмтрицитабина. Сочетание двух препаратов в одной пилюле снижает количество таблеток, которые должен ежедневно принимать пациент и повышает комплаентность антиретровирусной терапии.
| Тенофовир/эмтрицитабин | |
|---|---|
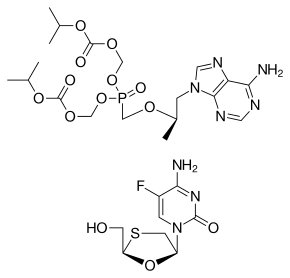 | |
| Химическое соединение | |
| Брутто-формула | C31H44FN8O17PS |
| PubChem | 11954236 |
| Состав | |
|
|
| Классификация | |
| АТХ | J05AR03 |
| Лекарственные формы | |
| Таблетки | |
| Способы введения | |
| Орально | |
| Другие названия | |
| Трувада | |
Препарат был исследован в качестве профилактического средства в отношении ВИЧ-инфекции. Исследования Cochrane показали, что тенофовир самостоятельно и в сочетании с эмтрицитабином значительно снижает риск заражения ВИЧ.[1] В мае 2012 года Комитет по антиретровирусным препаратам рекомендовал FDA назначать препарат неинфицированным мужчинам, имеющим половые контакты с несколькими партнерами-мужчинами.[2] 16 июля 2012 года FDA рекомендовало применение комбинации тенофовира/эмтрицитабина для снижения риска заражения ВИЧ.[3][4]
Лекарственный препарат имеет следующие побочные эффекты: тошнота, рвота, головокружение, снижение аппетита, диарея, препарат токсичен для печени и почек и вызывает снижение плотности костей.
Клинические исследования

Двойное слепое, рандомизированное, многоцентровое, плацебо-контролируемое исследование препарата показало, что ежедневное однократное применение эмтрицитабина/тенофовира и лопинавира/ритонавира или усиленного атазанавира или эфавиренца были эффективны в качестве первых препаратов для лечения ВИЧ-1.[5]
В других рандомизированных исследованиях эмтрицитабин/тенофовир в дозировке 200 мг/300 мг однократно ежедневно был эффективен в качестве первого препарата при лечении ВИЧ-1.[5][6]
Эмтрицитабин/тенофовир в сочетании с ингибиторами протеазы хорошо переносились взрослыми ВИЧ-инфицированными пациентами.[5]
Препарат «Трувада» был разработан компанией «Gilead Sciences» и разрешен к использованию FDA в 2004 году[7].
Примечания
- Okwundu C.I., Uthman O.A., Okoromah CAN. Antiretroviral pre-exposure prophylaxis (PrEP) for preventing HIV in high-risk individuals (англ.) // Cochrane Database Syst Rev : journal. — 2012. — No. 7. — P. CD007189. — doi:10.1002/14651858.CD007189.pub3. — PMID 22786505.
- HIV prevention pill Truvada backed by US experts (11 мая 2012).
- FDA approves first pill to help prevent HIV (16 июля 2012). Архивировано 21 декабря 2016 года.
- FDA approves first drug for reducing the risk of sexually acquired HIV infection
- Perry CM. Архивная копия от 24 февраля 2012 на Wayback Machine.Drugs 2009;69(7):843-857. doi:10.2165/00003495-200969070-00005.
- Jon Cohen. A Powerful and Perplexing New HIV Prevention Tool (англ.) // Science. — 2010. — 3 December (vol. 330). — P. 1298. — doi:10.1126/science.330.6009.1298.
- FDA Approves Two Fixed-Dose Combination Drug Products for the Treatment of HIV-1 Infection
Ссылки
Литература
- Kazmierski W.M. (Editor). Antiviral drugs: From basic discovery through clinical trials. — John Wiley and Sons., Inc., 2011. — С. 85—102. — 438 с. — ISBN 978-0-470-45563-0.