Адефовир
Адефовир (англ. Adefovir, ранее bis-POM PMEA) — рецептурное лекарство, используемое для лечения от вируса гепатита B (ВГВ). Распространяется под торговыми наименованиями Preveon и Hepsera. Это пероральный нуклеотидный аналог ингибитора обратной транскриптазы (ntRTI).
| Адефовир | |
|---|---|
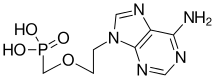 | |
| Химическое соединение | |
| ИЮПАК | {[2-(6-амино-9H-пурин-9-ил)этокси]метил}фосфоновая кислота |
| Брутто-формула | C8H12N5O4P |
| Молярная масса | 273,186 г/моль |
| CAS | 106941-25-7 |
| PubChem | 60172 |
| DrugBank | DB00718 |
| Состав | |
| Классификация | |
| АТХ | J05AF08 |
| Фармакокинетика | |
| Биодоступн. | 59% |
| Связывание с белками плазмы | <4% |
| Период полувывед. | 7,5 часа |
| Экскреция | Моча |
| Способы введения | |
| Орально | |
Применение
Адефовир используется для лечения гепатита B[1][2] и вируса простого герпеса[3].
Испытания адефовира у пациентов с ВИЧ, не демонстрирует никаких очевидных преимуществ[3][4].
История
Адефовир был изобретён в Институте органической химии и биохимии Академии наук Чешской Республики химиком Антонином Голи. Препарат разрабатывался компанией Gilead Sciences для лечения ВИЧ под маркой Preveon. Тем не менее, в ноябре 1999 года группа экспертов посоветовала FDA не одобрять препарат из-за опасений по поводу тяжести и частоты почечной токсичности при дозировке 60 или 120 мг. FDA последовала этому совету, отказавшись утвердить адефовир в качестве средства для лечения ВИЧ.
Gilead Sciences прекратила его разработку для лечения ВИЧ-инфекции в декабре 1999 г., но продолжила работать с ним как с препаратом для лечения гепатита В (HBV), в чём он оказался эффективен в гораздо меньшей дозе: 10 мг. Одобрение от FDA для использования в лечении гепатита В в США было получено 20 сентября 2002 г., после чего адефовир продаётся под маркой Hepsera. В марте 2003 года адефовир получил одобрение для лечения ВГВ и в Европейском Союзе.
Механизм действия
Адефовир работает путём блокирования обратной транскриптазы, фермента, который имеет решающее значение для размножения ВГВ в организме. Он одобрен для лечения хронического гепатита В у взрослых с признаками активной репликации вируса, о которой свидетельствует стойкое повышение аминотрансфераз (в первую очередь АЛТ) в сыворотке крови, или гистологически активной болезни.
Основным преимуществом адефовира по сравнению с ламивудином (первый ингибитор обратной транскриптазы, одобренный для лечения ВГВ) является то, что вирус гораздо дольше вырабатывает устойчивость к препарату.
Примечания
- Marcellin P., Chang T. T., Lim S. G., Tong M. J., Sievert W., Shiffman M. L., Jeffers L., Goodman Z., Wulfsohn M. S., Xiong S., Fry J., Brosgart C. L. Adefovir dipivoxil for the treatment of hepatitis B e antigen-positive chronic hepatitis B. (англ.) // The New England journal of medicine. — 2003. — Vol. 348, no. 9. — P. 808—816. — doi:10.1056/NEJMoa020681. — PMID 12606735.
- Manolakopoulos S., Bethanis S., Koutsounas S., Goulis J., Vlachogiannakos J., Christias E., Saveriadis A., Pavlidis C., Triantos C., Christidou A., Papatheodoridis G., Karamanolis D., Tzourmakliotis D. Long-term therapy with adefovir dipivoxil in hepatitis B e antigen-negative patients developing resistance to lamivudine. (англ.) // Alimentary pharmacology & therapeutics. — 2008. — Vol. 27, no. 3. — P. 266—273. — doi:10.1111/j.1365-2036.2007.03567.x. — PMID 17988233.
- A randomized placebo-controlled trial of adefovir dipivoxil in advanced HIV infection: the ADHOC trial. (англ.) // HIV medicine. — 2002. — Vol. 3, no. 4. — P. 229—238. — doi:10.1046/j.1468-1293.2002.00111.x. — PMID 12444940.
- Fisher E. J., Chaloner K., Cohn D. L., Grant L. B., Alston B., Brosgart C. L., Schmetter B., El-Sadr W. M., Sampson J. The safety and efficacy of adefovir dipivoxil in patients with advanced HIV disease: a randomized, placebo-controlled trial. (англ.) // AIDS (London, England). — 2001. — Vol. 15, no. 13. — P. 1695—1700. — doi:10.1097/00002030-200109070-00013. — PMID 11546945.
Ссылки
- Adefovir Dipivoxil (англ.). Drugs.com. Дата обращения: 14 мая 2016.
- Label and Approval History.. Active Ingredient(s): Adefovir dipivoxil (англ.). FDA. Дата обращения: 14 мая 2016.