Тетраборат натрия
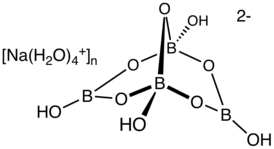
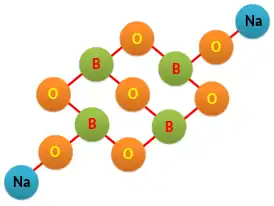
Тетрабора́т на́трия («бура́», «боракс» (от лат. borax), натрий тетраборнокислый) — неорганическое соединение, натриевая соль борной кислоты с химической формулой , наиболее распространённое и используемое соединение бора, образует несколько кристаллогидратов, широко применяется в промышленности.
| Тетраборат натрия | |
|---|---|
  | |
  | |
| Общие | |
| Традиционные названия | бура, боракс |
| Хим. формула | Na2B4O7 |
| Физические свойства | |
| Состояние | кристаллы |
| Молярная масса | 201,22 г/моль |
| Плотность | 2,37 ± 0,01 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления |
664 °C (β-модификация) 710 °C (γ-модификация) |
| • кипения | 1575 °C |
| • разложения | 2867 ± 1 ℉[1] |
| Давление пара | 0 ± 1 мм рт.ст.[1] |
| Химические свойства | |
| Растворимость | |
| • в воде |
3,2 г/100 мл (25 °C) 10,5 г/100 мл (50 °C) |
| • в этаноле | 0,05 (25 °C) |
| • в ацетоне | 0,006 (25 °C) |
| Классификация | |
| PubChem | 10219853 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E285 |
| RTECS | VZ2275000 и ED4588000 |
| ChemSpider | 8395345 |
| Безопасность | |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нахождение в природе
Существуют многочисленные минералы, содержащие тетраборат натрия. К ним относятся:
- бура (боракс, тинкал) — минерал состава — декагидрат тетрабората натрия;
- кернит — тетрагидрат тетрабората натрия — ;
- многочисленные минералы класса боратов, в которых помимо оксидов натрия и бора содержатся другие металлы, — кальций, магний, железо и др.;
- кристаллогидраты тетрабората натрия выпадают в осадок при пересыхании некоторых бессточных, сезонно пересыхающих солёных озёр, например, в озере Серлс, расположенном в пустыне Мохаве в США, и некоторых озёр в Турции.
Физические свойства
Имеет две метастабильные модификации: β и γ. β-модификация является ромбической с температурой плавления 664 °C, γ-модификация — моноклинная с температурой плавления 710 °C. Температура кипения — 1575 °C. При быстром охлаждении расплава образуется аморфная стекловидная масса с плотностью 2,36 г/см3[2]. При медленном охлаждении образуется α-форма (ромбические кристаллы)[3].
Химические свойства
Растворимость в воде составляет 3,2 г /100 мл (при 25 °C), 10,5 г / 100 мл (при 50 °C), в этаноле — 0,05 г / 100 г (при 25 °C), ацетоне — 0,006 г / 100 г (при 25 °C), не растворим в диэтиловом эфире и глицерине. Реагирует с метанолом при растворении с образованием бороорганических соединений[2].
Образует несколько кристаллогидратов с разным содержанием воды. Эти кристаллогидраты и безводный тетраборат натрия обычно называют «бура́». Примеры кристаллогидратов:
- пентагидрат (), так называемая «ювелирная бура», используется при пайке ювелирных изделий;
- декагидрат ().
Однако наиболее часто «буро́й» называют декагидрат . Эта соль представляет собой прозрачные кристаллы с молярной массой 381,43 г/моль, имеющие хорошую растворимость в тёплой воде[4]. При нагревании свыше 400 °C полностью теряет кристаллизационную воду.
Так как тетраборат натрия является солью слабой кислоты и сильного основания, в воде гидролизуется. Водный раствор тетрабората натрия имеет щелочную реакцию.
Взаимодействует с сильными кислотами, образуя соответствующую соль и борную кислоту:
- .
Многие соли металлов борной кислоты нерастворимы в воде и при взаимодействии в растворе их растворимых солей с тетраборатом натрия образующиеся бораты выпадают в осадок. На этом основано применение буры для «умягчения» воды:
- ,
- .
С оксидами многих переходных металлов бура при сплавлении образует разнообразно окрашенные соединения — бораты «перлы буры». По цвету перлов можно судить о качественном химическом составе пробы.
Соединение окрашивает пламя горелки в зелёный цвет (характерная реакция на соединения бора)[4].
Получение
Десятиводную соль получают из природных минералов, например, буры или кернита, осуществляя их перекристаллизацию. Также для этой цели применяют химическое взаимодействие некоторых природных боратов (ашарита и улексита) с карбонатом или гидрокарбонатом натрия[2].
Может быть получен реакцией карбоната натрия и борной кислоты при нагреве, пропусканием углекислого газа через раствор метабората натрия[2].
Применение
Тетраборат натрия применяется:
- как сырьё для получения борной кислоты и различных соединений бора[2];
- в производстве эмалей, глазурей, оптических и цветных стёкол, различных керамик[2];
- при пайке и плавке металлов в составе флюса[2];
- при ковке металлов;
- в бумажной и фармацевтической промышленности;
- в производстве строительных материалов как компонент антисептика для изготовления целлюлозного утеплителя «Эковата»
- как дезинфицирующее и консервирующее средство[2];
- для приготовления буферных растворов;
- в аналитической химии:
- в фотографии — в составе медленно действующих проявителей в качестве слабого ускоряющего вещества[4];
- как компонент моющих средств[2];
- как компонент косметики;
- как инсектицид в отравленных приманках для уничтожения тараканов;
- используется в слаймах.
В 1977 году мировое производство тетрабората натрия составило 1,5 млн тонн[2].
Токсичность
Вещество малотоксично для теплокровных животных, ЛД50 для крыс 2,66 г/кг. Пыль может вызывать раздражение слизистых оболочек и неблагоприятно влияет на органы дыхания.
Имеются сведения, что вещество снижает фертильность. По нормам Европейского союза (ЕС) вещества и смеси, импортируемые в ЕС и содержащие буру, с июля 2015 года должны быть маркированы предупреждениями «Может нанести ущерб фертильности» и «Может нанести вред нерожденному ребёнку»[5].
Также указывается, что длительное, в течение 10—15 лет потребление буры в виде пищевых добавок может провоцировать онкологические заболевания[6].
См. также
Примечания
- http://www.cdc.gov/niosh/npg/npgd0057.html
- Федоров, 1992.
- Franz v Bruchhausen, Siegfried Ebel, Eberhard Hackenthal, Ulrike Holzgrabe. Hagers Handbuch der Pharmazeutischen Praxis: Folgeband 5: Stoffe L-Z. — Springer-Verlag, 2013. — 299 с. — ISBN 978-3-642-58388-9.
- Иофис, 1981.
- Recommendation of the European Chemicals Agency of 1 July 2015 for the inclusion of substances in Annex XIV to REACH (List of Substances subject to Authorisation) Echa.europa.eu. Retrieved on July 6, 2015.
- Watch Out For The Food We Consume. Directorate of Consumer Protection, Jakarta, Indonesia (2006). Дата обращения: 10 февраля 2009. Архивировано 28 декабря 2008 года.
Литература
- Альмединген А. Н. Бура, фальсификация её // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Герценштейн Г. М. Бура, в медицине // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Натрия тетраборат // Фотокинотехника: Энциклопедия / Гл. ред. Е. А. Иофис. — М.: Советская энциклопедия, 1981. — С. 204. — 447 с.
- Левинсон-Лессинг Ф. Ю. Бура, нахождение в природе // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Федоров П. И. Натрия бораты // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Большая Российская энциклопедия, 1992. — Т. 3: Меди—Полимерные. — С. 180—181. — 639 с. — 48 000 экз. — ISBN 5-85270-039-8.
