Метаборат натрия
Метаборат натрия — неорганическое вещество, соль щелочного металла натрия и метаборной кислоты с формулой NaBO2. Бесцветные кристаллы. Образует кристаллогидраты.
| Метаборат натрия | |
|---|---|
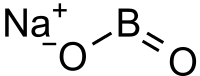 | |
| Общие | |
| Систематическое наименование |
Метаборат натрия |
| Традиционные названия | Метаборнокислый натрий |
| Хим. формула | NaBO2 |
| Физические свойства | |
| Состояние | Бесцветные кристаллы |
| Молярная масса | 65,80 г/моль |
| Плотность | 2,34; 2,462; 2,464 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 966 °C |
| • кипения | 1434 °C |
| Мол. теплоёмк. | 65,94 Дж/(моль·К) |
| Энтальпия | |
| • образования | -1059 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 16,40; 125,2100 г/100 мл |
| Классификация | |
| Рег. номер CAS | 98536-58-4 |
| PubChem | 145326 |
| Рег. номер EINECS | 231-891-6 |
| SMILES | |
| InChI | |
| RTECS | ED4640000 |
| ChEBI | 75227 |
| ChemSpider | 22899 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Торговые названия: Кодалк, Кодальк (США, Eastman Kodak).
Получение
- Сплавление бора с едким натром в присутствии кислорода:
- Сплавление тетрабората натрия с едким натром:
- Термическим разложением тетрагидроксобората натрия:
Физические свойства
Метаборат натрия образует бесцветные гигроскопические кристаллы тригональной сингонии, пространственная группа R 3c, параметры ячейки a = 1,1925 нм, c = 0,6439 нм, Z = 18. Известна метастабильная модификация с температурой плавления 934°С.
Хорошо растворим в воде, легко образует пересыщенные растворы.
При кристаллизации из водных растворов с небольшим избытком гидроксида натрия образует кристаллогидраты[1]:
- NaBO2•4H2O при температурах ниже 58 °С;
- NaBO2•2H2O при температурах 58—112 °C;
- NaBO2•½H2O при температурах выше 112°С и вплоть до температуры кипения насыщенного раствора — 120,2 °С;
- известны также кристаллогидраты NaBO2•H2O и Na3[B3O5(OH)2].
Гидрат NaBO2•½H2O можно обезводить путём нагрева до 306 °C[1].
Химические свойства
- Холодная вода переводит анион BO2- в тетрагидроксо форму:
- Разлагается в горячей воде:
- Разлагается кислотами:
Применение
- В производстве боросиликатных стекол.
- Как компонент гербицидов и антифризов.
В фотографии
В 1930-е годы фирма Kodak начала вводить метаборат натрия в состав проявителей под торговым именем кодалк вместо буры. Подобная замена позволяла более гибко регулировать щелочность при машинной обработке и помогает снизить образование пузырей в эмульсии при последующей обработке в кислых фиксажах. Рецепты, где бура была заменена кодалком содержали букву K в названии, идущую после буквы D (обозначавшую developer). Например, рецепт проявителя с бурой называется D-76, аналогичный рецепт с кодалком носит название DK-76. По щелочности метаборат натрия находится примерно между содой и бурой[2].
Примечания
- Федоров, 1992.
- Гурлев, 1988, с. 292.
Литература
- Гурлев Д. С. Справочник по фотографии (обработка фотоматериалов). — К.: Тэхника, 1988.
- Лидин Р. А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Федоров П. И. Натрия бораты // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Большая Российская энциклопедия, 1992. — Т. 3: Меди—Полимерные. — 639 с. — 48 000 экз. — ISBN 5-85270-039-8.
