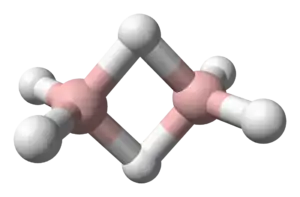
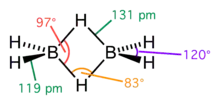Диборан
Диборан — бороводород, химическое соединение водорода и бора с формулой B2H6. Был впервые синтезирован в XIX веке. Представляет собой бесцветный газ с неприятным сладковатым запахом, слегка напоминающим сероводород. Сильно ядовит. При соприкосновении с воздухом может самопроизвольно воспламеняться.
| Диборан | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Диборан | ||
| Традиционные названия | Бороэтан | ||
| Хим. формула | B2H6 | ||
| Физические свойства | |||
| Состояние | газ | ||
| Примеси | Пентаборан | ||
| Молярная масса | 27,67 г/моль | ||
| Плотность | 0,447 (–112°C) | ||
| Энергия ионизации | 11,38 ± 0,01 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −165,5 °C | ||
| • кипения | −92,4 °C | ||
| Пределы взрываемости | 0,8 ± 0,1 об.%[1] | ||
| Мол. теплоёмк. | 298 К Дж/(моль·К) | ||
| Энтальпия | |||
| • образования | 36,4 кДж/моль | ||
| Давление пара | 39,5 ± 0,1 атм[1] | ||
| Классификация | |||
| Рег. номер CAS | 19287-45-7 | ||
| Рег. номер EINECS | 242-940-6 | ||
| SMILES | |||
| InChI | |||
| RTECS | HQ9275000 | ||
| ChEBI | 33590 | ||
| ChemSpider | 17215804 | ||
| Безопасность | |||
| ЛД50 |
40 мг/м3 (крыса, 4 часа) |
||
| Токсичность | очень ядовит | ||
| Пиктограммы СГС |
|
||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Получение
Существующие методы получения диборана основаны на взаимодействии галогенидов или алкоксидов бора с донорами гидрид-ионов.
В промышленности диборан получают путём восстановления BF3:
При получении диборана в лабораторных условиях восстанавливают фторид или хлорид бора:
Химические свойства
Диборан является сильной кислотой Льюиса, так как способен образовывать комплексы с основаниями (например, с аммиаком).
Диборан взаимодействует с водой. При этом выделяется водород и образуется борная кислота:
- .
Медленно вступает в реакцию с гидридом алюминия образуя (тетрагидридоборат алюминия), что позволяет запаковать его в кристаллы для получения водорода:
- ,
при 70 ℃ эти кристаллы разлагаются с образованием октадекабората (III) алюминия и выделением диборана.
На воздухе горит зелёным пламенем:
Сферы использования
Производные бороводородов применяются в качестве антиоксидантов, катализаторов окисления предельных и ароматических углеводородов в спирты и фенолы, добавки к смазочным маслам. Раньше (в СССР) диборан предлагался в качестве ракетного или самолётного топлива.
Физиологическое значение
Диборан (B2H6, Бороэтан) токсичен, числится в списке сильно действующих ядовитых веществ, относится к первому классу опасности и в высоких концентрациях обладает ярко выраженным удушающим действием. Также он может поражать центральную нервную систему.
ПДК диборана в воздухе рабочей зоны производственных помещений составляет 0,1 мг/м3 согласно ГОСТ 12.1.005-76.
Примечания
Ссылки
- Важнейшие соединения бора : [арх. 29 ноября 2019] // Кафедра общей и неорганической химии, Факультет естественных наук, Российский химико-технологический университет им. Д. И. Менделеева.