Пептидогликан
Пептидогликан (также известный как муреин) — гетерополимер N-ацетилглюкозамина и N-ацетилмурамовой кислоты, сшитый через лактатные остатки N-ацетилмурамовой кислоты короткими пептидными цепочками. Важнейший компонент клеточной стенки бактерий, выполняющий механические функции, осмотической защиты клетки, выполняет антигенные функции. Характерен только для бактерий (в клеточной стенке некоторых архей имеется аналог — псевдопептидогликан) и для глаукоцистофитовых водорослей (содержится в цианеллах). Аминокислотный состав пептидных цепочек является систематическим признаком.
Структура
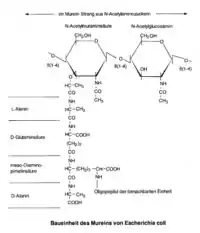
Пептидогликан образует упорядоченную структуру ячеистого строения, построенную из N-ацетилглюкозамина и N-ацетилмурамовой кислоты, соединенных β-1,4-гликозидными связями. Остатки N-ацетилмурамовой кислоты сшиты между собой при помощи коротких пептидов (сшивка производится ферментом транспептидазой). Типично пептидная цепочка содержит L-аланин, D-глутаминовую кислоту, мезо-диаминопимелиновую кислоту, L-лизин, D-аланин (следует отметить, что мезо-диаминопимелиновая кислота и D-аминокислоты в составе клеточных структур встречаются только в прокариотических клетках). Такая трёхмерная структура сообщает клеточной стенке бактерий прочность и защиту от осмотического лизиса.
Устойчивость пептидогликана
Пептидогликан характерен только для клеточной стенки бактериальных клеток и поэтому является мишенью для многих антибактериальных средств. Фермент лизоцим атакует β-1,4-гликозидные связи между остатками N-ацетилглюкозамина и N-ацетилмурамовой кислоты, вызывая гидролиз пептидогликана и лизис бактериальной клетки (См. Лизоцим). Муроэндопептидазы разрушают пептидные цепочки, сшивающие нити полимера. β- лактамные антибиотики (напр., пенициллин, цефалоспорин) нарушают синтез пептидогликана, связываясь с транспептидазой. D- циклосерин нарушает синтез D-аланина из L-аланина, тем самым нарушая синтез пептидных цепочек. Механизм защиты от антибиотиков может заключаться в мутации в гене транспептидазы (изменяя сродство пенициллина к транспептидазе), синтез β-лактамаз (расщепляют β-лактамное кольцо антибиотика), мутации, изменяющие проницаемость мембраны для D- циклосерина[1].