Циклогексилхлорид
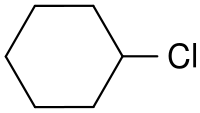
Циклогекси́лхлори́д (также хлòрциклогекса́н, циклогекси́л хло́ристый) — алициклическое хлорорганическое соединение с формулой (CH2)5CHCl, бесцветная жидкость. В природе практически не встречается.
| Циклогексилхлорид | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Cyclohexyl chloride, chlorocyclohexane |
| Традиционные названия | монохлорциклогексан, циклогексил хлористый |
| Хим. формула | C6H11Cl |
| Рац. формула | (CH2)5CHCl |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 118,604 г/моль |
| Плотность | 0,973[1] |
| Термические свойства | |
| Температура | |
| • плавления | −44 °C[2] |
| • кипения | 142,6 °C |
| • вспышки | 32 °C |
| Энтальпия | |
| • плавления | 2,043 кДж/моль |
| Удельная теплота испарения | 233500 Дж/кг |
| Химические свойства | |
| Растворимость | |
| • в воде | 0.002 (20°C) |
| Оптические свойства | |
| Показатель преломления | 1,4626 (20°C) |
| Классификация | |
| Рег. номер CAS | 542-18-7 |
| PubChem | 10952 |
| Рег. номер EINECS | 208-806-6 |
| SMILES | |
| InChI | |
| ChEBI | 39156 |
| ChemSpider | 10487 |
| Безопасность | |
| Предельная концентрация | 50 мг/м³ |
| ЛД50 | 1500 мг/кг |
| Краткие характер. опасности (H) | H302 |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Физические свойства
Циклогексилхлорид — бесцветная легковоспламеняющаяся жидкость с резким запахом. Мало растворим в воде, легко — в хлороформе, смешивается с ацетоном, бензолом, этанолом и диэтиловым эфиром.
Химические свойства
При кипячении со щёлочью образует циклогексен[1].
Получение
Циклогексилхлорид может быть получен с выходом 70 % из циклогексана галогенированием его пентахлоридом фосфора в безводном растворе 1,2-дихлорбензола при температуре около 80 ° С с перекисью бензоила в качестве катализатора[3]:
C6H12 + PCl5 → C6H11Cl
Другой способ — галогенирование циклогексана сульфурилхлоридом при нагревании в безводном растворителе, с азобисизобутиронитрилом в качестве катализатора[4]:
C6H12 + SO2Cl2 → C6H11Cl + SO2 + HCl
Также может быть получен нагреванием циклогексанола с концентрированной соляной кислотой[1].
Стереоизомерия
Стереоизомеры хлорциклогексана рассматриваются в рамках концепции остаточной стереоизомерии. Хлорциклогексан имеет два стереоизомера с аксиальным и экваториальным положением атома хлора, которые различаются при анализе ИК-спектроскопией или ЯМР-спектроскопией при −100 °С. При выделении же или анализе ЯМР при комнатной температуре хлорциклогексан является одним соединением, не имея стереоизомеров в обычном понимании[5].
Основные сферы применения
- Растворитель (жиров, смол, и др.).
- Экстрагент в химической промышленности.
- В органическом синтезе — например, для получения циклогексена[1].
- Является побочным продуктом в производстве капролактама[1].
- Сырьё для получения ядохимикатов.
Токсичность
Острое отравление у животных проявляется при вдыхании паров циклогексилхлорида — возбужденное состояние, раздражение слизистых, дрожание, боковое положение, затрудненное дыхание, тонические судороги и смерть. Для белых мышей при вдыхании в течение двух часов 100 % летальная концентрация ЛК100=78 мг/л, для белых крыс — 40-75 мг/л. При хроническом отравлении у крыс (ежедневное вдыхание 0,5 мг/л по 5 часов в сутки) — через месяц снижение артериального давления, через 4-5 месяцев функциональные сдвиги в ЦНС, снижение числа лейкоцитов. Введение циклогексилхлорида с питьевой водой в течение 6 месяцев в количестве 0,025-25 мг/кг не оказывало заметного влияния на крыс и кроликов. Повторное нанесение жидкого циклогексилхлорида на кожу мышей вызывало сухой некроз[1].
Рекомендуемая ПДК в воздухе рабочей зоны — 50 мг/м³, в воде — 0,05 мг/л[1].
Примечания
- Вредные вещества в промышленности. том I, 1976, с. 250.
- Bradley J., Williams A., Andrew S.I.D. Lang Jean-Claude Bradley Open Melting Point Dataset // Figshare — 2014. — doi:10.6084/M9.FIGSHARE.1031637.V2
- Daniel Bellus, Manfred Braun, Tonia Freysoldt и др. Science of Synthesis: Houben-Weyl Methods of Molecular Transformations (англ.), с. 28
- Preparation and characterisation of Chlorocyclohexane (англ.)
- Илиел и др., 2007, с. 44.
Источники
- Илиел Э., Вайлен С., Дойл М. Основы органической стереохимии = Basic Organic Stereochemistry / Пер. с англ. З. А. Бредихиной, под ред. А. А. Бредихина. — М.: Бином. Лаборатория знаний, 2007. — 703 с. — ISBN 978-5-94774-370-8.
- Лазарев Н. В.. Вредные вещества в промышленности. том I. — Л.: Химия, 1976. — 592 с.
- Хлорциклогексан на Acetyl.ru
- Хлорциклогексан на Himreakt.ru

