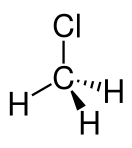
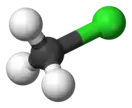
Хлорметан
Хлормета́н (монохлормета́н, метилхлори́д, хло́ристый мети́л) — органическое вещество, принадлежащее к группе галогеналканов. Впервые был получен французскими химиками Жаном Батистом Дюма и Эженом Пелиго в 1835 году кипячением смеси метанола, серной кислоты и хлорида натрия. Аналогичный способ используется и в наши дни. Хлорметан — бесцветный легколетучий ядовитый газ со сладковатым запахом. Из-за слабого запаха можно легко не заметить токсичной или взрывоопасной концентрации.
| Хлорметан | |||
|---|---|---|---|
 | |||
| Общие | |||
| Систематическое наименование |
Хлорметан | ||
| Традиционные названия | монохлорметан, метилхлорид, фреон 40, R 40, UN 1063 | ||
| Хим. формула | CH3Cl | ||
| Физические свойства | |||
| Состояние | газ | ||
| Молярная масса | 50,4877 г/моль | ||
| Плотность | 0,915 г/см³ | ||
| Энергия ионизации | 11,28 ± 0,01 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −97,7 °C | ||
| • кипения | −24,2 °C | ||
| • вспышки | −46 °C | ||
| • самовоспламенения | 625 °C | ||
| Пределы взрываемости | 8,1 ± 0,1 об.%[1] | ||
| Удельная теплота испарения | 423850 Дж/кг | ||
| Давление пара | 490 kPa | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 5,325 г/100 мл | ||
| Структура | |||
| Гибридизация | тетраэдр | ||
| Классификация | |||
| Рег. номер CAS | 74-87-3 | ||
| PubChem | 6327 | ||
| Рег. номер EINECS | 200-817-4 | ||
| SMILES | |||
| InChI | |||
| RTECS | PA6300000 | ||
| ChEBI | 36014 | ||
| Номер ООН | 1063 | ||
| ChemSpider | 6087 | ||
| Безопасность | |||
| Предельная концентрация | 10 мг/м³ | ||
| Токсичность | ядовит, огнеопасен, канцероген | ||
| Пиктограммы СГС |
|
||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
История
Впервые он был сделан в 1835 году французскими химиками Жан-Батистом Дюма и Эженом Пелиго. Они получали хлорметан, используя метод, аналогичный сегодняшнему методу, то есть нагревая смесь метанола, серной кислоты и хлорида натрия.
Производство
Большая часть хлорметана получается реакцией метанола с хлороводородом, согласно следующей химической реакции:
Это может быть осуществлено пропусканием хлороводорода через кипящий метанол вместе с хлоридом цинка в качестве катализатора или пропусканием смеси метанола и хлороводорода через окись алюминия при 350 °C.
Меньшие количества хлорметана производят нагреванием смеси метана и хлора до 400 °C. Однако этот метод дает смесь с более хлорированными производными метана (дихлорметан, хлороформ, тетрахлорметан) и используется тогда, когда необходимы эти вещества.
Применение
Хлорметан был широкоприменяемым хладагентом. Данное его применение прекратили из-за токсичности и пожароопасности. Хлорметан был использован для производства добавок к бензину на основе свинца (тетраметилсвинец).
Наиболее важное использование хлорметана сейчас в качестве химического полупродукта в производстве силиконовых полимеров. Меньшие количества используют в качестве растворителя при производстве бутилкаучука и очистке бензина.
Хлорметан используют как метилирующий или хлорирующий агент в органической химии. Он находит также множество различных применений: удаления жирных загрязнений, следов смол, как ракетное топливо, для получения пенополистирола. Как локальное обезболивающее, как промежуточный продукт при синтезе лекарств, как носитель в низкотемпературной полимеризации, как жидкость для термометрического и термостатического оборудования, в качестве гербицида.
Безопасность
Вдыхание газообразного хлорметана оказывает токсическое действие на центральную нервную систему. У пострадавшего возникает сонливость, головокружение, рассеянность, нарушение координации движений, спутанность речи, нарушение дыхания, удушье. При больших концентрациях наступают судороги, параличи и кома.
В случае проглатывания может возникнуть тошнота и рвота. Контакт сжиженного метилхлорида с кожей приводит к обморожению. Контакт с глазами может привести к ухудшению зрения.
Хроническое воздействие хлорметана вызывает тератогенный эффект.