Органическая химия
Органи́ческая хи́мия — раздел химии, изучающий структуру, свойства и методы синтеза соединений углерода с другими химическими элементами, относящихся к органическим соединениям.[1] [2] Первоначальное значение термина органическая химия подразумевало изучение только соединений углерода растительного и животного происхождения. По этой причине ряд углеродсодержащих соединений традиционно не относят к органическим (например, монооксид углерода, диоксид углерода, циановодород, сероуглерод, карбонилы металлов), а рассматривают как неорганические соединения. Условно можно считать, что структурным прототипом органических соединений являются углеводороды.[2]
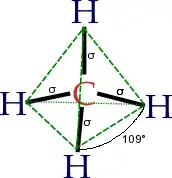
Наибольшее количество соединений углерод образует с так называемыми элементами-органогенами: H, N, O, S, P[3]. Способность углерода соединяться с большинством элементов и образовывать молекулы различного состава и строения обусловливает многообразие органических соединений. Органические соединения играют ключевую роль в существовании живых организмов (например, нуклеотиды, природные аминокислоты, углеводы).
Предмет органической химии включает следующие цели, экспериментальные методы и теоретические представления:
- Выделение индивидуальных веществ из растительного, животного или ископаемого сырья
- Синтез и очистка соединений
- Определение структуры веществ
- Изучение механизмов химических реакций
- Выявление зависимостей между структурой органических веществ и их свойствами
Количество известных органических соединений
24 мая 1999 года число известных химических соединений превышало 25 млн., из них 12 млн были органическими[4], ко 2 мая 2014 года общее число известных неорганических и органических соединений превысило 87 млн[5]. На 8 апреля 2018 года в реестре Химической реферативной службы США (CAS) зарегистрирован 141 млн. химических веществ .
История
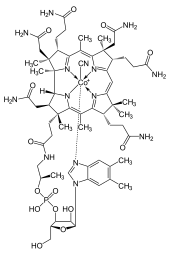
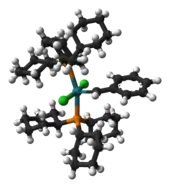
Способы получения различных органических веществ были известны ещё с древности. Египтяне и римляне использовали красители индиго и ализарин, содержащиеся в растительных веществах. Многие народы знали секреты производства спиртных напитков и уксуса из сахара и крахмалсодержащего сырья.
Во времена Cредневековья к этим знаниям ничего не прибавилось, некоторый прогресс начался только в XVI—XVII вв.: были получены некоторые вещества, в основном путём перегонки определённых растительных продуктов. Большое экономическое значение имело обнаружение Маргграфом сахара в свёкле[7]:6 (вдобавок к известному в то время его источнику — сахарному тростнику), о чём он сообщил в статье «Химические попытки извлекать настоящий сахар из растений нашей страны» в 1747 году[8]. В 1769—1785 г. Шееле выделил несколько органических кислот, среди них яблочная, винная, лимонная, галловая, молочная и щавелевая. В 1773 г. Руэль выделил из человеческой мочи мочевину.
Выделенные из животного или растительного сырья продукты имели между собой много общего, но отличались от неорганических соединений. При этом полагали, что эти вещества могут быть получены только в живых организмах благодаря «жизненной силе». Так, в 1753 году известный шведский естествоиспытатель Валлериус в предисловии к сборнику работ другого видного шведского учёного, Йерне, утверждал[9]: «…ни животные, ни растительные тела, ни их части не могут быть воспроизведены поэтому химическим искусством»[7]:7. В первом томе своей книги «Лекции по животной химии» («Föreläsningar i Djurkemien»), вышедшем в 1828 году Й. Я. Берцелиус впервые вводит понятие «органическая химия» (швед. organisk Kemi), определяя её как «часть физиологии, которая описывает состав живых тел вместе с химическими процессами, происходящими в них»[10].
Представление о «жизненной силе» было поколеблено синтезом образующихся в живых организмах веществ из неорганических, проведённым в первой половине XIX века[7]:15-16, например, в 1828 году Фридрих Вёлер во второй раз получил органическое вещество — мочевину — в результате упаривания водного раствора цианата аммония (NH4OCN). До этого, в 1824 году, он впервые получил щавелевую кислоту.
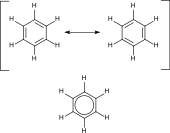
Важным этапом стала разработка теории валентности Купером и Кекуле в 1857 г., а также теории химического строения Бутлеровым в 1861 г. В основу этих теорий были положены четырёхвалентность углерода и его способность к образованию цепей. В первом томе своего труда по органической химии, вышедшем в 1859 году, Кекуле впервые вводит близкое к современному определение понятия «органическая химия» — это «химия соединений углерода»[11], что отражено уже в самом названии этого труда, которое переводится как «Учебник органической химии, или химии углеродистых соединений». В 1850-х годах профессор Московского университета Н. Э. Лясковский, по словам Н. М. Сарандинаки, говорил: «Органическая химия не есть химия веществ, встречаемых в организмах, а химия соединений углерода», что впоследствии сделалось господствующим в науке воззрением[12]. В 1865 году Кекуле предложил структурную формулу бензола, что стало одним из важнейших открытий в органической химии. В 1875 г. Вант-Гофф и Ле Бель предложили тетраэдрическую модель атома углерода, по которой валентности углерода направлены к вершинам тетраэдра, если атом углерода поместить в центр этого тетраэдра. В 1917 году Льюис предложил рассматривать химическую связь с помощью электронных пар.
В 1931 г. Хюккель применил квантовую теорию для объяснения свойств альтернативных ароматических углеродов, чем основал новое направление в органической химии — квантовую химию. В 1933 г. Ингольд провёл изучение кинетики реакции замещения у насыщенного атома углерода, что привело к масштабному изучению кинетики большинства типов органических реакций.
Историю органической химии принято излагать в связи с открытиями, сделанными в области строения органических соединений, однако такое изложение больше связано с историей химии вообще. Гораздо интереснее рассматривать историю органической химии с позиции материальной базы, то есть собственно предмета изучения органической химии.
На заре органической химии предметом изучения были преимущественно субстанции биологического происхождения. Именно этому факту органическая химия обязана своим названием. Научно-технический прогресс не стоял на месте, и со временем основной материальной базой органической химии стала каменноугольная смола, выделяемая при получении кокса прокаливанием каменного угля. Именно на основе переработки каменноугольной смолы в конце XIX века возник основной органический синтез. В 50-60 годах прошлого века произошёл переход основного органического синтеза на новую базу — нефть. Таким образом появилась новая область химии — нефтехимия. Огромный потенциал, который был заложен в новом сырье, вызвал бум в органической химии и химии вообще. Появление и интенсивное развитие такой области, как химия полимеров, связано прежде всего с новой сырьевой базой.
Несмотря на то, что современная органическая химия в качестве материальной базы по-прежнему использует сырьё биологического происхождения и каменноугольную смолу, объём переработки этих видов химического сырья по сравнению с переработкой нефти мал. Смена материально-сырьевой базы органической химии была вызвана прежде всего возможностями наращивания объёмов производства.
Классификация органических соединений
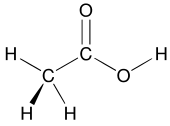
Правила и особенности классификации
В основе классификации лежит структура органических соединений. Основа описания структуры — структурная формула. Атомы элементов обозначаются латинскими символами, как они обозначены в периодической таблице химических элементов (таблице Менделеева). Водородные и электронодефицитные связи обозначаются пунктирной линией, ионные связи обозначаются указанием зарядов частиц, входящих в состав молекулы. Поскольку в подавляющее большинство органических молекул входит водород, его обычно не обозначают при изображении структуры. Таким образом, если в структуре у одного из атомов изображена недостаточная валентность, значит, возле этого атома расположен один или несколько атомов водорода.
Атомы могут образовывать циклические и ароматические системы.
Основные классы органических соединений
- Углеводороды — химические соединения, состоящие только из атомов углерода и водорода. В зависимости от топологии строения углеродного скелета углеводороды подразделяют на ациклические и карбоциклические. В зависимости от кратности углерод-углеродных связей углеводороды подразделяют на предельные (алка́ны или насыщенные), не содержащие кратные связи в своей структуре и непредельные или ненасыщенные — имеют в своём составе хотя бы одну двойную и/или тройную связь (алкены, алкины, диены). В свою очередь циклические углеводороды разделяют на алициклические (с открытой цепью) и циклоалканы (предельные с замкнутой цепью), ароматические углеводороды (непредельные, содержащие цикл).
| Ациклические (с открытой цепью) | Карбоциклические (с замкнутой цепью) | ||||
|---|---|---|---|---|---|
| предельные | непредельные | предельные | непредельные | ||
| с одинарной связью | с двойной связью | с тройной связью | с двумя двойными связями | с одинарной связью | с бензольным кольцом |
| ряд метана (алканы) | ряд этилена (алкены) | ряд ацетилена (алкины) | ряд диеновых углеводородов | ряд полиметиленов (нафтены) | ряд бензола (ароматические углеводороды, или арены) |
- Соединения с гетероатомами в функциональных группах — соединения, в которых углеродный радикал R связан с функциональной группой. По характеру функциональных групп делятся на:
- Галогенсодержащие
- Спирты, фенолы. Спирты́ (устар. алкого́ли, англ. alcohols; от лат. spiritus — дух) — органические соединения, содержащие одну или более гидроксильных групп (гидроксил, −OH), непосредственно связанных с насыщенным (находящемся в состоянии sp³ гибридизации) атомом углерода[13]. Спирты можно рассматривать как производные воды (H−O−H), в которых один атом водорода замещён на органическую функциональную группу: R−O−H. В номенклатуре IUPAC для соединений, в которых гидроксильная группа связана с ненасыщенным (находящемся в состоянии sp2 гибридизации атомом углерода, рекомендуются названия «енолы» (гидроксил связан с винильной C=C связью)[14] и «фенолы» (гидроксил связан с бензольным или другим ароматическим циклом)[15].
- Простые эфиры (этеры) — органические вещества, имеющие формулу R-O-R1, где R и R1 — углеводородные радикалы. Необходимо учитывать, что такая группа может входить в состав других функциональных групп соединений, не являющихся простыми эфирами (например, Кислородсодержащие органические соединения).
- Сложные эфиры (эстеры) — производные оксокислот (как карбоновых так и минеральных) RkE(=O)l(OH)m, (l ≠ 0), формально являющиеся продуктами замещения атомов водорода гидроксилов —OH кислотной функции на углеводородный остаток (алифатический, алкенильный, ароматический или гетероароматический); рассматриваются также как ацилпроизводные спиртов. В номенклатуре IUPAC к сложным эфирам относят также ацилпроизводные халькогенидных аналогов спиртов (тиолов, селенолов и теллуролов)[16]. Отличаются от простых эфиров, в которых два углеводородных радикала соединены атомом кислорода (R1—O—R2).
- Соединения, содержащие карбонильную группу
- Альдегиды (от лат. alcohol dehydrogenatum — спирт, лишённый водорода) — класс органических соединений, содержащих карбонильную группу (С=О) с одним алкильным или арильным заместителем.
- Кетоны — это органические вещества, в молекулах которых карбонильная группа связана с двумя углеводородными радикалами. Общая формула кетонов: R1-CO-R2. Наличие в кетонах именно двух атомов углерода, непосредственно связанных с карбонильной группой, отличает их от карбоновых кислот и их производных, а также альдегидов.
- Хиноны — полностью сопряжённые циклогексадиеноны и их аннулированные аналоги. Существуют два класса хинонов: пара-хиноны с пара-расположением карбонильных групп (1,4-хиноны) и орто-хиноны с орто-расположением карбонильных групп (1,2-хиноны). Благодаря способности к обратимому восстановлению до двухатомных фенолов некоторые производные пара-хинонов участвует в процессах биологического окисления в качестве коферментов ряда оксидоредуктаз.
 Доска для плавания изготовлена из полистирола — одного из полимеров.
Доска для плавания изготовлена из полистирола — одного из полимеров.
- Соединения, содержащие карбоксильную группу (карбоновые кислоты, сложные эфиры)
- Серосодержащие соединения
- Азотсодержащие соединения
- Металлоорганические соединения
- Гетероциклические — содержат гетероатомы в составе кольца. Различаются по числу атомов в цикле, по виду гетероатома, по количеству гетероатомов в цикле.
- Органического происхождения — как правило, соединения очень сложной структуры, зачастую принадлежат сразу к нескольким классам органических веществ, часто полимеры. Из-за этого их сложно классифицировать и их выделяют в отдельный класс веществ.
- Полимеры — вещества очень большой молекулярной массы, которые состоят из периодически повторяющихся фрагментов — мономерных звеньев.
Строение органических молекул
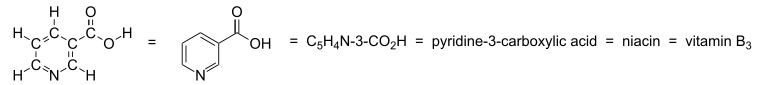
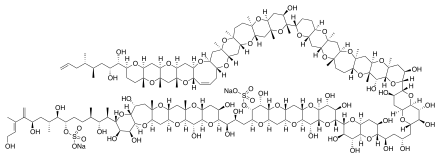
Органические молекулы в основном образованы ковалентными неполярными связями C—C, или ковалентными полярными типа C—O, C—N, C—Hal. Согласно октетной теории Льюиса и Косселя молекула является устойчивой, если внешние орбитали всех атомов полностью заполнены. Для таких элементов как C, N, O, Галогены необходимо 8 электронов, чтобы заполнить внешние валентные орбитали, для водорода необходимо только 2 электрона. Полярность объясняется смещением электронной плотности в сторону более электроотрицательного атома.
Классическая теория валентных связей не в состоянии объяснить все типы связей, существующие в органических соединениях, поэтому современная теория использует методы молекулярных орбиталей и квантово-химические методы.
Строение органического вещества
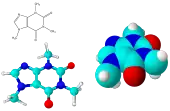
Свойства органических веществ определяются не только строением их молекул, но и числом и характером их взаимодействий с соседними молекулами, а также взаимным пространственным расположением. Наиболее ярко эти факторы проявляются в различии свойств веществ, находящихся в разных агрегатных состояниях. Так, вещества, легко взаимодействующие в виде газа, могут совершенно не реагировать в твёрдом состоянии, или приводить к другим продуктам.
В твёрдых органических веществах, в которых наиболее ярко проявляются эти факторы, различают органические кристаллы и аморфные тела. Их описанием занимается наука «химия органического твёрдого тела», основание которой связывают с именем советского физика-кристаллографа А. И. Китайгородского. Примеры полезных органических твёрдых тел — органические люминофоры, разнообразные полимеры, сенсоры, катализаторы, электропроводки, магниты и др.
Особенности органических реакций
В неорганических реакциях обычно участвуют ионы, они проходят быстро и до конца при комнатной температуре. В органических реакциях часто происходят разрывы ковалентных связей с образованием новых. Как правило, эти процессы требуют особых условий: определённой температуры, времени реакции, и часто наличия катализатора. Обычно протекает не одна, а сразу несколько реакций, поэтому выход целевого вещества зачастую не превышает 50 %. Поэтому при изображении органических реакций используют не уравнения, а схемы без расчёта стехиометрии.
Реакции могут протекать очень сложным образом и в несколько стадий, не обязательно так, как реакция условно изображена на схеме. В качестве промежуточных соединений могут возникать карбкатионы R+, карбанионы R−, радикалы R·, карбены CX2, катион-радикалы, анион-радикалы, и другие активные или нестабильные частицы, обычно живущие доли секунды. Подробное описание всех превращений, происходящих на молекулярном уровне во время реакции, называется механизмом реакции.
Реакции классифицируются в зависимости от способов разрыва и образования связей, способов возбуждения реакции, её молекулярности.
Определение структуры органических соединений
За все время существования органической химии как науки важной задачей было определить структуру органических соединений. Это значит узнать, какие атомы входят в состав соединения, в каком порядке эти атомы связаны между собой и как расположены в пространстве.
Существует несколько методов решения этих задач.
- Элементный анализ. Заключается в том, что вещество разлагается на более простые молекулы, по количеству которых можно определить количество атомов, входящее в состав соединения. С помощью этого метода невозможно установить порядок связей между атомами. Часто используется лишь для подтверждения предположенной структуры.
- Инфракрасная спектроскопия и спектроскопия комбинационного рассеяния (ИК-спектроскопия и КР-спектроскопия). Вещество взаимодействует с электромагнитным излучением (светом) инфракрасного диапазона (в ИК-спектроскопии наблюдают поглощение, в КР-спектроскопии — рассеяние излучения). Этот свет при поглощении возбуждает колебательные и вращательные уровни молекул. Опорными данными являются число, частота и интенсивность колебаний молекулы, связанных с изменением дипольного момента (ИК-спектроскопия) или поляризуемости (КР-спектроскопия). Методы позволяют установить наличие определённых функциональных групп в молекуле. Часто используются и для того чтобы подтвердить идентичность исследуемого вещества с некоторым уже известным веществом путём сравнения спектров.
- Масс-спектроскопия. Вещество при определённых условиях (электронный удар, химическая ионизация и др.) превращают в ионы без потери атомов (молекулярные ионы) и с потерей (осколочные). Позволяет определить молекулярный вес и иногда позволяет установить наличие различных функциональных групп.
- Метод ядерного магнитного резонанса (ЯМР). Основан на взаимодействии ядер, обладающих собственным магнитным моментом (спином) и помещённых во внешнее постоянное магнитное поле, с электромагнитным излучением радиочастотного диапазона. Один из главных методов, который может быть использован для определения химической структуры. Метод используют также для изучения пространственного строения молекул, динамики молекул. В зависимости от ядер, взаимодействующих с излучением различают, например:
- Метод протонного магнитного резонанса (ПМР). Позволяет определить положение атомов водорода 1H в молекуле.
- Метод ЯМР 19F. Позволяет определить наличие и положение атомов фтора в молекуле.
- Метод ЯМР 31P. Позволяет определить наличие, положение и валентное состояние атомов фосфора в молекуле.
- Метод ЯМР 13С. Позволяет определить число и типы атомов углерода в молекуле. Используется для исследования формы углеродного скелета молекулы.
В отличие от первых трёх в последнем методе используется неосновной изотоп элемента, поскольку ядро основного изотопа углерода — 12С имеет нулевой спин и не может наблюдаться методом ядерного магнитного резонанса, так же как и ядро 16O — самого распространённого в природе изотопа кислорода.
- Метод ультрафиолетовой спектроскопии (УФ-спектроскопия) или Спектроскопия электронных переходов. Метод основан на поглощении электромагнитного излучения ультрафиолетовой и видимой области спектра при переходе электронов в молекуле с верхних заполненных уровней на вакантные уровни (возбуждение молекулы). Чаще всего используется для определения наличия и характеристик конъюгированных π-систем.
- Методы аналитической химии. Позволяют определить наличие некоторых функциональных групп по специфическим химическим реакциям, факт протекания которых можно фиксировать визуально или с помощью других методов.
- Рентгеноструктурный анализ.
Примечания
- Органическая химия Архивная копия от 28 сентября 2015 на Wayback Machine. БСЭ.
- Органическая химия // Химическая энциклопедия : [рус.] : в 5 т. / под ред. И. Л. Кнунянца. — М. : Большая Российская энциклопедия, 1992. — Т. 3. — С. 396–399. — 639 с. — ISBN 5-85270-039-8.
- Предмет органической химии. Исторический обзор // Начала органической химии. — М.: Химия, 1970. — Т. 1. — С. 11—26. — 664 с. — 19 000 экз.
- Greenberg A. From Alchemy to Chemistry in Picture and Story (англ.). — John Wiley & Sons, 2006. — P. 422.
- American Chemical Society. CAS REGISTRY and CAS Registry Number FAQs (англ.). Дата обращения: 2 мая 2014.
- Torker, Sebastian; MüLler, Andre; Sigrist, Raphael; Chen, Peter (2010). “Tuning the Steric Properties of a Metathesis Catalyst for Copolymerization of Norbornene and Cyclooctene toward Complete Alternation”. Organometallics. 29 (12): 2735—2751. DOI:10.1021/om100185g.
- Быков Г.В. Возникновение органической химии как науки // Книга для чтения по органической химии. Пособие для учащихся. — М.: Просвещение, 1975. — С. 5—19.
- Marggraf A. Experiences chimiques faites dans le dessein de tirer un veritable sucre de diverses plantes, qui croissent dans nos contrées (фр.) // Histoire de l'académie royale des sciences et belles-lettres de Berlin. Année MDCCXLVII : magazine. — 1749. — P. 79—90.
- Urbani Hierne. Tentaminum Chemicorum in Reg. Laboratorio Holmiensi peractorum, tomus secundus, nunc primûm in lucem editorum cum annotationibus Joh. Gotschalk Wallerii. Praefatio (неопр.). — Stockholmiae, 1753. — С. VIII.
- Berzelius J.J. Föreläsningar i Djurkemien (неопр.). — Stockholm, 1806. — Т. 1. — С. 6.
- Издание 1861 года доступно в интернете, см. в нём: Kekulé A. Lehrbuch der organischen Chemie oder der Chemie der Kohlenstoffverbindungen (нем.). — 1861. — Bd. 1. — S. 11.
- В. Н. Лясковский. Николай Эрастович Лясковский (неопр.). — М.: Университетская типография (М. Катков), 1884. — С. 40.
- Alcohols (англ.). IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). doi:10.1351/goldbook.A00204. Дата обращения: 2 сентября 2010. Архивировано 21 августа 2011 года.
- Enols (англ.). IUPAC. Compendium of Chemical Terminology, 2nd ed. (the «Gold Book»). doi:10.1351/goldbook.E02124. Дата обращения: 2 сентября 2010. Архивировано 21 августа 2011 года.
- Phenols (англ.). IUPAC. Compendium of Chemical Terminology, 2nd ed. (the «Gold Book»). doi:10.1351/goldbook.P04539. Дата обращения: 2 сентября 2010. Архивировано 21 августа 2011 года.
- esters // IUPAG Gold Book
Литература
- Быков Г. В. История органической химии. М.: Химия, 1976. 360 с.
- Гауптман З., Грефе Ю., Ремане Х., «Органическая химия». Москва, «Химия», 1979.
- Марч Дж., «Органическая химия: реакции, механизмы и структура», в 4-х томах. Москва, «Мир», 1987.
- Кери Ф., Сандберг Р., «Углубленный курс органической химии», в 2-х томах. Москва, «Химия», 1981.
- Реутов О. А., Курц А. Л., Бутин К. П. «Органическая химия», в 4-х частях. Москва, Изд-во МГУ, «БИНОМ. Лаборатория знаний», 1999—2004. http://edu.prometey.org/library/autor/7883.html
- Травень В. Ф. «Органическая химия», в 2-х томах. Москва, ИКЦ «Академкнига», 2004.
- Химическая энциклопедия, п. ред. Кнунянц, т. 3. Москва, «Большая Российская Энциклопедия», 1992.
- Робертс Дж., Касерио М. , «Основы органической химии». Изд. 2, в 2-х томах. Москва, «Мир», 1978.
- Моррисон Р., Бойд Р., «Органическая химия». Москва, «Мир», 1974.
- Clayden J., Greeves N., Warren S., Wothers P. Organic Chemistry. — Oxford University Press, 2012.
