Механизм реакции
Механизм реакции — это детальное описание процесса превращения реагентов в продукты, включающее в себя как можно более полное описание состава, строения, геометрии, энергии и других свойств интермедиатов, переходных состояний и продуктов. Часто в описание механизма включают обозначения, касающиеся движения электронов в частицах, которыми сопровождается переход от продуктов к реагентам. Приемлемый механизм реакции должен согласоваться с экспериментальными данными, например, стереохимией реакции, её стехиометрией, кинетическим уравнением и т. п. Речь идёт о приемлемом механизме, поскольку нередки случаи, когда полученным данным удовлетворяет несколько возможных механизмов. Для большинства реакций неизвестен весь набор данных, необходимых для точного установления механизма, и предлагаемые механизмы основываются на неполных данных[1]. По этой причине можно либо предложить, либо опровергнуть ранее предложенный механизм реакции. Утверждение о доказанности механизма реакции представляется некорректным.
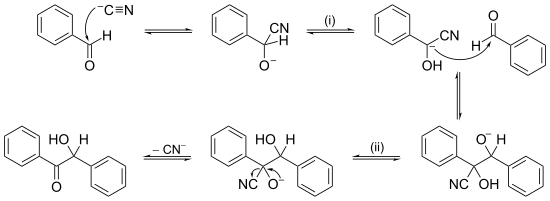
Классификация механизмов
В соответствии с правилами отбора по спину выделяют спин-запрещенный и спин-разрешенный механизмы реакции. Механизм реакции является спин-запрещенным, если какая-либо из элементарных стадий реакции протекает с изменением спинового состояния реагирующих частиц относительно продуктов или интермедиатов. В случае сохранения спинового состояния вовлеченных частиц на протяжении всей реакции, механизм относят к спин-разрешенному. Стоит отметить, что термин "спин-запрещенный" не является абсолютным и учёт спин-орбитального, спин-спинового и др. взаимодействий при описании механизма реакции снимает запрет на консервацию спина. Указанные механизмы могут конкурировать между собой, приводя к различным продуктам реакции[2]. Вероятность спин-запрещенного шага всегда меньше единицы и в этом смысле он проигрывает спин-разрешенному[3]. Однако, конечная кинетика и термодинамика реакции зависят не только от вероятности перехода в критической точке, но и от величины барьера, который необходимо преодолеть. Спин-запрещенный механизм был предложен для описания различных реакций, в том числе в области неорганической[4], бионеорганической[5] и металлоорганической химии[6]. Ярким примером спин-запрещенного процесса выступает интеркомбинационная конверсия, в то время как примером спин-разрешенного процесса служит внутренняя конверсия.
Обозначения механизмов
В настоящее время для обозначения механизмов реакции наиболее часто используются обозначения, предложенные Кристофером Ингольдом в книге «Structure and Mechanism in Organic Chemistry». Ингольд разделил механизмы на несколько основных типов и некоторые из них обозначил определённым сокращением: присоединение (A/Ad), отщепление (E), замещение (S), перегруппировки и т. д. Согласно этой системе, реакции также относились к разным группам по природе стадии образования или разрушения связи. Так, выделяли нуклеофильные, электрофильные и радикальные реакции. Они обозначались символами N, E и R соответственно, которые помещались в виде подстрочного индекса после обозначения типа реакции. Например, реакции электрофильного присоединения обозначали сокращением AE или AdE[7].
В 1988 ИЮПАК предложил новую систему обозначений для механизмов. Она основана на описании базовых актов создания и разрыва связей. Эти акты обозначаются соответственно как A и D и записываются слитно, если процесс представляет собой согласованное присоединение — отщепление либо разделяются знаком «+», если эти два акта происходят как отдельные стадии реакции. Для промежуточных ситуаций, когда интермедиат живёт очень короткое время (меньше времени диффузии), но дольше, чем происходит колебательное движение в молекуле, вместо знака «+» используется знак «*»[8].
Вместе с символами A и D используются нижние индексы N и E, если в реакции участвуют нуклеофильные/нуклеофугные или электрофильные/электрофугные группы. Индекс R применяется для гомолитических (радикальных) простейших изменений в молекуле. Аналогичные индексы, записываемые строчными буквами, употребляются в тех случаях, когда элементарный акт происходит у так называемых периферических атомов, то есть атомов, не составляющих непосредственно образуемую или разрываемую связь А–В. Подобным образом правила применяются и для циклических систем и других более сложных случаев. Поскольку данный подход подразумевает запись каждого разрыва и каждого образования связи, то традиционные обозначения механизмов (по Ингольду) здесь приобрели достаточно громоздкий вид[8].
| Ингольд | ИЮПАК |
|---|---|
| SN2 | ANDN |
| SN1 | DN + AN |
| SE1 | DE + AE |
| E1 | DN + DH (или DN + DE) |
| E2 | AxhDHDN |
| E1cB | AnDE + DN (или AxhDH + DN) |
Сам ИЮПАК пояснил необходимость в новой системе обозначений тем, что номенклатура Ингольда предназначена не для описания механизмов, а для обозначения типа превращения, вследствие чего могут возникать двусмысленные ситуации, когда, например, ингольдовское обозначение SE2 применяется как для одностадийного ароматического замещения, так и для двустадийной реакции у алифатического атома углерода[9].
Примечания
- IUPAC Gold Book — Mechanism of a reaction. Дата обращения: 24 декабря 2014.
- Jeremy N. Harvey. Spin-forbidden reactions: computational insight into mechanisms and kinetics (англ.) // Wiley Interdisciplinary Reviews: Computational Molecular Science. — 2014-01-01. — Vol. 4, iss. 1. — P. 1–14. — ISSN 1759-0884. — doi:10.1002/wcms.1154.
- Aleksandr O. Lykhin, Danil S. Kaliakin, Gwen E. dePolo, Alexander A. Kuzubov, Sergey A. Varganov. Nonadiabatic transition state theory: Application to intersystem crossings in the active sites of metal-sulfur proteins (англ.) // International Journal of Quantum Chemistry. — 2016-05-15. — Vol. 116, iss. 10. — P. 750–761. — ISSN 1097-461X. — doi:10.1002/qua.25124.
- Dmitry A. Fedorov, Spencer R. Pruitt, Kristopher Keipert, Mark S. Gordon, Sergey A. Varganov. Ab Initio Multiple Spawning Method for Intersystem Crossing Dynamics: Spin-Forbidden Transitions between3B1and1A1States of GeH2 (EN) // The Journal of Physical Chemistry A. — 2016-04-27. — Т. 120, вып. 18. — С. 2911–2919. — doi:10.1021/acs.jpca.6b01406.
- Danil S. Kaliakin, Ryan R. Zaari, Sergey A. Varganov. Effect of H 2 Binding on the Nonadiabatic Transition Probability between Singlet and Triplet States of the [NiFe-Hydrogenase Active Site] (EN) // The Journal of Physical Chemistry A. — 2015-01-30. — Т. 119, вып. 6. — С. 1066–1073. — doi:10.1021/jp510522z.
- Jeremy N Harvey, Rinaldo Poli, Kevin M Smith. Understanding the reactivity of transition metal complexes involving multiple spin states // Coordination Chemistry Reviews. — 2003-03-01. — Т. 238–239. — С. 347–361. — doi:10.1016/S0010-8545(02)00283-7.
- Olah G. A. Comments on “IUPAC Recommendations for the Representation of Reaction Mechanisms” (англ.) // Acc. Chem. Res. — 1990. — Vol. 23, no. 2. — P. 31—32. — doi:10.1021/ar00170a001.
- Guthrie D. R. System for symbolic representation of reaction mechanisms (Recommendations 1988) (англ.) // Pure & Appl. Chem. — 1989. — Vol. 61, no. 1. — P. 23—56. — doi:10.1351/pac198961010023.
- Guthrie R. D., Jencks W. P. IUPAC Recommendations for the Representation of Reaction Mechanisms (англ.) // Acc. Chem. Res. — 1989. — Vol. 22, no. 10. — P. 343—349. — doi:10.1021/ar00166a001.