Фосфорорганические соединения
Фосфороргани́ческие соедине́ния (ФОС) — органические соединения, в которых содержится химическая связь фосфор — углерод.
| Фосфорорганические соединения | |
|---|---|
Применение термина
Иногда фосфорорганическими соединениями называют органические соединения фосфора, не содержащие связи фосфор — углерод (например, органические эфиры фосфорных кислот, нуклеотиды).
Применение
Соединения на основе фосфора пытались использовать в самых разных отраслях химической промышленности: для изготовления резины, пластмасс и пр. Кроме того, еще в XIX веке некоторые соединения из этой группы химики той поры называли «пахнущие жидкости с огненным вкусом», в тот же период были заложены основы для получения новых соединений на основе фосфора. Затем они обратили на себя внимание как боевые отравляющие вещества (в 1936 году в Германии был синтезирован газ табун).[1]
В конце Второй мировой войны были сделаны промышленные установки по синтезу первых пестицидов, которые с 1965 года были введены в сельскохозяйственное производство вместо персистентныx и низкоэкологичных хлорорганических соединений типа ДДТ, гексахлорана и других.
В настоящее время фосфорорганические соединения применяют как нервно-паралитические отравляющие вещества, инсектициды, лекарственные средства, стабилизаторы пластмасс, антиокислители моторных масел, антипирены. Применяются также как катализаторы и лиганды для металлокомплексного катализа.
Действие на живые организмы
Чаще всего промышленные фосфорорганические соединения — это яды нервно-паралитического действия, вызывающие смерть в течение первых часов после контакта. Данные вещества, попадая в организм, замещают ферменты, отвечающие за передачу нервного импульса в синапсах, вследствие нарушения передачи сигнала возникает тремор, переходящий в полный паралич (смерть наступает от паралича дыхательных мышц). Также фосфорорганические соединения, воздействуя на центральную нервную систему, способны вызывать конвульсии, потерю чувствительности к свету, потерю равновесия, нарушения сознания, потерю сна, кому. При этом яд может с легкостью проникать в организм через кожу, желудок или дыхательные пути[1] (обладая жирорастворимостью, легко проникают через фосфолипиды билипидного слоя клеточных мембран).
Механизм действия заключается в том, что при попадании в организм они фосфорилируют белковый фермент ацетилхолинэстеразу, который играет важную роль в передаче нервного импульса.
Есть довольно много фосфорорганических соединений, не ингибирующих холинэстеразу (этидронат, антиокислители моторных масел, антипирены) и обладающих другими симптомами отравления.
Важнейшие типы
| Общая формула | Название класса соединений |
|---|---|
| P(R)3 или R1R2R3P | Фосфины |
| RP(OH)2 или R-P(O)H-OH | фосфонистые кислоты |
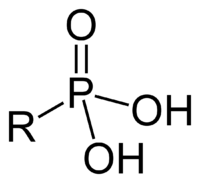 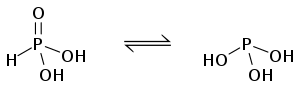 |
Фосфоновые кислоты |
| R(РООН)R1 | Фосфиновые кислоты |
| Фосфонаты | |
 Двойная спираль ДНК |
Нуклеиновые кислоты |
 Аденозиндифосфат |
Нуклеотиды |
Действие на материалы
Разрушает металлы, пробку, резину, бакелит, полиэтилен. Не действует на фторопласт и полиакрилаты.
Примечания
- Роман Потапов. Химия, изменившая мир. — Москва, 2018. — С. 16. — 70 с. — ISBN 978-5-4490-4468-6.
Литература
- Фосфорорганические соединения / Нифантьев Э. Е. // Уланд — Хватцев. — М. : Большая российская энциклопедия, 2017. — С. 504. — (Большая российская энциклопедия : [в 35 т.] / гл. ред. Ю. С. Осипов ; 2004—2017, т. 33). — ISBN 978-5-85270-370-5. (Фосфорорганические соединения / Нифантьев Э. Е. // Большая российская энциклопедия [Электронный ресурс]. — 2018.)
- Фосфорорганические соединения / Розенгарт E. В. // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1985. — Т. 26 : Углекислые воды. — 560 с. : ил.
- Фосфорорганические соединения // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
- Фосфорорганические отравляющие вещества // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
- Фосфорорганические пестициды // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
- Фосфорорганические инсектициды // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.