Изонитрилы
Изонитрилы (изоцианиды, карбиламины) — органические соединения общей формулы ![]() , изомерны нитрилам R—C≡N. ИЮПАК рекомендует использовать название «изоцианиды»[1]. Изонитрилы токсичны и обладают сильным отвратительным запахом, низшие изонитрилы представляют собой жидкости.
, изомерны нитрилам R—C≡N. ИЮПАК рекомендует использовать название «изоцианиды»[1]. Изонитрилы токсичны и обладают сильным отвратительным запахом, низшие изонитрилы представляют собой жидкости.
Свойства
Структуру изонитрильной группы можно представить как резонансный гибрид двух канонических форм — биполярной с отрицательным зарядом на атоме углерода и карбеновой с двухвалентным углеродом:
Изонитрильная группа, подобно нитрильной, линейна (угол C-N-C составляет 180°), длина связи C=N в изонитрилах — 0,117 нм также близка длине нитрильной связи — 0,116 нм, близки и параметры ИК-спектров у изонитрилов характеристическая полоса при 2100—2200 см−1, у нитрилов — при 2200—2250 см−1, что свидетельствует о большем вкладе биполярной структуры.
В ЯМР-спектрах 13C изонитрильный атом углерода дает сигнал при 150—160 м.д.
Реакционная способность
Изонитрильная группа - единственная стабильная функциональная группа, содержащая двухвалентный углерод (в карбеновой резонансной форме), поэтому для неё характерны реакции 1,1-присоединения к углероду, восстанавливающие его устойчивое четырехвалентное состояние, а не 1,2 присоединения к кратной связи, характерные для нитрилов.
Другой особенностью является локализация отрицательного заряда на углероде в биполярной резонансной форме, что обусловливает их высокую реакционную способность к электрофильным агентам и пониженную, в отличие от нитрилов, по отношению к нуклеофильным.
Реакции с электрофилами
Изонитрилы реагируют с электрофильными реагентами с образованием продуктов 1,1-присоединения к атому углерода, при этом Изонитрилы бурно реагируют с галогенами - хлором, бромом и даже йодом, образуя иминокарбонилдигалогениды, в синтетической практике реакцию проводят при охлаждении:
- R—N≡C + Hal2 RNC(Hal)2
Взаимодействие изоцианидов с безводными галогеноводородами ведет к образованию солей формимидоилгалогенидов:
- R—N≡C + HHal RN=CHHal•HHal
Изонитрилы ацилируются хлорангидридами карбоновых кислот с образованием α-кетоимидоилхлоридов:
- R—N≡C + R1COCl RN=C(Cl)COR1
Реакция карбоновых кислот с изонитрилами через промежуточное образование ацилимидатов ведет к образованию ангидридов карбоновых кислот и N-формамидов:
- R—N≡C + R1COOH RN=CHOCOR1
- RN=CHOCOR1 + R1COOH RNHCHO + (R1CO)2O
Электрофильная атака sp2 С-электрофилов (кетонов и солей иминов) на нуклеофильный атом углерода изонитрилов лежит в основе реакций Пассерини и Уги.
Реакции с нуклеофилами
Изонитрилы устойчивы к нуклеофильным атакам: они не гидролизуются в щелочных условиях, не взаимодействуют со спиртами и не реагируют с аминами даже при нагревании.
Однако при протонировании атома углерода изонитрильной группы образуется высокоэлектрофильный катион:
- R—N≡C + H+ R—N+≡CH ,
который реагирует с нуклеофилами: в условиях кислотного катализа изонитрилы реагируют со спиртами, тиолами и аминами; аналогичный каталитический эффект оказывают и соли некоторых переходных металлов (в частности, цинка и одновалентной меди).
Так, в кислой среде изонитрилы легко гидролизуются до N-замещенных формамидов и присоединяют сероводород с образованием N-замещенных тиоформамидов:
- R—N≡C + H2X RNHCHX
В присутствии хлорида меди(I) амины реагируют с изонитрилами с образованием замещенных формамидинов, аналогично в этих условиях реагируют и гидразины, образуя формамидразоны:
- R—N≡C + R1NH2 HC(=NR)NHR1,
- R1 = Ar, Alk, ArNH, AlkNH
Окисление и восстановление
Изонитрилы окисляются до изоцианатов под действием разнообразных окислителей - диметилсульфоксида[2], оксида ртути(II) и т.д.:
- R—N≡C + [O] RN=C=О
Окисление изонитрилов в присутствии соответствующих нуклеофилов является синтетическим эквивалентом реакции изоцианата с нуклеофилом.
Так, окисление изонитрилов ацетатом трехвалентного таллия в присутствии спиртов приводит к образованию соответствующих карбаматов[3]:
- R—N≡C + Tl(OAc)3 + R1ОН R-N=C(OR1)Tl(OAc)3 + AcOH
- R-N=C(OR1)Tl(OAc)3 + R1ОН R-N=C(OR1)2
- R-N=C(OR1)2 + AcOH RNHCO2R1 + AcOR1
Окислительное присоединение первичных аминов к изонитрилам ведет к образованию карбодиимидов, в качестве окислителя в таких реакциях выступает молекулярный кислород[4]:
- R—N≡C + R1NH2 + [O] R-N=C=N-R1 + H2O
Аналогичным образом изонитрилы взаимодействуют и с серой, образуя изотиоцианаты:
- R—N≡C + [S] RN=C=S
Восстановление изонитрилов (алюмогидридом лития, натрием в этаноле, каталитическое над платиновой чернью и т.п.), как правило, ведет к образованию вторичных метиламинов:
- R—N≡C + [H] RNHCH3 ,
однако под действием трибутилгидрида олова алкилизонитрилы восстанавливаются до алканов:
- R—N≡C + [H] RH
Комплексообразование
Изонитрилы образуют комплексы с переходными металлами, открытие комплексов изонитрилов произошло одновременно с синтезом первого представителя изонитрилов - аллилизонитрила - взаимодействием аллилйодида с цианидом серебра: в этой реакции происходит образование изоцианидного комплекса серебра.
Изонитрилы являются σ-донорными лигандами средней силы и сильными π-акцепторными лигандами и в силу этого изонитрильные комплексы схожи с карбонилами металлов: так, изонитрилы, как и окись углерода, в комплексе стабилизируют низшие степени окисления металлов и могут образовывать мостики между атомами металлов, образуя многоядерные комплексы - в том числе и многоядерные нульвалентные комплексы, например, трет-бутилизонитрильный комплекс железа Fe2(t-BuNC)9, аналогичный нонакарбонилу железа Fe2(CO)9[5].
Синтез
Изонитрилы были впервые синтезированы в 1859 году, когда Лике синтезировал аллилизоцианид взаимодействием [6] аллилйодида с цианидом серебра. Этот метод синтеза подобен синтезу нитрилов алкилированием «свободного» цианид-иона цианидов щелочных металлов алкилгалогенидами, однако в случае использования цианидов серебра и одновалентной меди, образующих цианидные комплексы, в которых с металлом связывается атом азота цианид-иона, алкилирование происходит по атому углерода и образуется изоцианидный комплекс:
- AlkI + AgCN AlkN≡C·AgI
Из такого комплекса изонитрил высвобождается действием цианида калия:
- AlkN≡C·AgI + KCN AlkN≡C + K[AgI(CN)]
Выходы в классическом варианте этой реакции относительно невысоки (до 55 %), однако могут быть повышены её проведением в апротонных растворителях в условиях межфазного катализа в присутствии четвертичных фосфониевых или аммониевых солей. Наилучшие результаты дает проведение реакции в гомогенной среде, например, при использовании в качестве донора цианида дицианоаргентатом тетраметиламмония, выходы в этом случае близки к количественным.
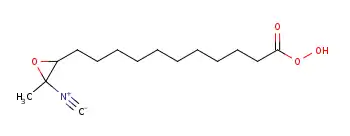
Близким к этому методу является взаимодействие эпоксидов с триметилсилилцианидом, катализируемое хлоридом цинка, ведущее к образованию алифатических β-триметилсилоксиизонитрилов, которые могут быть далее гидролизованы до β-гидроксиизонитрилов, выходы в реакции высоки и превышают по β-гидроксиизонитрилам превышают 90%[7].
Другим классическим методом синтеза изонитрилов является открытая в 1867 году Готье[8] и Гофманом[9] реакция между первичным амином и хлороформом в спиртовом растворе щелочи (карбиламинная реакция Гофмана), идущая через образование дихлоркарбена и его взаимодействие с амином:
- CHCl3 + KOH :CCl2 + KCl + H2O
- RNH2 + :CCl2 + 2KOH R-N≡C + 2KCl + 2H2O
По аналогичному механизму протекает взаимодействие первичных аминов с трихлорацетатом натрия, разлагающегося при нагревании с образованием дихлоркарбена.
Изонитрилы также синтезируются дегидратацией N-монозамещенных формамидов под действием различных водоотнимающих агентов - например, хлорангидридов кислот[10] или комбинации трифенилфосфина с четыреххлористым углеродом[11]:
- RNHCHO R-N≡C
Другим общим методом синтеза изонитрилов исходя из альдегидов является их конденсация с 5-аминотетразолом, восстановлением образовавшихся иминов в N-замещенные 5-аминотетразолы и их окислениее гипобромитом натрия[12]:
- RCHO + Tetr-NH2 RCHNTetr
- RCHNTetr + [H] RCH2NHTetr
- RCH2NHTetr + NaBrO R-N≡C + 3N2 + H2O + NaBr
Изонитрильная проба по Гофману
Изонитрилы обладают сильным отвратительным запахом, эта особенность используется для качественного обнаружения первичных аминов в изонитрильной пробе по Гофману: раствор исследуемого вещества в хлороформе добавляется к спиртовому раствору щелочи, образующийся из первичного амина изонитрил легко обнаруживается по сильному характерному запаху; благодаря сильному запаху изонитрилов проба высокочувствительна.
Нахождение в природе
Изонитрилы относительно редко встречаются в природе, первым обнаруженным в природных источниках изонитрилом стал ксантоциллин, продуцируемый Penicillium notatum и выделенный в 1957 г. В дальнейшем был выделен и ряд других изонитрилов, обладающих биологической активностью, в частности, антибиотик аэроцианидин из бактерий Chromobacterium violaceum:
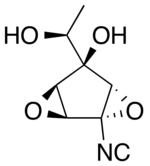
и микотоксин триховиридин грибов рода Trichoderma spp.:
В морских беспозвоночных — губках и голожаберных моллюсках — обнаружены терпеноидные изонитрилы и биогенетически связанные с ними формамиды, изотиоцианаты и, в некоторых случаях, даже иминокарбонилдихлориды[13].
Примечания
- isocyanides // IUPAC Gold Book
- Martin, D.; A. Weise. Acid‐Catalysed Oxidation of Isocyanides with Dimethyl Sulfoxide (англ.) // Angewandte Chemie International Edition in English : journal. — 1967. — 1 February (vol. 6, no. 2). — P. 168—169. — ISSN 1521-3773. — doi:10.1002/anie.196701682.
- Tanaka, Sakuya; Hiroshi Kido, Sakae Uemura, Masaya Okano. Oxidation of Isocyanides by Hg(II), Tl(III), and Pb(IV) Acetates (англ.) // Bulletin of the Chemical Society of Japan : journal. — 1975. — Vol. 48, no. 11. — P. 3415—3416. — ISSN 0009-2673. — doi:10.1246/bcsj.48.3415. (недоступная ссылка)
- Cotarca, Livius; Heiner Eckert. Phosgenations--a handbook (неопр.). — Wiley-VCH, 2004. — С. 445—446. — ISBN 9783527298235.
- Bassett, J.M.; Barker, G.K.; Green, M.; Howard, J.A.; Stone, G.A.; Wolsey, W.C. "Chemistry of low-valent metal isocyanide complexes" J.C.S. Dalton, 1981, 219-227.
- Lieke, W., Justus Liebigs Ann. Chem. 1859, 112, 316
- Paul G. Gassman and Thomas L. Guggenheim. Conversion of epoxides to β-hydroxy isocyanides: trans-2-isocyanocyclohexanol. Org. Synth. 1986, 64, 39 DOI: 10.15227/orgsyn.064.0039
- Gautier, A., Justus Liebigs Ann. Chem. 1867, 142, 289; Ann. Chim. (Paris) 1869, 17, 103, 203
- Hofmann, A. W., Ber. Dtsch. Chem. Ges. 1870, 3, 63
- R. E. Schuster, James E. Scott, Joseph Casanova, Jr. Methyl isocyanide. Organic Syntheses, Coll. Vol. 5, p.772 (1973); Vol. 46, p.75 (1966). (недоступная ссылка). Дата обращения: 13 апреля 2011. Архивировано 15 января 2011 года.
- Francesco Amato and Stefano Marcaccini. 2,2-Diethoxy-1-isocyanoethane. Org. Synth. 2005, 82, 18. DOI: 10.15227/orgsyn.082.0018
- Höfle, Gerhard, Bernd Lange. Oxidation of 5-aminotetrazoles: benzyl isocyanide, Organic Syntheses (1983), С. 14. Архивировано 17 октября 2012 года. Дата обращения 19 мая 2011.
- Garson, M. J.; J. S. Simpson. Marine isocyanides and related natural products–structure, biosynthesis and ecology (англ.) // Natural product reports : journal. — 2004. — Vol. 21, no. 1. — P. 164—179.