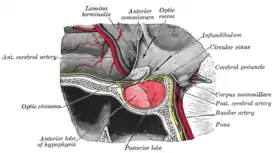
Краниофарингиома
Краниофарингио́ма (др.-греч. κρανίον — череп + φάρυγξ — глотка + -ωμα от ὄγκωμα — опухоль) — врождённая опухоль головного мозга эпителиального строения, которая развивается из эмбриональных клеток гипофизарного хода (т. н. кармана Ратке). В большинстве случаев доброкачественная, озлокачествление происходит чрезвычайно редко[1].
| Краниофарингиома | |
|---|---|
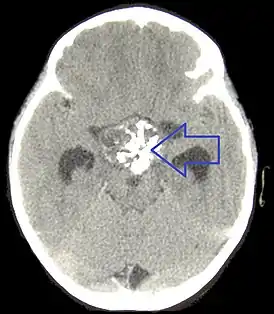 КТ головы. Краниофарингиома находится в центре изображения | |
| МКБ-11 | XH1AZ2 |
| МКБ-10 | D44.4 |
| МКБ-9 | 237.0 |
| МКБ-О | 9350/1 |
| DiseasesDB | 3153 |
| MedlinePlus | 000345 |
| eMedicine | radio/196 |
| MeSH | D003397 |
Синонимами термина «краниофарингиома» являются опухоль кармана Ратке, опухоль гипофизарного хода, опухоль Эрдхайма[1].
Это относительно редкое новообразование центральной нервной системы. Ежегодно выявляют 0,5—2 новых случая заболевания на 1 миллион населения[2][3].
В клинической картине характерны нарушения зрения, головная боль, гормональные расстройства и поражение черепных нервов. Также могут возникать психотические состояния[4]. Лечение преимущественно хирургическое. Прогноз во многом определяется размерами и локализацией опухоли, а также качеством оказания медицинской помощи. Послеоперационная летальность составляет 5—10 %, а 5-летняя выживаемость 55—85 %[5].
История изучения

Первое описание краниофарингиомы датируется 1857 годом. В этом году немецкий патологоанатом Фридрих Ценкер опубликовал статью о внутримозговом новообразовании соответствующей локализации, которое содержало кристаллы холестерина[6][7]. В 1892 году российский невропатолог Яков Онанов, обнаружив общие гистологические черты краниофарингиомы и опухолей челюсти, предложил название «гипофизарная адамантинома»[7]. В 1899 году британскими патологоанатомами Моттом и Бареттом были исследованы несколько эпителиальных опухолей в области турецкого седла. Они пришли к выводу, что данный тип новообразований произрастает либо из клеток кармана Ратке, либо из гипофизарного протока[8]. Знаменитые неврологи Жозеф Бабинский[9] и Альфред Фрёлих[10] описали заболевание как «супраселлярное новообразование без акромегалии». Первая операция по удалению краниофарингиомы была произведена в 1909 году У. Холстедом[11].

В 1924 году данный тип новообразований был назван опухолями краниофарингеального кармана[12]. Также встречались названия амелобластома, эпидермоидная и краниофарингеальная жировая (англ. craniopharyngeal fat tumor) опухоль. Основоположником американской и мировой нейрохирургии Х. Кушингом был предложен термин «краниофарингиома», который и получил мировое признание[13].
Первые попытки удаления данных новообразований сопровождались высокой смертностью (до 40 %) и низким удельным весом тотального их удаления (до 15 %)[14]. В связи с этим в 1960-х годах превалировало мнение о том, что пункция краниофарингиом, с целью уменьшения их объёма, с последующей радиотерапией предпочтительней попыток их радикального хирургического удаления[15]. После улучшения оперативных технологий в 1970-х лечебная тактика была пересмотрена в пользу хирургии[16][17][18].
Эпидемиология
Краниофарингиомы составляют от 1 до 4 % всех первичных внутричерепных новообразований[19][20]. У детей их удельный вес среди опухолей мозга колеблется от 5 до 10 %. У лиц старше 16 лет встречается до 60 % новообразований данного типа. Существует два пика заболеваемости — от 6 до 16 лет и от 50 до 70[21].
Чаще всего заболевание встречается в Китае (до 6,5 % всех первичных внутричерепных новообразований), реже всего в Австралии (до 1,5 %)[22][23][24].
Исследование заболеваемости населения нескольких штатов США определило, что ежегодно на 100 тысяч населения определяется 0,13 новых случаев[25]. Согласно другим исследованиям на 1 миллион населения ежегодно диагностируют от 0,5 до 2,0 новых случаев данных новообразований[2][3].
Эмбриология
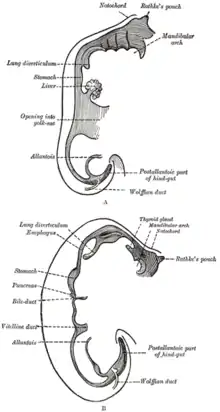
На 4-й неделе формирования плода начинает происходить инвагинация эпителия эмбриональной ротовой ямки. Образуется так называемый карман Ратке. Впоследствии из его клеток сформируется аденогипофиз. Одновременно со стороны гипоталамуса мигрируют нейроэпителиальные клетки, которые являются основой для образования нейрогипофиза[7].
Когда карман Ратке достигает определённого размера, он отсоединяется от эмбриональной ротовой ямки. После этого происходит его ротация вокруг собственной оси. Этот поворот приводит к тому, что эмбриональные клетки заносятся супра- и параселлярно[7]. После формирования аденогипофиза происходит инволюция эмбриональных клеток кармана Ратке (краниофарингеального пути). В 1904 году Эрдхайм показал, что при отсутствии инволюции данных клеток именно из них развивается краниофарингиома[26]. Современные исследования подтверждают выводы Эрдхайма[27][28].
Существует противоположное теории Эрдхайма предположение о том, что краниофарингиомы возникают за счёт метаплазии клеток аденогипофиза[7].
Патологическая анатомия
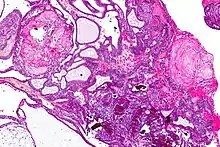
В зависимости от структуры различают два основных вида краниофарингиом — состоящий из плотной ткани и кистозный. В диаметре их размер колеблется от 2 до 5 см, реже больше. Растёт медленно, экспансивно. Кистозно перерождённые участки опухоли содержат от 10 до 50 (в редких случаях до 200) мл жидкости жёлтого, янтарного или кофейного цвета. Имеет плотную капсулу, довольно прочно связанную с окружающей её мозговой тканью, оболочками и сосудистой сетью. Кровоснабжение опухоли осуществляется из ветвей артериального круга большого мозга[1].
Структура краниофарингиомы с течением времени может значительно видоизменяться. В её компактных слоях происходит колликвационный некроз с формированием кист, которые содержат жидкость с большим содержанием белка (от 20 до 100 ‰ и более), кристаллов холестерина и жирных кислот. На внутренней поверхности капсулы происходит отложение солей. Гистологически краниофарингиомы состоят из эпителиальных клеток различной степени дифференциации. Выделяют адамантиматозный и папиллярный гистологические варианты строения краниофарингиомы[29]. Наряду с эпителиальными клетками эмбрионального типа встречается и эпителий эпидермального типа. Клеточные скопления в ряде случаев могут напоминать адамантиномы. Также в краниофарингиомах всегда наблюдаются дистрофические изменения различной степени выраженности в виде кистообразования, обызвествления или даже оссификации стромы. Капсула состоит из соединительной или глиальной тканей. Разнообразие в строении краниофарингиом может расцениваться как результат фазности развития новообразования[1].
Классификация
На основании опыта лечения 437 больных врачи из университета Сычуаня предложили топографо-анатомическую классификацию краниофарингиом[30].
- Тип I — располагающиеся спереди ножки гипофиза
- подтип A — расположенные под диафрагмой турецкого седла
- подтип B — расположенные над диафрагмой турецкого седла спереди от перекрёста зрительных нервов
- подтип С — расположенные над диафрагмой турецкого седла между перекрёстом зрительных нервов и ножкой гипофиза
- Тип II — располагающиеся непосредственно над ножкой гипофиза (обычно сдавливают полость III желудочка головного мозга)
- Тип III — располагающиеся сзади от ножки гипофиза
- подтип A — расположенные под диафрагмой турецкого седла
- подтип B — расположенные над диафрагмой турецкого седла. Достигают передней трети варолиевого моста
- подтип С — расположенные над диафрагмой турецкого седла. Достигают мостомозжечкового угла
- Тип IV — расположенные около ножки гипофиза (обычно в области базальных ганглиев)
- Тип V — эктопически расположенные краниофарингиомы (в полости III, IV желудочков головного мозга, в области придаточных пазух носа)
Классификация имеет непосредственное прикладное значение. В зависимости от типа и подтипа краниофарингиомы рекомендуется проводить тот или иной хирургический доступ[30].
Клиника
Наиболее ранними симптомами являются зрительные нарушения и головная боль, которые вызваны давлением новообразования на хиазму зрительных нервов и повышением внутричерепного давления. Внутричерепная гипертензия возникает вследствие нарушения оттока ликвора из сдавленного опухолью III желудочка. В зависимости от расположения опухоли по отношению к хиазме, то есть снизу, сверху или сбоку, возникают различные варианты сужения полей зрения. Чаще всего заболевание дебютируют с нижней или верхней квадрантной гемианопсии. Значительно реже наблюдается слепота на один глаз вследствие полного поражения одного зрительного тракта и внутренней половины другого[4].
При интраселлярных краниофарингиомах боль сосредоточена в височных областях и во лбу над переносьем. Боль усиливается при перкуссии этих областей. При супра- и интрасупраселлярных краниофарингиомах, которые вызывают повышение внутричерепного давления, головная боль имеет общий характер[4].
К частым симптомам краниофарингиом относится адипозогенитальный синдром, особенно у подростков. Реже встречается синдром Фрёлиха. Его развитие связывают с поражением серого бугра. Вместе с похудением развивается синдром гипогенитализма: нарушения менструального периода, недоразвитие вторичных половых признаков, инфантилизм, а также значительная задержка роста[4].
Достаточно часто возникает несахарный диабет. Суточное количество мочи может достигать 10 л и более. Заболевание может носить преходящий характер и иногда является первым проявлением заболевания[4].
При супраселлярной локализации краниофарингиом, особенно при их прорастании в III желудочек, часто наблюдаются расстройства сна[4].
При супраселлярных краниофарингиомах также отмечается оглушение, обусловленное гидроцефально-гипертензионным синдромом. Могут наблюдаться психотические состояния: спутанность, двигательное возбуждение, шизофреноподобные состояния, маниакальное возбуждение, сменяющиеся кататоническим состоянием и т. п.[4]
При краниофарингиомах сравнительно часто наблюдаются симптомы поражения черепных нервов. При росте опухоли в направлении лобных долей наблюдаются расстройства обоняния, а в параселлярном направлении — нарушение функции глазодвигательных нервов, реже одно- или двусторонний парез отводящего нерва, невралгии первой и второй ветвей тройничного нерва. Таким образом, поражение того или иного черепного нерва позволяет судить о направлении роста новообразования[4].
Нарушение двигательных функций встречается редко. Они могут наблюдаться при росте опухоли кзади в интерпедункулярное пространство и сдавлении ножек мозга. В четверти случаев у больных отмечаются эпилептические припадки[4].
Диагностика
Диагностика основана на применении методов медицинской визуализации, заподозрить заболевание можно при рентгенографии черепа, подтверждается диагноз при компьютерной томографии или МРТ.
Рентгенография
Обзорная рентгенография в диагностике краниофарингиом устарела. На данный момент для специфической диагностики опухолей в клинической практике она не используется. В ряде случаев выявление признаков опухоли на краниограммах является случайной находкой. При их обнаружении следует дообследовать больного с помощью более совершенных методов диагностики (КТ, МРТ).
На рентгенограммах при краниофарингиоме видны обызвествление опухоли, атрофия от давления на прилежащие костные образования и признаки гидроцефально-гипертензионного синдрома[31].
Обызвествления краниофарингиом обычно развиваются по периферии капсулы кисты или в самой опухоли. Возможно их сочетание. Они проецируются над диафрагмой турецкого седла и исключительно редко — под диафрагмой. Являясь непосредственным признаком роста и расположения опухоли, обызвествления не полностью отражают её протяжённость, так как развиваются в дегенерированной ткани. Расположение обызвествлений в опухоли и атрофия костных образований позволяют косвенно судить о преимущественном направлении роста новообразований[31].
Компьютерная томография
Компьютерная томография головного мозга хорошо выявляет как плотную, так и кистозную части краниофарингиом. Кальцификаты определяются в 95 % случаев у детей и примерно в 50 % у взрослых. Кистозный компонент имеет несколько бо́льшую плотность по сравнению с ликвором, распространяется кпереди и/или латерально и обычно окружает солидный компонент. При введении контрастных веществ яркость узловой части опухоли в половине наблюдений увеличивается на 8—10 единиц Хаунсфилда[32], что встречается в 90 % случаев[33]. Может визуализироваться смещение А1 сегмента передней мозговой артерии или хиазмы зрительного нерва[34].
Магнитно-резонансная томография
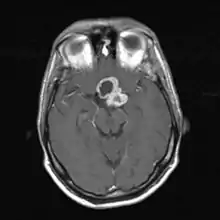
Магнитно-резонансная томография (МРТ) даёт возможность определить точные размеры краниофарингиом, соотношение их узловой и кистозной частей, размеры и локализацию. Также МРТ даёт представление о состоянии желудочковой системы, наличии или отсутствии гидроцефалии, топографо-анатомическом взаимоотношении опухоли и дна III желудочка[32].
Сигнал от данного новообразования вариабелен[35]. В большинстве случаев кистозный компонент имеет гипоинтенсивный сигнал в режиме Т1 и гиперинтенсивный — в режиме Т2. При наличии высокой концентрации белка, продуктов распада крови, холестерина сигнал от кистозной жидкости может существенно меняться[36]. Это проявляется в повышении интенсивности сигнала. Данная особенность является высокоспецифичной именно для краниофарингиом. В режиме Т2 яркость сигнала может варьировать от гипер- до изоинтенсивного[32].
Солидная часть краниофарингиом в большинстве случаев не отличается по интенсивности сигнала от вещества мозга. При введении контрастных препаратов плотность сигнала усиливается[32].
При эндоселлярных краниофарингиомах размеры турецкого седла увеличены. Распространяясь вверх, новообразование заполняет область хиазмальных цистерн, в той или иной степени поддавливает дно III желудочка. Супраселлярная часть краниофарингиом чаще кистозная. Кисты могут распространяться на основание передней черепной ямки, перивентрикулярно или определяться внутри узловой части опухоли. Краниофарингиома чаще всего хорошо отграничена от прилежащего мозгового вещества[32].
При стебельных краниофарингиомах обнаруживаются характерная асимметрия, значительная величина и распространение по основанию мозга, частичное внедрение в полость боковых желудочков. Локализуясь в полости бокового желудочка, кисты могут тампонировать его[32].
Лечение
Лечение преимущественно хирургическое. Его целью является тотальное удаление опухоли. В ряде случаев это не представляется возможным. В послеоперационном периоде и при возникновении рецидивов оправдано применение лучевой терапии и радиохирургии.
Хирургическое лечение
Лечение краниофарингиом преимущественно хирургическое. Тип доступа зависит от топографо-анатомических типа и подтипа опухоли[30]:
| Тип краниофарингиомы | Вид применяемых оперативных доступов |
|---|---|
| Транссфеноидальный | |
| Субфронтальный | |
| Птериональный, транссфеноидальный, транскаллёзный | |
| Птериональный, транссфеноидальный, транскаллёзный, трансламинальный | |
| Транссфеноидальный | |
| Птериональный, транссфеноидальный, транскалёзный, трансламинальный | |
| Комбинированный супра- и инфратенториальный | |
| Птериональный, субтемпоральный | |
| Зависит от места расположения и величины новообразования | |
В послеоперационном периоде больным следует назначать глюкокортикоиды. Отменяют их постепенно. Частым послеоперационным осложнением является появление признаков несахарного диабета. Главным при его лечении является замещение теряемой жидкости. При необходимости применяют препараты антидиуретического гормона[5].
Лучевая терапия и радиохирургия
На вторую половину 2011 года радиохирургия и лучевая терапия не рассматриваются как самостоятельный вид лечения краниофарингиом. При этом их проведение показано в послеоперационном периоде и при рецидивировании опухоли[37][38][39]. Результаты облучения противоречивы. К побочным действиям относят эндокринные нарушения, неврит зрительных нервов, деменцию[5]. У детей проведение радиотерапии хоть и препятствует росту остатков опухоли[40], отрицательно влияет на умственное развитие[5].
Прогноз
Прогноз во многом определяется размерами и локализацией опухоли, а также качеством оказания медицинской помощи. Послеоперационная летальность составляет 5—10 %, в основном в связи с повреждением гипоталамических структур. Пятилетняя выживаемость (количество больных, которые живы через 5 лет после операции) составляет 55—85 %. Показатель является хоть и широко используемым, но относительным, так как включает также смертность от не связанных с основным заболеванием причин. Большинство рецидивов наблюдается в течение 1 года после операции, значительно меньше — в срок более 3 лет[5]. Согласно различным данным, краниофарингиома рецидивирует в 5—35 % случаев. Большинство рецидивов возникают в течение пяти лет после операции[41][2][42][43][44].
Примечания
- Арендт А. А., Коновалов А. Н. Краниофарингиома // Большая медицинская энциклопедия / под общей редакцией Б. В. Петровского. — 3-е издание. — М.:: «Советская энциклопедия», 1979. — Т. 11. — С. 487—489. — 544 с. — 150 000 экз.
- Sorva R., Heiskanen O. Craniopharyngioma in Finland. A study of 123 cases // Acta Neurochir (Wien). — 1986. — Т. 81. — С. 85—89. — PMID 3489356.
- Banna M. Craniopharyngioma in adults // Surg Neurol. — 1973. — Т. 1. — С. 202—204. — PMID 4542446.
- Раздольский И. Я. Невринома слухового нерва // Опухоли кармана ратке (краниофарингиомы). — Ленинград: Медгиз, 1957. — С. 117—123. — 224 с. — 10 000 экз.
- Гринберг Марк. Краниофарингиома // Нейрохирургия. — М.:: МЕДпресс-информ, 2010. — С. 474—476. — 1008 с. — 1000 экз. — ISBN 978-5-98322-550-3.
- Zenker F. A. Enormcystenbildung im gehirn, von hiranhang ausgehend (нем.) // Arch Pathol Anat Physiol Klin Med. — 1857. — Bd. 2. — S. 454—466.
- Mehta V., Black P. Chapter 67. Craniopharyngioma in the Adult // Youmans Neurological Surgery / ed. by H. R. Winn. — 5th edition. — Philadelphia, PA: SAUNDERS, 2004. — Vol. 1. — P. 1207—1222. — ISBN 0-7216-8291-X.
- Mott F. W., Barrett J. O. W. Three cases of tumors of the third ventricle // Arch Heurol (London). — 1899. — Т. 1. — С. 417—440.
- Babinski J. Tumeur du corps pituitaire sans acromegalie et avec arret de development des organes genitaus // Rev Neurol (Paris). — 1900. — Т. 8. — С. 531—533.
- Fröhlich Alfred. Ein Fall von Tumor der Hypophysis Cerebri ohne Akromegalie // Wien Klin Rundschau. — 1901. — Т. 15. — С. 883—906.
- Halsteadt. Remarks on an operative treatment of tumors of the hypophysis // Surg Gynecol Obstet. — 1910. — Т. 10. — С. 494—502.
- McKenzie K. G., Sosman M. C. The roentgenological diagnosis of craniopharyngeal pouch tumors // Am J Roenthenol. — 1924. — Т. 11. — С. 171—176.
- Cushing H. The craniopharyngiomas // Intracranial Tumors: Notes upon a Series of Two Thousand Verified Cases with Surgical Mortality Percentages Pertaining Thereto / ed. by Thomas CC. — Springfield, Il: Charles C. Thomas, 1932. — P. 93—98.
- Grant F. C. Surgical experience with tumors of the pituitary gland // J Am Med Assoc. — 1948. — Т. 136. — С. 668—72. — PMID 18900421.
- Kramer S., McKissock M., Concannon J. P. Craniopharyngiomas: Treated by combined surgery and radiation therapy // J Neurosurg. — 1961. — Т. 18. — С. 217—226.
- Hoffman H. J., De Silva M., Humphreys R. P., Drake J. M., Smith M. L., Blaser S. I. Aggressive surgical management of craniopharyngiomas in children // J Neurosurg. — 1992. — Т. 76. — С. 47—52. — PMID 1727168.
- Sweet W. H. Radical surgical treatment of craniopharyngioma // Clin Neurosurg. — 1976. — Т. 23. — С. 52—79. — PMID 975700.
- Katz E. L. Late results of radical excision of craniopharyngiomas in children // J Neurosurg. — 1975. — Т. 42. — С. 86—93. — PMID 1110394.
- Russell D. S., Rubinstein L. J. Pathology of Tumors of the Nervous System. — 5th. — Baltimore: Williams&Wilkins, 1989. — С. 695—702.
- Zulch K. J. Brain Tumours: Their Biology and Pathology. — 3rd edition. — New York: Springer, 1986. — С. 426—433.
- Choux M., Lena G., Genitori L. Le craniopharyngiome de l`enfant // Neurochirurgie. — 1991. — Т. 37 (Suppl 1). — С. 12—165.
- Stiller C. A., Nectoux J. International incidence of childhood brain and spinal tumours // Int J Epidemiol. — 1994. — Т. 23. — С. 458—464. — PMID 7960369.
- Cheng M. K. Brain tumors in the People's Republic of China: a statistical review // Neurosurgery. — 1982. — Т. 10. — С. 16—21. — PMID 7057973.
- Ohaegbulam S. C. Craniopharyngioma // J Neurosurg. — 1999. — Т. 89. — С. 984—085. — PMID 10223471.
- Bunin G. R., Surawicz T. S., Witman P. A. et al. The descriptive epidemiology of craniopharyngioma // Neurosurg Focus. — 1997. — Т. 3. — С. e1. — PMID 17206775.
- Erdheim J. Uber Hypophysenganggeschwulste und Hirncholesteathome // Sitzungsbericht der Kaiserlichen Akademie der Wissenschaften. Mathematisch-Naturwissenschaftliche Classe (Wien). — 1904. — Т. 113. — С. 537—726.
- Zumkeller W., Sääf M., Rähn T., Hall K. Demonstration of insulin-like growth factors I, II and heterogeneous insulin-like growth factor binding proteins in the cyst fluid of patients with craniopharyngioma // Neuroendocrinology. — 1991. — Т. 54. — С. 196—201. — PMID 1719442.
- Tachibana O., Yamashima T., Yamashita J., Takabatake Y. Immunohistochemical expression of human chorionic gonadotropin and P-glycoprotein in human pituitary glands and craniopharyngiomas // J Neurosurg. — 1994. — Т. 80. — С. 79—84. — PMID 7903692.
- Коновалов А. Н., Кардышев Б. А., Коршунов А. Г. Опухоли центральной нервной системы // Болезни нервной системы / Под редакцией Н. Н. Яхно, Д. Р. Штульмана. — 3-е. — М.:: Медицина, 2003. — Т. 1. — С. 665. — 744 с. — 5000 экз. — ISBN 5-225-04662-2.
- L. Zhou, C. You. Craniopharyngioma classification // Journal of Neurosurgery. — 2009. — Т. 111, № 1. — С. 197—199.
- Коваль Г. Ю., Даниленко Г. С., Нестеровская В. И. и др. Внемозговые опухоли // Рентгенодиагностика заболеваний и повреждений черепа. — К.:: Здоров`я, 1984. — С. 259—262. — 376 с.
- Коновалов А. Н., Корниенко В. Н., Пронин И. Н. Краниофарингиомы // Магнитно-резонансная томография в нейрохирургии. — М.:: «ВИДАР», 1997. — С. 188—198. — 472 с. — 1500 экз. — ISBN 5-88429-022-5.
- Harwood-Nash DC. Neuroimaging of childhood craniopharyngioma // Pediatric neurosurgery. — Т. 21 Suppl, № 1. — С. 2—10.
- Краниофарингиома. Радиография. Radiographia (03/01/2017).
- Zimmerman R. A. Imaging of intrasellar, suprasellar, and parasellar tumors // Semin Roentgenol. — 1990. — Т. 25. — С. 174—197. — PMID 2190325.
- Ahmadi J., Destian S., Apuzzo M. L., Segall H. D., Zee C. S. Cystic fluid in craniopharyngiomas: MR imaging and quantitative analysis // Radiology. — 1992. — Т. 182. — С. 783—785. — PMID 1535894.
- Jeon C., Kim S., Shin H. J., Nam D. H., Lee J. I., Park K., Kim J. H., Jeon B., Kong D. S. The therapeutic efficacy of fractionated radiotherapy and gamma-knife radiosurgery for craniopharyngiomas // J Clin Neurosci. — 2011. — С. epub. — PMID 22015100.
- Smee RI, Williams JR, Kwok B, Teo C, Stening W. Modern radiotherapy approaches in the management of craniopharyngiomas // J Clin Neurosci. — 2011. — Т. 18. — С. 613—617. — PMID 21439832.
- Liubinas S. V., Munshey A. S., Kaye A. H. Management of recurrent craniopharyngioma // J Clin Neurosci. — 2011. — Т. 18. — С. 451—457. — PMID 21316970.
- Manaka S., Teramoto A., Takakura K. The efficacy of radiotherapy for craniopharyngioma // J Neurosurg. — 1985. — Т. 62. — С. 648—656. — PMID 3989587.
- Samii M., Tatagiba M. Craniopharyngioma // Brain Tumors: An Encyclopedic Approach / Kaye AH, Laws ER Jr (eds). — New York: Churchill Livingston, 1995. — С. 873—894.
- Weiner H. L., Wisoff J. H., Rosenberg M. E., Kupersmith M. J., Cohen H., Zagzag D., Shiminski-Maher T., Flamm E. S., Epstein F. J., Miller D. C. Craniopharyngiomas: a clinicopathological analysis of factors predictive of recurrence and functional outcome // Neurosurgery. — 1994. — Т. 35. — С. 1001—1010. — PMID 7885544.
- Yonekawa Y., Ogata N., Imhof H. G., Olivecrona M., Strommer K., Kwak T. E., Roth P., Groscurth P. Selective extradural anterior clinoidectomy for supra- and parasellar processes. Technical note // J Neurosurg. — 1997. — Т. 87. — С. 636—642. — PMID 9322855.
- Baskin D. S., Wilson C. B. Surgical management of craniopharyngiomas. A review of 74 cases // J Neurosurg. — 1986. — Т. 65. — С. 22—27. — PMID 3712025.