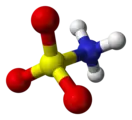
Аминосульфоновая кислота
Аминосульфоновая кислота (Сульфаминовая кислота, моноамид серной кислоты, амидосерная кислота) — кислота, формула которой NH2SO2OH (также NH2SO3H). Производные этой кислоты называют сульфаматами.
| Аминосульфоновая кислота | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Аминосульфоновая кислота | ||
| Традиционные названия | Сульфаминовая кислота; амидосерная кислота | ||
| Хим. формула | NH2SO3H | ||
| Физические свойства | |||
| Молярная масса | 97,09 г/моль | ||
| Плотность | 2,126 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 207 °C | ||
| • разложения | 260 °C | ||
| Химические свойства | |||
| Константа диссоциации кислоты | 1,01 | ||
| Растворимость | |||
| • в воде | 12,80; 17,5720; 22,7740; 27,0660; 32,0180 г/100 мл | ||
| • в ацетоне | 0,04 г/100 мл | ||
| • в диэтиловом эфире | 0,01 г/100 мл | ||
| • в формамиде | 0,18 г/100 мл | ||
| Классификация | |||
| Рег. номер CAS | 5329-14-6 | ||
| PubChem | 5987 | ||
| Рег. номер EINECS | 226-218-8 | ||
| SMILES | |||
| InChI | |||
| RTECS | WO5950000 | ||
| ChEBI | 9330 | ||
| Номер ООН | 2967 | ||
| ChemSpider | 5767 | ||
| Безопасность | |||
| ЛД50 | 3100 мг/кг (мыши) | ||
| Токсичность | Едкое вещество | ||
| Пиктограммы ECB |
|
||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Физические свойства
Аминосульфоновая кислота образует бесцветные кристаллы ромбической сингонии, параметры ячейки a = 0,8036 нм, b = 0,8025 нм, c = 0,9236 нм, Z = 8. Кристаллы состоят из цвиттер-ионов.
Химические свойства
В кристаллическом состоянии сульфаминовая кислота образует цвиттер-ион . При нагревании до 260 °C разлагается на SO2, SO3, N2 и Н2О. При комнатной температуре сульфаминовая кислота практически не подвергается гидролизу, при повышенных температурах гидролизуется до NH4HSO4 (в кислой среде скорость гидролиза увеличивается). С металлами, их оксидами, гидроксидами и карбонатами сульфаминовая кислота образует соли NH2SO3M (сульфаматы), с тионилхлоридом — сульфамоилхлорид NH2SO2Cl. При взаимодействии с HNO2 подвергается окислительному дезаминированию:
Последнюю реакцию используют для количественного определения сульфаминовой кислоты и для разложения избытка HNO2 в производстве азокрасителей.
Хлор, бром, хлораты, КМnО4 и азотная кислота окисляют сульфаминовую кислоту до H2SO4 и N2 (продуктом реакции с HNO3 является N2O). Реакция с НClО или NaClO приводит к N-хлор- или N,N-дихлорпроизводным. Реакция с Na в жидком NH3− к NaSO3NHNa, а с Na2SO4− к аддукту 6HSO3NH2·5Na2SO4·15Н2О.
Во время реакции с азотной кислотой выделяется оксид азота(I):
Сульфаминовая кислота реагирует с фенолами, первичными и вторичными спиртами, например:
Первичные, вторичные и третичные амины образуют с сульфаминовой кислотой аминосульфаматы RNH2·HOSO2NH2 (ариламиносульфаматы, как правило, неустойчивы), амиды карбоновых к-т-N-ацилсульфаматы аммония, например: .
Для идентификации сульфаминовой кислоты используют реакцию с HNO2, сплавление с бензоином и другими.
Применение
Сульфаминовую кислоту применяют для очистки промышленных аппаратов и оборудования (входит в состав антинакипинов), для введения групп SO3H и NHSO3H в органических соединениях, в качестве стандартного вещества в ацидиметрии, для определения нитрит-ионов. Сульфамат аммония NH2SO3NH4 применяют для придания огнезащитных свойств текстильным материалам, сульфамат никеля (NH2SO3)2Ni — как компонент электролитов для никелирования, N-хлорпроизводные сульфаминовой кислоты в качестве дезинфицирующих средств. Соли циклогексилсульфаминовой кислоты C6H11NHSO3M (цикламаты, например где М это Na или К) производились в США как малокалорийные заменители сахара, однако из-за канцерогенных свойств их производство запрещено.
Опасность применения

Сульфаминовая кислота вызывает ожоги кожных покровов и слизистых оболочек. ЛД50 1600 мг/кг (крысы), 3100 мг/кг (мыши). Обладает значительно меньшей коррозионной активностью, чем соляная и серная кислоты.
Литература
- Лидин Р. А., Андреева Л. Л., Молочко В. А. Химические свойства неорганических веществ: Учеб. пособие для вузов — 3-е изд., испр — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.