Бензоин
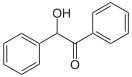
Бензои́н — органическое соединение с формулой PhCH(OH)C(O)Ph. Это гидроксикетон с двумя фенильными группами. Он представляет собой белесые кристаллы с легким запахом камфоры. Бензоин синтезируется из бензальдегида посредством бензоиновой конденсации. Он обладает хиральностью и существует в виде пары энантиомеров: (R)-бензоин и (S)-бензоин.
| Бензоин | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
2-гидрокси-1,2-дифенилэтан-1-он | ||
| Традиционные названия |
2-гидрокси-2-фенилацетонон 2-гидрокси-1,2-дифенилэтанон Дезиловый спирт Горькое миндальное масло камфоры |
||
| Хим. формула | C14H12O2 | ||
| Физические свойства | |||
| Состояние | белесые кристаллы | ||
| Молярная масса | 212.25 г/моль | ||
| Плотность | 1.31 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 132-137 °C | ||
| • кипения | 344 °C | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | малорастворимо | ||
| • в этаноле | малорастворимо | ||
| • в спиртах | Растворяется | ||
| • в эфирах | малорастворимо | ||
| • в хлоре | растворяется | ||
| Классификация | |||
| Рег. номер CAS | 119-53-9 | ||
| PubChem | 8400 | ||
| Рег. номер EINECS | 204-331-3 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 17682 | ||
| ChemSpider | 8093 | ||
| Безопасность | |||
| ЛД50 | 10.000 мг/кг | ||
| Меры предостор. (P) | R36/38 [1] | ||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Бензоин не входит в состав бензойной смолы которую получают из бензоинового дерева (Стиракс) или бензойной настойки. Основным компонентом этих натуральных продуктов является бензойная кислота.
История
Бензоин впервые описан в 1832 году Юстусом фон Либихом и Фридрихом Вёлером в ходе своих исследований масла горького миндаля, которое представляет собой бензальдегид со следами синильной кислоты[2]. Во время своей работы с Либихом Николай Зинин усовершенствовал каталитическую бензоиновую конденсацию[3][4].
Применение
Основным направлением использования бензоина являются синтез бензила, используемого в качестве фотоинициатора[5]. Преобразование происходит путем органического окисления с помощью меди(II)[6], азотной кислоты, или пероксимоносульфата калия. В одном исследовании, эта реакция осуществляется кислородом воздуха и оксидом алюминия в дихлорметане[7].
Получение
Бензоин получают из бензальдегида посредством бензоиновой конденсации[6].
Примечания
- Wöhler, Liebig; Wöhler, Liebig. Untersuchungen über das Radikal der Benzoesäure (нем.) // Annalen der Pharmacie : magazin. — 1832. — Bd. 3, Nr. 3. — S. 249—282. — doi:10.1002/jlac.18320030302.
- N. Zinin; N. Zinin. Beiträge zur Kenntniss einiger Verbindungen aus der Benzoylreihe (нем.) // Annalen der Pharmacie : magazin. — 1839. — Bd. 31, Nr. 3. — S. 329—332. — doi:10.1002/jlac.18390310312.
- N. Zinin; N. Zinin. Ueber einige Zersetzungsprodukte des Bittermandelöls (нем.) // Annalen der Pharmacie : magazin. — 1840. — Bd. 34, Nr. 2. — S. 186—192. — doi:10.1002/jlac.18400340205.
- Hardo Siegel, Manfred Eggersdorfer «Ketones» in Ullmann’s Encyclopedia of Industrial Chemistry Wiley-VCH, 2002 by Wiley-VCH, Wienheim. doi:10.1002/14356007.a15_077
- Clarke, H. T. & Dreger.E. E. (1941), Benzil, Org. Synth., <http://www.orgsyn.org/orgsyn/orgsyn/prepContent.asp?prep=cv1p0087>; Coll. Vol. Т. 1: 87
- Konstantinos Skobridis. A very simple and chemoselective air oxidation of benzoins to benzils using alumina (англ.) // Arkivoc : journal. — 2006. — Vol. 06—1798JP. — P. 102—106. Архивировано 26 марта 2020 года.
Ссылки
- Benzoin synthesis, Organic Syntheses, Coll. Vol. 1, p. 94 (1941); Vol. 1, p. 33 (1921)