Гидрид натрия
Гидри́д на́трия — сложное неорганическое вещество с химической формулой NaH. Представляет собой белый порошок, реагирует с водой; ядовит.
| Гидрид натрия | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Гидрид натрия |
| Традиционные названия | Гидрид натрия; водородистый натрий |
| Хим. формула | NaH |
| Рац. формула | NaH |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 23,99777 г/моль |
| Плотность | 1.396 (20 °C) |
| Термические свойства | |
| Температура | |
| • плавления | 800 °C |
| • разложения | 300 °C |
| Энтальпия | |
| • образования | -56,4 кДж/моль |
| Классификация | |
| Рег. номер CAS | 7646-69-7 |
| PubChem | 24758 |
| Рег. номер EINECS | 231-587-3 |
| SMILES | |
| InChI | |
| ChemSpider | 23144 |
| Безопасность | |
| Предельная концентрация | 0,5 мг/м³ |
| ЛД50 | 40-149 мг/кг (крысы, внутривенно) |
| Токсичность | высокая |
| Пиктограммы ECB |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Описание
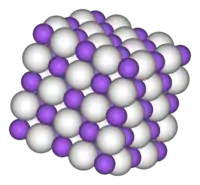
При стандартных условиях гидрид натрия представляет собой бесцветные кубические кристаллы с кристаллической решёткой типа . Является сильным восстановителем. Воспламеняется в атмосфере некоторых галогенов: фтора, хлора, а также при 230 °C в кислороде. При нагревании до 300 °C в вакууме гидрид натрия разлагается. Реагирует с водой, спиртами, жидким аммиаком, ацетиленом, трифторидом бора, оксидом углерода (IV).
Химические свойства
1. Бурное взаимодействие с водой с образованием щёлочи — гидроксида натрия:
2. Разложение при сильном нагревании в вакууме:
Сферы применения
Гидрид натрия применяют для очистки железа от магнетита. В органической химии он используется в качестве конденсирующего и полимеризующего агента. Раствор в гидроксиде натрия применяют для снятия окалины с тугоплавких металлов и специальных сталей.
Биологическое действие
Вещество токсично. При контакте гидрида натрия с водой может образоваться натриевая щёлочь (едкий натр).
ПДК в воде — 200 мг/дм³ (по ионам натрия), 2-й класс опасности в соответствии с гигиеническими нормативами.
При контакте со слизистыми оболочками гидрид натрия может вызвать щелочной ожог; коррозионно-активен.
Примечания
- Pradyot Patnaik. Handbook of Inorganic Chemicals. — McGraw-Hill, 2003. — С. 850. — 1086 с. — ISBN 0-07-049439-8.
