Амид натрия
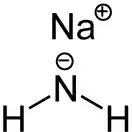
Ами́д на́трия — неорганическое вещество с формулой NaNH2, производное аммиака. Представляет собой твёрдое вещество, которое реагирует с водой. Применяется в органическом синтезе.
| Амид натрия | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Амид натрия | ||
| Хим. формула | NaNH2 | ||
| Рац. формула | NaNH2 | ||
| Физические свойства | |||
| Состояние | твёрдое | ||
| Молярная масса | 39,01244 г/моль | ||
| Плотность | 1.37 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 210 °C | ||
| • кипения | 400 °C | ||
| • разложения | 500 °C | ||
| Уд. теплоёмк. | 66,15 Дж/(кг·К) | ||
| Энтальпия | |||
| • образования | -118,8 кДж/моль | ||
| Классификация | |||
| Рег. номер CAS | 7782-92-5 | ||
| PubChem | 24533 | ||
| Рег. номер EINECS | 231-971-0 | ||
| SMILES | |||
| InChI | |||
| Номер ООН | 1390 | ||
| ChemSpider | 22940 и 21111834 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Описание
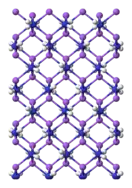
Амид натрия NaNH2 представляет собой белое кристаллическое вещество. Технические образцы имеют серый цвет из-за присутствия небольших количеств металлического железа, оставшихся от производственного процесса. Амид натрия является неустойчивым веществом, сильным восстановителем и водоотнимающим веществом. При работе с амидом натрия следует проявлять осторожность.
Получение
- Реакция гидрида натрия с аммиаком при температуре 350 °C:
- Реакция оксида натрия с жидким аммиаком при температуре −50 °C:
Применение
Амид натрия NaNH2 применяется при синтезах цианида натрия NaCN, индиго C16H10N2O2, сульфидина, витамина А и других веществ. Также его применяют для синтеза азидов: NaNH2 + N2O → NaN3 + H2O.
Примечания
Литература
- Ахметов Н. С. Общая и неорганическая химия. — М.: Высшая школа, 2001.
- Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия. — М.: Химия, 1994.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.