Ядерные спеклы
Я́дерные спе́клы, или спе́клы, или B-снурпосо́мы, или компа́ртменты фа́кторов спла́йсинга, или доме́ны SC-35, или кла́стеры интерхромати́новых гра́нул[1] (англ. nuclear speckles) — ядерные тельца, регулирующие сплайсинг. В ядерных спеклах находятся факторы сплайсинга и малые ядерные рибонуклеопротеины. Изменения в белковом составе и функционировании ядерных спекл приводят к изменениям в альтернативном сплайсинге пре-мРНК, поэтому считается, что ключевой функцией ядерных спекл является регуляция доступности факторов сплайсинга в сайтах транскрипции. Недавние исследования показали, что в ядерных спеклах также находятся белки, задействованные в регуляции локализации хромосом, модификации хроматина, транскрипции, процессинге 3'-концов транскриптов, модификации мРНК, белки, полностью покрывающие мРНК, и мРНК-рибонуклеопротеины, поэтому ядерные спеклы рассматриваются как крупнейшие центры регуляции всех этапов экспрессии ядерных генов[1].
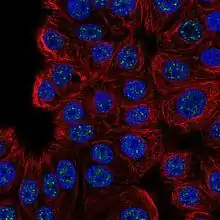
Структура и белковый состав
В интерфазных ядрах клеток человека содержится от 20 до 50 ядерных спекл, имеющих диаметр в несколько мкм. Одна ядерная спекла состоит из интерхроматиновых гранул диаметром 20—25 нм, которые соединяются фибриллами и формируют кластер — ядерную спеклу. Размер и форма ядерных спекл может значительно меняться и отличаться в клетках разных типов. На размер и форму спекл оказывают влияние множество факторов, в числе которых уровень АТФ в клетке, фосфорилирование/дефосфорилирование различных белков, транскрипция генов, активируемых стрессом, ремоделирование хроматина комплексом SWI/SNF, а также транскрипция, опосредуемая РНК-полимеразой II[1].
Распределение белков в ядерных спеклах неравномерно. Так, SRSF2 локализуется в центре спекл, а длинная некодирующая РНК MALAT1 и малые ядерные РНК находятся на периферии. Показано, что размер спекл зависит от содержания РНК в них[2].
По биофизическим свойствам ядерные спеклы и нуклеоплазма не имеют значительных различий, однако ядерные спеклы слегка плотнее окружающей их нуклеоплазмы. Сборка и стабильность ядерных спекл зависит от взаимодействий их белковых компонентов. Многие белки спекл имеют очень гибкие участки низкой сложности (то есть не имеющие выраженной пространственной структуры), которые играют важную роль в белок-белковых взаимодействиях и взаимодействиях белков с РНК. Они также играют важную роль в разделении фаз на границе жидкость-жидкость — ещё одном механизме, который обеспечивает целостность ядерных спекл. На разделение фаз на границе спекл и нуклеоплазмы влияют температура, pH, ионная сила и посттрансляционные модификации белков с участками низкой сложности. Цепочки повторяющихся аминокислот, например, пять или более последовательно соединённых остатков гистидина, служат сигналами локализации в ядерных спеклах[1].
В течение интерфазы ядерные спеклы очень стабильны. Разрушение ядерной оболочки в ходе митоза запускает разборку ядерных спекл, в результате которой белки спекл оказываются в цитоплазме. Там они собираются в так называемые митотические интерхроматиновые гранулы, которые можно видеть в метафазе, анафазе и телофазе. После того как в дочерней клетке восстановится ядерная оболочка, большинство факторов сплайсинга покидают митотические интерхроматиновые гранулы и в течение 10 минут перемещаются в ядро, однако некоторые факторы (например, SRSF2) могут оставаться в цитоплазме до G1-фазы. Когда начинается транскрипция, к новообразованным транскриптам привлекаются факторы сплайсинга и процессинга РНК, что приводит к нуклеации ядерных спекл вблизи сайтов активной транскрипции. Возможно, поведение ядерных спекл в клеточном цикле регулируется циклинами, потому что единственным неподвижным белком в интерфазных спеклах является циклин L1[1].
Как и другие ядерные тельца, ядерные спеклы постоянно динамически обмениваются белковыми молекулами с нуклеоплазмой. Например, сплайсосомные рибонуклеопротеины собираются в тельцах Кахаля до перемещения в спеклы; кроме того, они регулируют созревание 3'-концов гистоновых транскриптов в тельцах гистоновых локусов. В ядерных спеклах можно обнаружить белки параспекл PSF и PSP2, и часто спеклы и параспеклы располагаются близко друг к другу. Белок Pat1b локализуется в ядерных спеклах и PML-тельцах. Однако функциональное значение столь тесных связей между ядерными тельцами ещё нужно установить[1].
В ядерных спеклах происходят многие посттрансляционные модификации белков, такие как фосфорилирование, метилирование, ацетилирование, убиквитинилирование и SUMO-илирование. В спеклах были обнаружены 31 протеинкиназа, и обратимое фосфорилирование играет важную роль в внутриклеточной локализации белков спекл, например, факторов сплайсинга, обогащённых аргинином и серином (SRSFs). Фосфорилирование и дефосфорилирование этих белков влияют на сплайсинг и сборку белков в спеклах[1].
Ядерные спеклы тесно связаны с сигнальными путями, включающими производные фосфоинозитола (PIs). Многие белки спекл могут непосредственно с ними связываться, другие регулируются PIs косвенно через активность PI-зависимых белков, а именно, протеинкиназ и убиквитинлигаз. Существуют также прямые указания на то, что PIs сами локализуются в ядерных спеклах. Они могут оказывать значительное влияние на ядерные спеклы, поскольку регулируемые ими сигнальные белки чрезвычайно многофункциональны, как, например, некоторые протеинкиназы, локализующиеся в спеклах[1].
В ядерных спеклах были обнаружены некоторые белки цитоскелета. Перестройки цитоскелета находятся под контролем белков спекл, участвующих в сигнальных путях PI (PIP5K1A, INPPL1, PDLIM7/ENIGMA и профилин-1) и кальция (L-пластин, PTK2B и EPB41). Цитоскелетные белки могут регулировать не только сборку ядра, но и транскрипцию. Полимеризация актина имеет важное значение для ядерного транспорта и транскрипции, поскольку перестройки ядерных спекл при подавлении РНК-полимеразы II и привлечение РНК-полимеразы II к активированным промоторам зависят от полимеризации актина. В ядерных спеклах, кроме того, накапливается мономерный актин[1].
Значительная доля белков ядерных спекл подвергается ковалентному присоединению убиквитина или подобных ему белков, таких как SUMO1, ISG15 и UBL5. При этом деубиквитинирующие ферменты в спеклах обнаружены не были. Присоединение SUMO-1 служит типичным сигналом, привлекающим белки в ядерные спеклы[1].
В ядерных спеклах были обнаружены молекулы РНК, в том числе поли(А)-содержащие РНК и разнообразные некодирующие РНК. Накопление мРНК в спеклах зависит от ядерного экспорта, поскольку при отключении этого процесса в спеклах накапливается значительное количество мРНК. Некоторые исследования показали, что в ядерных спеклах может идти и сам сплайсинг, однако это утверждение требует дополнительной проверки. К некодирующим РНК, накапливающимся в спеклах, относятся малые ядерные РНК, 7SK РНК и длинная некодирующая РНК MALAT1. Эта РНК стабилизируется не поли(А)-хвостом, а при помощи консервативной триспиральной структуры, и накапливается в ядре. Она взаимодействует с некоторыми SRSFs и малой ядерной РНК U1. MALAT1 влияет на альтернативный сплайсинг, регулируя фосфорилирование и распределение по ядру факторов сплайсинга. Однако было показано, что MALAT1 не является жизненно необходимой для нормального развития у мышей[1].
Функции
Более половины белков ядерных спекл задействованы в регуляции транскрипции и сплайсинга. Спеклы формируются в непосредственной близости от сайтов транскрипции, опосредуемой РНК-полимеразой II, и даже содержат несколько её субъединиц. Многие белки спекл регулируют элонгацию транскрипции, например, элонгин (фактор элонгации транскрипции SIII) и TRIM28. В спеклах можно найти белки, регулирующие активность РНК-полимеразы II, и белки, вовлечённые в репарацию ДНК. Показана роль ядерных спекл в пространственной организации транскрипционно активного хроматина. Многие белки спекл задействованы в эпигенетической регуляции экспрессии генов, например, в спеклах были выявлены гистоны, гистонацетилтрансферазы, метилтрансферазы, деацетилазы и белок HP1, ответственный за переход эухроматина в гетерохроматин[1].
Показано участие ядерных спекл в процессинге и экспорте мРНК. В частности, спеклы играют важную роль в выборе сайта альтернативного полиаденилирования. В ядерных спеклах происходит N6-метилирование аденозина (m6A). Метилированный аденозин изменяет структуру молекулы РНК и влияет на её взаимодействие с белками, что оказывает важное влияние на метаболизм РНК. В ходе ранних этапов сплайсинга к сплайсосоме привлекается комплекс сращивания экзонов (EJC). Многие белки спекл взаимодействуют с EJC и ускоряют последующие этапы экспрессии генов, такие как сплайсинг соседних сайтов, ядерный экспорт мРНК и трансляция[1].
Клиническое значение
Изменения в структуре и функционировании ядерных спекл происходят при самых разнообразных заболеваниях. Некоторые из них, связанные непосредственно с мутациями в генах белков и РНК спекл, относительно редки. К их числу относят пигментный ретинит, мандибулофациальный дизостоз и синдром TAR[1].
Возникновение рака связано с нарушениями в альтернативном сплайсинге, которые вызваны изменениями в экспрессии генов, кодирующих факторы сплайсинга, что часто происходит в результате морфологических изменений спекл. При многих видах рака наблюдается сверхэкспрессия белков спекл, таких как SR-белки. Повышенного уровня SRSF1 достаточно для запуска развития опухоли[1].
Многие вирусы в ходе жизненного цикла используют белки клетки-хозяина, такие как белки сплайсинга и ядерного экспорта. Так, SRSFs и белки гетерогенных рибонуклеопротеинов контролируют сплайсинг РНК ВИЧ и других вирусов, влияя на трансляцию вирусных белков. В свою очередь, при вирусной инфекции меняются локализация и уровень факторов сплайсинга, в частности, они удаляются из ядерных спекл. Вирусы также используют белки, отвечающие за процессинг 3'-конца мРНК. Любопытно, что на функционирование ядерных спекл влияют даже вирусы, реплицирующиеся в цитоплазме[1].
Ядерные спеклы вовлечены в патогенез многих нейрологических заболеваний, таких как болезнь Альцгеймера, болезнь Паркинсона, лобно-височная деменция, боковой амиотрофический склероз, спинальная мышечная атрофия и шизофрения. Белки спекл вовлечены в дифференцировку нейронов и контролируют сплайсинг белков, специфичных для нейронов. Показана возможная роль ядерных спекл в заболеваниях, связанных с увеличением числа простых повторов в определённых генах[1].
Примечания
- Galganski L., Urbanek M. O., Krzyzosiak W. J. Nuclear speckles: molecular organization, biological function and role in disease. (англ.) // Nucleic Acids Research. — 2017. — 13 October (vol. 45, no. 18). — P. 10350—10368. — doi:10.1093/nar/gkx759. — PMID 28977640.
- Fei J., Jadaliha M., Harmon T. S., Li ITS, Hua B., Hao Q., Holehouse A. S., Reyer M., Sun Q., Freier S. M., Pappu R. V., Prasanth K. V., Ha T. Quantitative analysis of multilayer organization of proteins and RNA in nuclear speckles at super resolution. (англ.) // Journal Of Cell Science. — 2017. — 15 December (vol. 130, no. 24). — P. 4180—4192. — doi:10.1242/jcs.206854. — PMID 29133588.