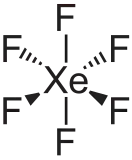Фторид ксенона(VI)
Гексафтори́д ксено́на — XeF6, бинарное неорганическое химическое соединение ксенона с фтором, представляющее собой при комнатной температуре бесцветные кристаллы. Формально является высшим фторидом ксенона. Обладает чрезвычайно высокой химической активностью, агрессивностью.
| Фторид ксенона(VI) | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
Фторид ксенона(VI) | ||
| Традиционные названия | Гексафторид ксенона | ||
| Хим. формула | XeF6 | ||
| Рац. формула | XeF6 | ||
| Физические свойства | |||
| Состояние | бесцветные кристаллы | ||
| Молярная масса | 245 г/моль | ||
| Плотность | 3,56 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 49,25 °C | ||
| • кипения | 75,6 °C | ||
| Классификация | |||
| Рег. номер CAS | 13693-09-9 | ||
| PubChem | 139546 | ||
| SMILES | |||
| InChI | |||
| ChemSpider | 123066 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Физико-химические свойства
| Свойство | Значение |
|---|---|
| Диэлектрическая проницаемость (при 55 °C) | 4,1 |
| Энтальпия образования (298К, в газовой фазе) | −277,2 кДж/моль |
| Энтропия образования (298К, в газовой фазе) | 387,242 Дж/(моль·К) |
| Теплоёмкость (298К, в газовой фазе) | 131,168 Дж/(моль·К) |
| Энтальпия плавления | 5,74 кДж/моль |
| Энтальпия возгонки | 60,8 кДж/моль |
Получение
- Обычно гексафторид получают длительным нагревом дифторида ксенона (XeF2) при 300°C под давлением 60 атм( в качестве катализатора используется фторид никеля):
- Однако известный советский учёный академик Легасов впервые в мире осуществил каталитический синтез гексафторида ксенона из простых веществ:
Строение
Исследование кристаллической структуры гексафторида ксенона заняло долгие годы, однако в результате применения современных физико-химических методов исследования удалось выявить шесть различных кристаллических модификаций. Например, при исследовании изотопно обогащённого соединения 129Xe19F6 методом 19F-ЯМР-спектроскопии было установлено, что при стандартных условиях четыре атома ксенона находятся в одинаковом электронном окружении из 24 атомов фтора.[1]
Достаточно хорошо изучены 3 кристаллические структуры вещества:
| № | Температура перехода, °C | Строение |
|---|---|---|
| 1 | >10 | Моноклинная, 8 XeF6 в ячейке |
| 2 | 10÷-25 | Орторомбическая, 16 XeF6 в ячейке |
| 3 | −25 | Моноклинная, 64 XeF6 в двойной ячейке[2] |
Химические свойства
Водой бурно гидролизуется до триоксида ксенона и плавиковой кислоты в три этапа. Все промежуточные продукты гидролиза выделены в индивидуальном состоянии:
При растворении в жидком фтороводороде происходит частичная диссоциация:
Гексафторид ксенона является достаточно сильной кислотой Льюиса. В присутствии фторид-ионов возможно протекание следующих реакций:
Например, вещество легко реагирует с фторидами щелочных металлов (кроме LiF):
Однако при нагревании таких солей выше 50 °C происходит разложение:
Соединения состава M2XeF8 достаточно устойчивы. Например, натриевое производное устойчиво до 100 °C, а цезиевое — до 400 °C.
С фторидами менее активных элементов гексафторид ксенона образует двойные соли[3], которые впервые получили ещё в 1967 году. Например, были получены 4XeF6·GeF4, 2XeF6·GeF4 и XeF6·GeF4, но получить аналогичное соединение с фторидом кремния не удалось, за счёт слабой основной функции SiF4. Вещество также взаимодействует с BF3 и AsF5 в соотношении 1:1. При этом образуются белые устойчивые кристаллы, слаболетучие при комнатной температуре (давление паров составляет около 1 мм.рт.ст). XeF6·BF3 плавится при 80 °C с образованием жёлтой вязкой жидкости.[4]
Также были сообщения о получении высшего фторида XeF8 из XeF6 и F2, однако эти данные не подтвердились. Существование октафторида ксенона не возможно из-за размера атома ксенона: атомы фтора были бы очень близко расположены относительно друг друга, и сила отталкивания одноименных зарядов была бы больше энергии связи Xe-F.
Применение
- Гексафторид ксенона — мощный фторирующий агент.
- Возможно применение в качестве окислителя ракетного топлива.
Биологическая роль и токсичность
Фторид ксенона (VI) XeF6 (гексафторид ксенона) очень ядовит, сильный окислитель. Предельно допустимая концентрация фторида ксенона (VI) составляет не более 0,05 мг/м³.
Примечания
- The structure of xenon hexafluoride in the solid state. Journal of Fluorine Chemistry Volume 127, Issue 10, Pages 1415—1422 (недоступная ссылка)
- Xenon Hexafluoride: Structural Crystallography of Tetrameric Phases R.D. Burbank, G. R. Jones. Science Vol. 171. №. 3970, pp. 485—487
- Изучение системы XeF6-GeF4 и XeF6-SiF4 (недоступная ссылка). Дата обращения: 20 августа 2008. Архивировано 4 марта 2016 года.
- Xenon Hexafluoride Complexes. Science. Vol. 144. no. 3618, p. 537
Литература
- Holleman A.F., Wiberg E. Inorganic Chemistry. Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- Некрасов Б. В. Основы общей химии. В 2-х томах., М.: Химия, 1973 г.