Реакция Кнёвенагеля
Реа́кция Кнёвена́геля — химическая реакция, заключающаяся в конденсации альдегидов или кетонов в присутствии оснований с соединениями, содержащими активные метиленовые группы.
Реакция названа в честь немецкого химика Эмиля Кнёвенагеля[1][2][3].
Механизм реакции
Данная реакция является модификацией известной реакции Перкина и имеет сходный с ней механизм. Первая часть реакции протекает по механизму нуклеофильного присоединения: основания (первичные или вторичные амины) отщепляют протон от активной метиленовой группы. Образовавшийся карбанион реагирует с карбонильной группой альдегида или кетона, в результате чего выделяется молекула воды (поэтому реакцию иногда называют «Конденсация Кнёвенагеля»)[3]. В качестве продуктов обычно образуются α,β-сопряжённые еноны.
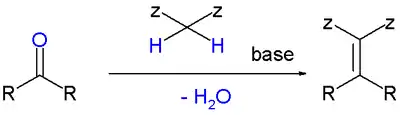
Активная метиленовая группа обычно присутствует в следующих формах[4]:
- Z-CH2-Z или Z-CHR-Z, например диэтилмалонат, кислота Мельдрума, этилацетоацетат, малоновая кислота или циануксусная кислота[5].
- Z-CHR1R2, например нитрометан.
Z — электроноакцепторная функциональная группа, достаточно сильная для облегчения депротонирования даже в присутствии слабого основания. Использование в качестве катализатора сильного основания нежелательно, поскольку это приведёт к самоконденсации альдегида или кетона.
Реакция Кнёвенагеля как промежуточный шаг входит в такие реакции как «синтез пиридина по Ганчу», «реакция Гевальда» и «синтез Файста-Бенари». Благодаря этой реакции было открыто боевое отравляющее вещество — газ Сирень.
Область применения
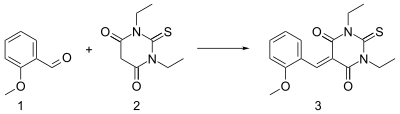
Яркий пример реакции Кнёвенагеля — реакция 2-метоксибензальдегида 1 с N',N-диэтилбарбитуровой кислотой 2 в этаноле, в присутствии пиперидина в качестве основания[6]. Образовавшийся в результате реакции енон 3 — это комплекс с переносом заряда.
Конденсация Кнёвенагеля — ключевой шаг в промышленном производстве противомалярийного препарата люмефантрина (компонент Коатрема)[7]:
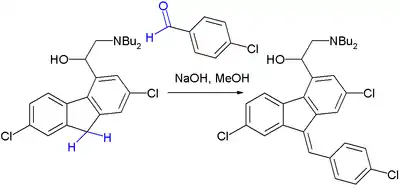
В результате реакции получается смесь E- и Z-изомеров в соотношении 50:50, но, поскольку оба изомера быстро переходят один в другой через спирт, в конечном итоге всё же удаётся получить более стабильный Z-изомер.
В качестве примера многокомпонентной реакции можно указать микроволновой синтез из циклогексанона, малононитрила и 3-aмино-1,2,4-триазола[8]:
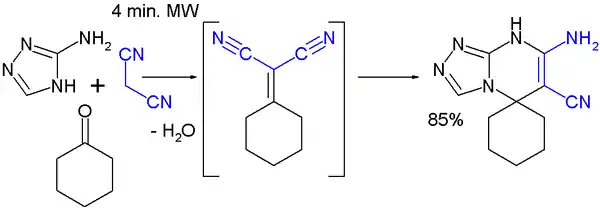
Синтез Дебнера
Синтез Дебнера является модификацией реакции Кнёвенагеля и заключается в конденсации альдегидов с малоновой кислотой в присутствии пиридина или пиперидина. В результате такой реакции происходит дополнительный шаг — декарбоксилирование[9]. Например, в результате реакции между акролеином и малоновой кислотой в присутствии пиридина образуется транс −2,4-пентадиеновая кислота у которой остаётся всего одна карбоксильная группа[10][11]:

Реакция Вейса-Кука
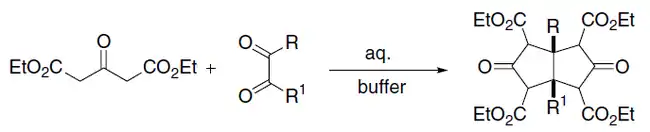
Реакция Вейса-Кука представляет собой синтез цис-бицикло[3.3.0]октан-3,7-дионов с использованием сложных эфиров ацетондикарбоновой кислоты и α-дикарбонильных соединений. Реакция происходит по тому же механизму, что и реакция Кнёвенагеля[12]:
См. также
- Альдольная конденсация
- Нитроалкен
Примечания
- Jones, G. Org. React. 1967, 15.
- Emil Knoevenagel. Condensation von Malonsäure mit Aromatiachen Aldehyden durch Ammoniak und Amine (нем.) // Berichte der deutschen chemischen Gesellschaft : magazin. — 1898. — Bd. 31, Nr. 3. — S. 2596—2619. — doi:10.1002/cber.18980310308.
- Серрей, 1962, с. 150.
- March, Jerry (1985), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (3rd ed.), New York: Wiley, ISBN 0-471-85472-7
- G. Jones. The Knoevenagel Condensation // Organic Reactions (неопр.). — 2004. — doi:10.1002/0471264180.or015.02.
- 1,3-Diethyl-5-(2-methoxybenzylidene)-2-thioxodihydropyrimidine-4,6(1H,5H)-dione Abdullah Mohamed Asiria, Khaled Ahmed Alamrya Abraham F. Jalboutb, Suhong Zhang Molbank 2004, M359 Архивная копия от 9 июля 2011 на Wayback Machine publication.
- An Improved Manufacturing Process for the Antimalaria Drug Coartem. Part II Ulrich Beutler, Peter C. Fuenfschilling, and Andreas Steinkemper Org. Process Res. Dev.; 2007; 11(3) pp. 341-45; (Article) doi:10.1021/op060244p
- Mild and ecofriendly tandem synthesis of 1,2,4-triazolo[4,3-a]pyrimidines in aqueous medium Arkivoc 2007 (06-2251BP) Anshu Dandia, Pritima Sarawgi, Kapil Arya, and Sarita Khaturia Link
- O. Doebner. Ueber die der Sorbinsäure homologen, ungesättigten Säuren mit zwei Doppelbindungen (нем.) // Berichte der deutschen chemischen Gesellschaft : magazin. — 1902. — Bd. 35. — S. 1136—1136. — doi:10.1002/cber.190203501187.
- Peter J. Jessup, C. Bruce Petty, Jan Roos, and Larry E. Overman (1988), 1-N-Acylamino-1,3-dienes from 2,4-pentadienoic acids by the curtius rearrangement: benzyl trans-1,3-butadiene-1-carbamate, Org. Synth., <http://www.orgsyn.org/orgsyn/orgsyn/prepContent.asp?prep=cv6p0095>; Coll. Vol. Т. 6: 95
- Серрей, 1962, с. 151.
- Weiss, U.; Edwards, J. M. A one-step synthesis of ketonic compounds of the pentalane, [3,3,3]- and [4,3,3]-propellane series (англ.) // Tetrahedron Letters : journal. — 1968. — Vol. 9, no. 47. — P. 4885. — doi:10.1016/S0040-4039(00)72784-5.
Литература
- А. Серрей. Справочник по органическим реакциям / пер. с англ. М. Н. Ефимова, О. Н. Камышан и Э. М. Бамдас; под редакцией и с дополнениями докт. хим. наук Н. С. Вульфсона. — 2-е издание, уточнённое и дополненное. — М.: Государственное научно-техническое издательство химической литературы, 1962. — 300 с. — 25 000 экз.