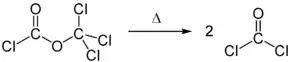Дифосген
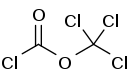
Дифосген — трихлорметиловый эфир хлормуравьиной кислоты.
| Дифосген | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
трихлорметиловый эфир хлормуравьиной кислоты | ||
| Традиционные названия | дифосген | ||
| Хим. формула | C2Cl4O2 | ||
| Рац. формула | CCl3OCOCl | ||
| Физические свойства | |||
| Состояние | жидкость | ||
| Молярная масса | 197,82 г/моль | ||
| Плотность | 1,65 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −57 °C | ||
| • кипения | 127,5 °C | ||
| Оптические свойства | |||
| Показатель преломления | 1,4566 | ||
| Классификация | |||
| Рег. номер CAS | 503-38-8 | ||
| PubChem | 10426 | ||
| Рег. номер EINECS | 207-965-9 | ||
| SMILES | |||
| InChI | |||
| RTECS | LQ7350000 | ||
| ChemSpider | 21154424 | ||
| Безопасность | |||
| Токсичность | высокотоксичен, обладает сильным удушающим действием | ||
| Пиктограммы ECB |
|
||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Свойства
Подвижная жидкость, без цвета, с характерным запахом прелого сена, на воздухе дымит. Хорошо растворим в органических растворителях (бензол, толуол, четырёххлористый углерод, ацетон), плохо растворим в воде.
Высокотоксичен, вызывает удушающее и раздражающее действие.
История
Впервые получен в 1847 году французским химиком О. Кауром. Во время Первой мировой войны в различных формах применялся обеими воюющими сторонами в качестве удушающего отравляющего вещества. Впервые был применён Германией в июле 1916 года против французских войск под Верденом.
Синтез
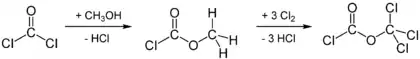
Промышленным методом синтеза дифосгена является хлорирование на свету метилхлорформиата, получаемого из фосгена и метанола:
Дифосген также может быть синтезирован радикальным хлорированием метилформиата при облучении ультрафиолетом:
 Синтез дифосгена
Синтез дифосгена
Химические свойства
При нагревании дифосген разлагается на две молекулы фосгена, этот процесс катализируется активированным углём, оксидом и хлоридом железа(III), хлоридом алюминия:
В случае использования в качестве катализатора оксида алюминия дифосген разлагается с образованием четырёххлористого углерода и диоксида углерода:
Применение
Дифосген используется в синтезе хлоркарбонатов из спиртов:
Применяется как синтетический эквивалент фосгена в синтезе органических карбонатов, изоцианатов.
Используется для получения фосгена в лабораторных условиях.
В Первой мировой войне применялся в качестве удушающего боевого отравляющего вещества.
Токсичность
Дифосген является ядом удушающего действия для человека и других животных с замедленным по времени наступлением смерти. Симптомы отравления фосгеном и дифосгеном: мучительный кашель, выделение мокроты с примесью крови, посинение кожи (цианоз), отёк лёгких. Отравление может протекать незаметно для человека, поскольку первые симптомы отравления появляются только спустя несколько часов (5-12 часов с момента начала вдыхания малых концентраций фосгена или дифосгена). Обнаружить фосген или дифосген в воздухе можно по характерному «тухлому» запаху, похожему на запах прелого сена. Табачный дым в атмосфере даже с малой примесью фосгена или дифосгена меняет свой запах и для курящего становится неприятным, что может служить простым методом определения фосгена и дифосгена в воздухе. Отравление дифосгеном может произойти при авариях на предприятиях по производству различных пластмасс.
Литература
- Александров В. Н., Емельянов В. И. Отравляющие вещества: Учебное пособие / Под ред. д-ра хим. наук, проф. Г. А. Сокольского. — 2-е изд., перераб. и доп. — М.: Воениздат, 1990. — 272 с. — 100 000 экз. — ISBN 5-203-00341-6.