м-Фенилендиамин
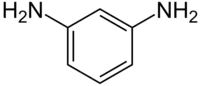
м-Фенилендиамин — органическое вещество, ароматический диамин с формулой 1,3-C6H4(NH2)2. Вещество ядовито; является метгемоглобинообразователем.
| м-Фенилендиамин[1][2] | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
1,3-фенилендиамин |
| Сокращения | MPDA |
| Традиционные названия | м-фенилендиамин |
| Хим. формула | C6H8N2 |
| Рац. формула | C6H4(NH2)2 |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 108,14 г/моль |
| Энергия ионизации | 689 кДж/моль |
| Термические свойства | |
| Температура | |
| • плавления | 62,8; 103 °C |
| • кипения | 257; 282-284; 287 °C |
| • самовоспламенения | 560 °C |
| Мол. теплоёмк. | 159,6 Дж/(моль·К) |
| Энтальпия | |
| • образования | –7,8 кДж/моль |
| Давление пара | 0,62 мм рт. ст. (100 °C) |
| Химические свойства | |
| Растворимость | |
| • в воде | 35,125 г/100 мл |
| Классификация | |
| Рег. номер CAS | 108-45-2 |
| PubChem | 24898321 |
| Рег. номер EINECS | 203-584-7 |
| SMILES | |
| InChI | |
| RTECS | SS7700000 |
| ChEBI | 8092 |
| Безопасность | |
| Предельная концентрация | 0,1 мг/м³ |
| ЛД50 | 110-149,25 мг/кг (мыши, перорально) |
| Токсичность | ирритант |
| Фразы риска (R) | R23/24/25, R36, R43, R50/53, R68 |
| Фразы безопасности (S) | S28, S36/37, S45, S60, S61 |
| Краткие характер. опасности (H) |
H301, H311, H317, H319, H331, H341, H410 |
| Меры предостор. (P) |
P261, P273, P280, P301+P310, P305+P351+P338, P311 |
| Сигнальное слово | Опасно |
| Пиктограммы СГС |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Получение и лабораторная очистка
м-Фенилендиамин производят путём каталитического гидрирования 1,3-динитробензола, который, в свою очередь получается при нитровании бензола смесью азотной и серной кислот. В качестве катализатора гидрирования выступает палладий либо никель Ренея, а реакция проводится в воде или метаноле[3].
В лаборатории м-фенилендиамин очищают перегонкой в вакууме с последующей кристаллизацией из этанола. Вещество необходимо охранять от солнечных лучей, поскольку на свету оно быстро темнеет[4].
Физические свойства
м-Фенилендиамин легко растворим в горячей воде, а также основны́х органических растворителях (спиртах, кетонах и эфирах)[3].
Химические свойства
м-Фенилендиамин проявляет свойства типичного ароматического амина, например, действует в водных растворах как основание и образует устойчивые соли. Также он может быть ацилирован хлорангидридами карбоновых кислот, а с хлорангидридами дикарбоновых кислот он образует полиамиды, используемые в промышленности для производства волокон. При обработке избытком азотистой кислоты данное соединение вступает само с собой в реакцию азосочетания, образуя краситель бисмарк коричневый. Ароматическое кольцо м-фенилендиамина может гидрироваться с образованием диаминоциклогексана[3].
Применение
Наиболее широкое применение м-фенилендиамин находит в производстве арамидного волокна поли(м-фениленизофталамида), синтезируемого по реакции с хлорангидридом изофталевой кислоты. Данный материал обладает высокой температурной устойчивостью и огнеупорностью. Также м-фенилендиамин служит исходным соединением в синтезе ряда азокрасителей[3].
Физиологическое действие
Мета-Фенилендиамин особо токсичен; относится ко второму классу опасности и в очень больших концентрациях может раздражать кожу и слизистые оболочки.
1,3-диаминобензол окисляет гемоглобин в метгемоглобин.
ПДК в рабочей зоне - 0,1 мг/м³ в соответствии с ГОСТ 12.1.007-76.
ЛД50 на мышах - около 110 мг/кг (при пероральном введении).
Примечания
- Sigma-Aldrich. m-Phenylenediamine. Дата обращения: 9 января 2014.
- Dean J. A. Lange's Handbook of Chemistry. — McGraw-Hill, 1999. — ISBN 0-07-016384-7.
- Smiley R. A. Phenylene- and Toluenediamines // Ullmann's Encyclopedia of Industrial Chemistry. — Wiley. — 2000. — doi:10.1002/14356007.a19_405.
- Amarego W. L. F., Chai C. L. L. Purification of Laboratory Chemicals. — Sixth ed. — Elsevier, 2009. — P. 329. — ISBN 978-1-85617-567-8.
Ссылки
- Sigma-Aldrich. ЯМР-спектр м-фенилендиамина. Дата обращения: 9 января 2014.
- Sigma-Aldrich. ИК-спектр м-фенилендиамина. Дата обращения: 9 января 2014.
- Sigma-Aldrich. КР-спектр м-фенилендиамина. Дата обращения: 9 января 2014.