Диэтиламин
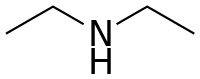
Диэтиламин (N,N-Диэтиламин, диэтамин) — органическое соединение, вторичный амин, производное аммиака, в молекуле которого два атома водорода замещены этильными радикалами.
| Диэтиламин | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
диэтиламин, N-этилэтанамин |
| Традиционные названия | диэтиламин, N,N-диэтиламин, диэтамин |
| Хим. формула | C4H11N |
| Рац. формула | (C2H5)2NH |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 73,14 г/моль |
| Плотность | 0,71 г/см³ |
| Энергия ионизации | 8,01 ± 0,01 эВ[1] |
| Термические свойства | |
| Температура | |
| • плавления | -48 °C |
| • кипения | 56,3 °C |
| • вспышки | -26 °C |
| • самовоспламенения | 310 °C |
| Пределы взрываемости | 1,8-10,1 % |
| Критическая точка | |
| • температура | 223,3 °C |
| • давление | 36,6 атм |
| Мол. теплоёмк. | 169,2 Дж/(моль·К) |
| Энтальпия | |
| • образования | -103,7 (ж) кДж/моль |
| Давление пара | 192 ± 1 мм рт.ст.[1] |
| Химические свойства | |
| Константа диссоциации кислоты | 1,17*10-11 |
| Оптические свойства | |
| Показатель преломления | 1,3864 |
| Классификация | |
| Рег. номер CAS | 109-89-7 |
| PubChem | 8021 |
| Рег. номер EINECS | 203-716-3 |
| SMILES | |
| InChI | |
| RTECS | HZ8750000 |
| ChEBI | 85259 |
| Номер ООН | 1154 |
| ChemSpider | 7730 |
| Безопасность | |
| Предельная концентрация | 30 мг/м³ |
| ЛД50 | 450-500 (крысы, внутрижелудочно) |
| Токсичность | ирритант, среднетоксичен. |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Получение
В промышленности получают взаимодействием этанола с аммиаком (при 350-450 °C и катализе Al2O3, SiO2) или с аммиаком в присутствии водорода (при 150-230 °C и катализе Ni, Co, Cu, Re). Также диэтиламин получают взаимодействием диэтилового эфира с аммиаком, восстановительным аминированием ацетальдегида и этилированием аммиака этилхлоридом:
2C2H5Cl + 3NH3 → (C2H5)2NH + 2NH4Cl
В лаборатории диэтиламин получают разложением 4-нитрозо-N,N-диэтиланилина щелочью[2].
Физические свойства
Бесцветная жидкость со специфическим запахом: аммиачным с небольшой примесью рыбного. Смешивается с водой, растворим в ацетоне, этаноле, диэтиловом эфире.
При атмосферном давлении не образует азеотропных смесей с водой, метанолом и этанолом.
Химические свойства
Как и другие замещённые амины, обладает основными свойствами — реагирует с кислотами с образованием солей диэтиламмония:
(C2H5)2NH + HCl → (C2H5)2NH2Cl.
Нитрозируется азотистой кислотой до N-нитрозодиэтиламина:
(C2H5)2NH + HNO2 → (C2H5)2N-NO + H2O
Ацилируется хлорангидридами и ангидридами карбоновых кислот до N,N-диэтиламидов.
Алкилируется алкилгалогенидами, диметилсульфатом.
С сероуглеродом в щелочной среде дает N,N-диэтилдитиокарбаматы:
(C2H5)2NH + CS2 + KOH → (C2H5)2NC(S)SK + H2O
При взаимодействии с сильными основаниями, отщепляя протон у атома азота, образует соли в роли кислоты. Например, получение ЛДА по реакции с бутиллитием.
(C2H5)2NH + LiC4H9 → (C2H5)2NLi + C4H10
Применение
Для получения присадок к моторным топливам и маслам, отвердителей эпоксидных смол, ускорителей вулканизации, красителей, флотореагентов, репеллентов (например, диэтилтолуамида), пестицидов, лекарственных средств (например, кордиамина, новокаина), ингибиторов коррозии (например, N,N-диэтилмочевина, динитробензоат диэтиламмония). Также используется для получения LSD-25, в смеси с лизергиновой кислотой образуя диэтиламид d-лизергиновой кислоты.
28 февраля 2020 года неформальный союз стран, способствующих контролю за нераспространением химического оружия, Австралийская группа, добавил в свой список прекурсоров химического оружия[3] 22 вещества с идентификаторами AG66 — AG87, которые могут использоваться для синтеза отравляющего вещества «Новичок». Диэтиламин включён в список прекурсоров под номером AG64. Хотя Россия не является членом Австралийской группы, одновременно с «Новичками» диэтиламин также был включён в список веществ подлежащих экспортному контролю[4].
Безопасность
Токсичность
Диэтиламин — токсичное вещество. В соответствии с ГОСТ 12.1.007-76 диэтиламин является токсичным малоопасным веществом по степени воздействия на организм, 4-го класса опасности[5]. В больших концентрациях N,N-диэтиламин раздражает слизистые оболочки верхних дыхательных путей и глаз, обладает удушающим действием. ПДК 30 мг/м3[6][7].
Симптомы отравления у животных: раздражение слизистых верхних дыхательных путей и глаз, возбуждение ЦНС с последующим угнетением, тремор, судороги, смерть при явлениях асфиксии. После 1-ч ингаляции при 500—1000 мг/м3 у крыс нарушения условных и безусловных рефлексов на протяжении месяца, при 300 мг/м3 — кратковременные нарушения. Макроскопически: отек легких, полнокровие внутренних органов; гистологических: резко выраженная клеточная дистрофия и некробиотические изменения в печени (Васильева).
Пожароопасность
Горюч. Температура самовоспламенения 490 °C. Концентрационные пределы воспламенения 2,2-14 объёмных %.
Примечания
- http://www.cdc.gov/niosh/npg/npgd0209.html
- Голодников Г.В., Мандельштам Т.В. Практикум по органическому синтезу. - Л.: ИЛУ, 1976 стр. 92-93
- Australia Group Chemical Weapons Precursors List. costanziresearch.com.
- Указ Президента Российской федерации № 760. Официальный интернет-портал правовой информации (7 декабря 2020). Дата обращения: 7 декабря 2020.
- name=https://docs.cntd.ru_ГОСТ(недоступная+ссылка) 12.1.005-76. Воздух рабочей зоны. Общие санитарно-гигиенические требования
- name=https://docs.cntd.ru_Diethylamine
- name=https://docs.cntd.ru_ГОСТ(недоступная+ссылка) 12.1.007-76. ССБТ. Вредные вещества. Классификация и общие требования
Литература
- Вредные химические вещества: Азотсодержащие органические соединения. — Под общей редакцией Курляндского Б. А., Филова В. А. — СПб.: Химия, 1992. — С. 35
- Рабинович В. А., Хавин З. Я. Краткий химический справочник. — Л.: Химия, 1977. — С. 148
- Химическая энциклопедия. — Т.5. — М.: Советская энциклопедия, 1999. — С. 493—494
См. также
- Этиламин
- Триэтиламин
