Аденоассоциированный вирус
Аденоассоциированный вирус (англ. Adeno-associated dependoparvovirus A, AAV) — малый вирус, инфицирующий клетки человека и некоторых других приматов. Аденоассоциированный вирус, по-видимому, не вызывает заболевания у человека и, соответственно, вызывает слабый иммунный ответ.
| Аденоассоциированный вирус | ||||||||
|---|---|---|---|---|---|---|---|---|
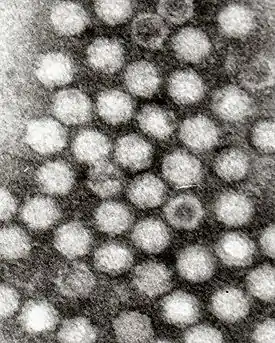 Аденоассоциированные вирусы | ||||||||
| Научная классификация | ||||||||
|
Реалм: Царство: Shotokuvirae Тип: Cossaviricota Класс: Quintoviricetes Порядок: Piccovirales Семейство: Подсемейство: Parvovirinae Род: Dependoparvovirus Вид: Аденоассоциированный вирус |
||||||||
| Международное научное название | ||||||||
| Adeno-associated dependoparvovirus A | ||||||||
| Синонимы | ||||||||
| Группа по Балтимору | ||||||||
| II: оцДНК-вирусы | ||||||||
| ||||||||
Аденоассоциированный вирус может инфицировать делящиеся и неделящиеся клетки и может встраивать свой геном в геном хозяина. Эти особенности делают AAV особенно привлекательным кандидатом для создания вирусных векторов для генной терапии[4].
Аденоассоциированный вирус принадлежит к роду Dependoparvovirus семейства парвовирусов (Parvoviridae). Вирус имеет небольшие размеры (20 нм), не имеет липидной оболочки и не кодирует собственных ферментов репликации.
История
В 1965 году Роберт Атчисон опубликовал статью, в которой был описан новый вирус, названный аденоассоциированным вирусом[5]. Вирусные частицы были обнаружены при помощи электронной микроскопии в препаратах аденовируса обезьян, которые были несколько раз пересажены на первичных культурах клеток почки макаки резус. Группой Атчисона частицы нового вируса диаметром 24 нм были отделены от более крупных частиц аденовируса диаметром 80 нм при помощи ультрафильтрации[6].
После выделения было показано, что частично очищенные вирионы аденоассоциированного вируса не могут самостоятельно реплицироваться, однако могут реплицироваться и распространяться в культурах, заражённых аденовирусом. Таким образом, аденоассоциированный вирус оказался дефектным вирусом-спутником, нуждающимся во вспомогательном вирусе для полноценной репликации. Так как аденоассоциированной вирус не кодирует собственной ДНК-полимеразы, для размножения ему требуется вспомогательный вирус, как правило, аденовирус[7].
В июле 2013 года в результате ревизии семейства 4 близких вида объединили в один, сменив название рода на Dependoparvovirus, а вида — на Adeno-associated dependoparvovirus A[3].
Вектор для генной терапии
Преимущества и недостатки
Аденоассоциированный вирус дикого типа имеет некоторые преимущества для генной терапии. Одним из основных преимуществ является то, что этот вирус не является патогенным. Аденоассоциированный вирус может инфицировать неделящиеся клетки и может встраиваться в геном хозяина по специфическим участкам (AAVS1) девятнадцатой хромосомы[8].
Данная особенность делает аденоассоциированный вирус более предсказуемым, чем ретровирусы. Ретровирусы являются потенциально опасными как мутагены, так как встраиваются в геном хозяина случайным образом, что может привести к возникновению раковых опухолей. Геном аденоассоциированного вируса обычно встраивается по специфическому сайту, а случайные встраивания происходят с ничтожной частотой. При создании векторов для генной терапии на основе аденоассоциированного вируса из ДНК вируса удаляют гены rep и cap. Нужный ген вместе с промотором встраивают между инвертированными концевыми повторами (англ. inverted terminal repeats, ITR)), в результате чего в ядре после синтеза клеточной ДНК-полимеразой второй цепочки ДНК образуются конкатемеры. Векторы для генной терапии на основе аденоассоциированных вирусов образуют эписомальные конкатемеры в ядре клетки хозяина. В неделящихся клетках данные конкатамеры остаются интактными, в делящихся клетках ДНК аденоассоциированного вируса теряется при делениях клетки, так как эписомальная ДНК не реплицируется при репликации ДНК клетки хозяина. Случайное встраивание ДНК аденоассоциированного вируса в геном хозяина происходит весьма редко. Аденоассоциированный вирус также обладает очень низкой иммуногенностью, по-видимому, ограниченной низкой эффективностью образования нейтрализующих антител, в то время как для последних чётко не показана цитотоксичность[9][10][11]. Описанные особенности, а также возможность заражать неделящиеся клетки, обуславливает преимущества аденоассоциированного вируса над аденовирусами для генной терапии.
Использование аденоассоциированного вируса имеет также и некоторые недостатки. Ёмкость генома вируса, доступная для клонирования терапевтических генов, составляет всего около 4800 пар нуклеотидов. Таким образом, данный вектор не подходит для клонирования крупных генов. Инвертированные концевые повторы двух геномов могут гибридизоваться и образовывать конкатемеры голова-хвост, практически удваивая ёмкость вектора.
Инфекция вирусом дикого типа часто вызывает активацию гуморального иммунитета. Активность нейтрализующих антител в некоторых случаях снижает применимость серотипа AAV2. AAV2 может проникать и в мозг и является строго специфичным к нейронам.
Клинические испытания
В настоящий момент препараты (векторы) на основе аденоассоциированного вируса для лечения муковисцидоза и гемофилии проходят первый этап клинических испытаний. Многообещающие результаты были получены после первой фазы клинических испытаний препаратов против болезни Паркинсона. По результатам других клинических испытаний показана безопасность векторов на основе аденоассоциированного вируса при болезни Канавана, мышечной дистрофии и при синдроме Бильшовского-Янского.
| Заболевание | Ген | Способ введения | Фаза испытаний | Количество испытуемых | Статус |
|---|---|---|---|---|---|
| Муковисцидоз | CFTR | Легкие, аэрозоль | I | 12 | Завершены |
| CFTR | Легкие, аэрозоль | II | 38 | Завершены | |
| CFTR | Легкие, аэрозоль | II | 100 | Завершены | |
| Гемофилия B | FIX | Внутримышечено | I | 9 | Завершены |
| FIX | Печеночная артерия | I | 6 | Закончены | |
| Артрит | TNFR:Fc | Внутрисуставно | I | 1 | Продолжаются |
| Наследственная эмфизема | AAT | Внутримышечено | I | 12 | Продолжаются |
| Мышечная дистрофия | Саркогликан | Внутримышечено | I | 10 | Продолжаются |
| Болезнь Паркинсона | GAD65, GAD67 | Внутрь черепа | I | 12 | Завершены[13] |
| Болезнь Канавана | AAC | Внутрь черепа | I | 21 | Продолжаются |
| Болезнь Баттена | CLN2 | Внутрь черепа | I | 10 | Продолжаются |
| Синдром Альцгеймера | NGF | Внутрь черепа | I | 6 | Продолжаются |
| Спинальная мышечная атрофия | SMN1 | интратекально | I–III | 15 | Несколько испытаний завершено, несколько продолжается (Zolgensma) |
Клинические испытания для лечения рака простаты находятся на 2005 год в третьей стадии[12], однако, эти исследования ex vivo не включают прямого назначения аденоассоциированного вируса пациентам.
Патология
Считается, что аденоассоциированный вирус не вызывает заболеваний человека. Однако показано, что данный вирус является фактором риска развития мужского бесплодия[14]. Геномную ДНК аденоассоциированных вирусов обнаруживают в образцах спермы с нарушениями структуры и функции сперматозоидов. Однако, не выявлено прямой связи между данной инфекцией и мужским бесплодием.
Роль в развитии гепатоцеллюлярной карциномы
По результатам недавних исследований больных с редкими формами гепатоцеллюлярной карциномы, высказывается предположение, что вирус AAV2 может играть роль в пусковых механизмах развития этого вида рака. Поскольку мишенью вируса AAV2 являются гены, играющие важную роль в размножении клеток, исследователи полагают, что инфицирование приводит к их чрезмерной активации, в результате чего запускается опухолевый рост. Это открытие ставит под сомнение безопасность использования вирусов AAV2 для генной терапии[15].
Структура
Геном, транскриптом и протеом
Геном аденоассоциированного вируса содержит (+ или -) одноцепочечную ДНК (ssDNA) длиной около 4,7 тысяч нуклеотидов. На концах молекулы геномной ДНК располагаются инвертированные концевые повторы (англ. inverted terminal repeats, ITRs). Геном содержит две открытые рамки считывания (англ. ORF): rep и cap. Первая содержит четыре перекрывающихся гена, кодирующих белки Rep, которые необходимы для жизненного цикла вируса, вторая рамка считывания содержит перекрывающиеся нуклеотидные последовательности белков капсида: VP1, VP2 и VP3, которые формируют икосаэдрическую головку капсида[16].
Инвертированные концевые повторы
Последовательность инвертированных концевых повторов (англ. Inverted Terminal Repeat, ITR) составляет 145 нуклеотидов. ITR располагаются симметрично в геноме аденоассоциированных вирусов и необходимы для репликации геномной ДНК[17]. Другим из свойств ITR является способность образовывать шпильки, что обеспечивает возможность синтеза второй цепочки ДНК без участия праймазы. Инвертированные концевые повторы также требуются для интеграции ДНК вируса в специфический участок девятнадцатой хромосомы человека и для освобождения ДНК провируса из хромосомы[18][19], а также для образования комплексов ДНК аденоассоциированного вируса с белками оболочки, устойчивых к действию дезоксирибонуклеазы[20].
В случае генной терапии в цис-положении после терапевтического гена должен находиться ITR. Эту закономерность используют при получении рекомбинантных векторов на основе аденоассоциированного вируса (англ. recombinant AAV, rAAV), содержащих репортёрные или терапевтические гены. Показано, что ITR не требуются в цис-положении для осуществления репликации и укладки в капсид. В составе последовательности нуклеотидов гена rep обнаружен Rep-зависимый элемент, действующий в cis-положении (англ. cis-acting Rep-dependent element, CARE). В цис-положении CARE усиливает репликацию и сборку вирусных частиц[21][22][23][24].
Гены и белки rep
«Левая сторона генома» содержит два промотора — p5 и p19, с которых транскрибируются две перекрывающихся мРНК различной длины. Каждый ген, кодирующий соответствующую мРНК содержит интрон, который может быть вырезан в процессе сплайсинга. В результате этого могут синтезироваться четыре различных мРНК, и, соответственно, четыре различных белка Rep с перекрывающимися последовательностями. Белки названы в соответствии с их молекулярными массами в кДа: Rep78, Rep68, Rep52 и Rep40[25]. Rep78 и 68 специфически связывают в качестве праймера шпильку, которую образуют инвертированные концевые повторы и затем разрезают её по сайту концевого разрешения (англ. terminal resolution site). Было показано, что Rep78 и 68 необходимы для специфической интеграции ДНК аденоассоциированного вируса в геном хозяина. Четыре белка Rep связывают АТР и обладают хеликазной активностью. Данные белки усиливают транскрипцию с промотора p40, но ослабляют транскрипцию с промоторов p5 и p19[19][25][26][27][28][29].
Гены cap и белки VP
«Правая часть» (+)-цепи геномной ДНК аденоассоциированного вируса содержит перекрывающиеся последовательности, кодирующие три белка капсида — VP1, VP2 и VP3. Транскрипция этих генов начинается с одного промотора, p40. Молекулярная масса соответствующих белков составляет 87, 72 и 62 кДа, соответственно[30]. Все три белка транслируются с одной мРНК. После транскрипции пре-мРНК может подвергаться сплайсингу двумя разными способами, при этом вырезается более длинный или более короткий интрон и образуются мРНК длиной 2300 или 2600 нуклеотидов. Обычно, особенно в присутствии аденовируса, вырезается более длинный интрон. В такой форме вырезается первый стартовый кодон AUG, с которого начинается синтез белка VP1, и уровень синтеза белка VP1 снижается. Первый кодон AUG, который остаётся в случае более длинного транскрипта, является стартовым кодоном для белка VP3. Однако, последовательность нуклеотидов, предшествующая этому кодону в пределах той же рамки считывания, содержит последовательность ACG, кодирующую треонин, которая окружена оптимальной последовательностью Козак . Это приводит к снижению синтеза белка VP2 (который представляет собой белок VP3 с дополнительными остатками аминокислот на N-конце[31][32][33][34].
Так как больший интрон предпочтительно вырезается из пре-мРНК и так как кодон ACG является более слабым стартовым кодоном, соответствующие белки in vivo экспрессируются в соотношении примерно 1:1:20, в таком же соотношении белки входят и в состав вирусной частицы[35]. Уникальный фрагмент на N-конце белка VP1 имеют активность фосфолипазы А2 (англ. PLA2), которая, вероятно, требуется для освобождения вирусных частиц из поздних эндосом[36]. Муралидар с соавторами показали, что белки VP2 и VP3 крайне необходимы для сборки вирусной частицы[33]. Уоррингтон с соавторами показали, что белок VP2 не является строго необходимым для сборки вирусной частицы, а также не влияет на патогенные свойства вируса. Однако, на функционирование белка VP2 не влияют значительные встройки в N-концевую часть, в то время как встройки в VP1 снижают его фосфолипазную активность[37].
Кристаллическая структура белка VP3 в 2002 году была определена исследователями Кси и Бью с соавторами[38].
Серотипы и рецепторы
К 2006 году были описаны 11 серотипов аденоассоциированного вируса[39]. Все известные серотипы могут инфицировать клетки многих видов тканей. Тканевая специфичность определяется серотипом белков капсида, поэтому векторы на основе аденоассоциированого вируса конструируют, задавая необходимый серотип.
Серотип 2
Серотип 2 аденоассоциированного вируса изучен наиболее подробно[40][41][42][43][44][45]. Аденоассоциированный вирус серотипа 2 обладает природным сродством к скелетным мышцам[46], нейронам[40], гладким мышцам сосудов[47] и гепатоцитам[48].
Для аденоассоциированного вируса серотипа 2 описан три клеточных рецептора: гепарансульфатпротеогликан (англ. HSPG), интегрин aVβ5 и рецептор 1 фактора роста фибробластов (англ. FGFR-1). Первый является первичным рецептором, последние два являются корецепторами, и позволяют аденоассоциированному вирусу попадать в клетку путём рецептор-опосредованного эндоцитоза[49][50][51][52]. HSPG значительно представлен во внеклеточном веществе и действует как первичный рецептор, при этом очищая организм от частиц аденоассоциированного вируса и снижая эффективность заражения[53].
Исследования показали, что аденоассоциированный вирус серотипа 2 убивает раковые клетки, не повреждая при этом здоровые клетки. "Наши исследования показали, что аденоассоциированный вирус второго типа, который инфицирует большую часть популяции клеток, убивает многие типы раковых клеток, но не здоровые клетки, " сообщает Крейг Мейер, профессор иммунологии и микробиологии Медицинского колледжа Penn State в Пенсильвании[54]. Данные исследования могут привести к созданию новых противораковых препаратов.
Другие серотипы
Хотя аденоассоциированный вирус серотипа 2 является наиболее популярным серотипом в научных исследованиях, было показано, что другие серотипы могут быть более эффективными векторами для доставки генов. Например, аденоассоциированный вирус серотипа 6 лучше инфицирует клетки эпителия дыхательных путей, вирус серотипа 7 имеет очень высокий уровень трансдукции клеток скелетных мышц мыши, вируса серотипа 8 прекрасно трансдуцирует гепатоциты[55][56][57], а вирусы серотипа 1 и 5 очень эффективно доставляют гены в клетки эндотелия сосудов[58]. Аденоассоциированный вирус серотипа 6, являющийся гибридом серотипов 1 и 2[57], также обладает более низкой иммунногенностью, чем вирус серотипа 2[56].
Серотипы отличаются рецепторами, с которыми происходит их связывание. Например, трансдукция вирусами серотипов 4 и 5 может быть ингибирована раствором сиаловой кислоты[59], а вирус серотипа 5 проникает в клетки через рецептор фактора роста тромбоцитов[60].
Иммунный ответ
Аденоассоциированный вирус представляет особый интерес для генной терапии, ввиду ограниченной способности индуцировать иммунный ответ у человека. Эта особенность данного вируса делает его особенно удобным для трансдукции, так как снижает риск иммунных патологий.
Врождённый иммунитет
У животных показан врождённый иммунный ответ на аденоассоциированный вирус. Внутривенное введение вируса мышам вызывает образование цитокинов воспаления, инфильтрацию нейтрофилов и других лейкоцитов в печени, что, по-видимому, значительно снижает количество введённых вирусных частиц[61].
Гуморальный иммунитет
Показано, что вирус может вызывать гуморальный ответ как у животных, так и у человека. До 80 % человеческой популяции являются серопозитивными к серотипу 2. Показано, что нейтрализующие антитела могут снижать трансдукцию векторов на основе аденоассоциированного вируса при нескольких путях введения[62].
Клеточный иммунитет
Клеточный иммунный ответ к вирусу и векторам, созданным на основе вируса был недостаточно изучен до 2005 года[62]. Клинические исследования вектора на основе аденоассоциированного вируса серотипа 2 для лечения гемофилии В показали, что может происходить разрушение трансдуцированных клеток[63]. Исследования показали, что CD8+ T-лимфоциты могут распознавать элементы капсида аденоассоциированного вируса in vitro[64], что свидетельствует о потенциальной возможности цитотоксического ответа на векторы в отношении Т-лимфоцитов. Однако, данные исследования не закончены и возможность такого цитотоксического ответа полностью не изучена.
Жизненный цикл
В жизненном цикле аденоассоциированного вируса от стадии инфицирования клетки до образования новых вирусных частиц можно выделить несколько этапов:
- прикрепление к плазматической мембране
- эндоцитоз
- перемещение в составе эндосомы
- выход из поздней эндосомы или лизосомы
- перемещение в ядро клетки
- образование репликативной вирусной двуцепочечной ДНК
- экспрессия генов rep
- репликация геномной ДНК
- экспрессия генов cap, синтез дочерней одноцепочечной ДНК
- сборка вирионов
- высвобождение вирусных частиц из заражённой клетки
Некоторые из этих этапов могут отличаться в зависимости от типа клеток. Параметры репликации ДНК вируса могут также отличаться и среди клеток одного типа, в зависимости от стадии клеточного цикла[65].
Аденоассоциированный вирус не способен реплицироваться в клетках, которые не заражены аденовирусами. Эта особенность образовывать вирусные частицы свидетельствует о том, что аденоассоциированный вирус произошёл от аденовирусов. Показано, что репликация ДНК аденоассоциированного вируса облегчается при наличии некоторых белков аденовирусов[66][67] или других вирусов, например простого герпеса[68], или генотоксичных агентов, таких, как ультрафиолетовое излучение или гидроксимочевина[69][70][71].
Минимальный набор генов аденовируса, необходимых для размножения аденоассоциированных вирусов был описан Мацуситой и Эллингером с соавторами[66]. Данное открытие позволило создать рекомбинантные аденоассоциированные вирусы, которым не требуется ко-инфицирование аденовирусом. В отсутствие вспомогательных вирусов или гентоксичных факторов, ДНК аденоассоциированного вируса может встраиваться в геном хозяина в эписомальной форме. В первом случае интеграция в геном хозяина осуществляется белками Rep78 и Rep68 и требует наличия инвертированных концевых повторов (англ. ITR) фланкирующих встраиваемую последовательность. У мышей геном аденоассоциированного вируса может находиться в виде эписомы (кольцевой ДНК, в ориентации голова-хвост) в неделящихся тканях—например, в скелетных мышцах[72].
См. также
Примечания
- Таксономия вирусов (англ.) на сайте Международного комитета по таксономии вирусов (ICTV).
- ICTV Taxonomy history: Adeno-associated dependoparvovirus A на сайте ICTV (англ.) (Дата обращения: 7 мая 2017).
- Rationalization and extension of the taxonomy of the family Parvoviridae : [англ.] // ICTVonline. — Code assigned: 2013.001a-aaaV. — 2013. — P. 8.
- Grieger J. C., Samulski R. J. Adeno-associated virus as a gene therapy vector: vector development, production and clinical applications (англ.) // Advances in biochemical engineering/biotechnology. — Berlin, Germany, 2005. — Iss. 99. — P. 119—145. — PMID 16568890.
- Atchison RW, Castro BC, Hammon WM. Adenovirus-associated defective virus particles (англ.) // Science. — 1965. — Vol. 149. — P. 754—756.
- Smith R. H. Adeno-associeated virus integration: virus versus vector // Gene Therapy. — 2008. — Т. 15, № 11. — С. 817—822. — doi:10.1038/gt.2008.55.
- Ni T-H, McDonald WF, Zolotukhin I, Melendy T, Waga S, Stillman B, Muzyczka N. Cellular proteins required for adeno-associated virus DNA replication in the absence of adenovirus coinfection // J Virol. — 1998. — Т. 72. — С. 2777—2787.
- Surosky, RT; Urabe, M & Godwin, SG et al. (1997), Adeno-associated virus Rep proteins target DNA sequences to a unique locus in the human genome, Journal of virology Т. 71 (10), PMID 9311886
- Chirmule, N; Propert, K & Magosin, S et al. (1999), Immune responses to adenovirus and adeno-associated virus in humans, Gene therapy (no. September): 1574-83, PMID 10490767
- Hernandez, YJ; Wang, J & Kearns, WG et al. (1999), Latent adeno-associated virus infection elicits humoral but not cell-mediated immune responses in a nonhuman primate model, Journal of virology (no. October): 8549-58, PMID 10482608
- Ponnazhagan, S; Mukherjee, P & Yoder, MC et al. (1997), Adeno-associated virus 2-mediated gene transfer in vivo: organ-tropism and expression of transduced sequences in mice, Gene (no. Apr 29): 203-10, PMID 9185868
- Carter, BJ (2005), Adeno-Associated Virus Vectors in Clinical Trials, Human Gene Therapy Т. 16: 541-50, PMID 15916479
- Kaplitt, MG; Feigin, A; During, MJ & others (2007), Safety and tolerability of gene therapy with an adeno-associated virus (AAV) borne GAD gene for Parkinson's disease: an open label, phase I trial, Lancet Т. 369: 2097-2105, PMID 17586305
- Erles K., Rohde V., Thaele M., Roth S., Edler L., Schlehofer J.R. DNA of adeno-associated virus (AAV) in testicular tissue and in abnormal semen samples (англ.) // Hum. Reprod. : journal. — 2001. — November (vol. 16, no. 11). — P. 2333—2337. — PMID 11679515.
- Nault J. C. et al. Recurrent AAV2-related insertional mutagenesis in human hepatocellular carcinomas // Nature genetics. — 2015.
- Carter, BJ (2000), Adeno-associated virus and adeno-associated virus vectors for gene delivery, in DD Lassic & N Smyth Templeton, Gene Therapy: Therapeutic Mechanisms and Strategies, New York City: Marcel Dekker, Inc., с. 41-59, ISBN 0-585-39515-2
- Bohenzky, RA; LeFebvre, RB & Berns, KI (1988), Sequence and symmetry requirements within the internal palindromic sequences of the adeno-associated virus terminal repeat, Virology (San Diego: Academic Press) . — Т. 166 (2), PMID 2845646
- Wang, X.S.; Ponnazhagan & Srivastava (1995), Rescue and replication signals of the adeno-associated virus 2 genome, Journal of Molecular Biology Т. 250: 573-80, PMID 7623375
- Weitzman, MD; Kyostio, SR; Kotin, RM & Owens, RA (1994), Adeno-associated virus (AAV) Rep proteins mediate complex formation between AAV DNA and its integration site in human DNA, Proceedings of the National Academy of Sciences of the United States of America Т. 91 (13): 5808-12, PMID 8016070
- Zhou, X & Muzyczka, N (1998), In vitro packaging of adeno-associated virus DNA, Journal of virology Т. 72 (4): 3241-7, PMID 9525651
- Nony, P; Tessier, J; Chadeuf, G & Ward, P et al. (2001), Novel cis-acting replication element in the adeno-associated virus type 2 genome is involved in amplification of integrated rep-cap sequences, Journal of virology Т. 75 (20): 9991-4, PMID 11559833
- Nony, P; Chadeuf, G; Tessier, J & Moullier, P et al. (2003), Evidence for packaging of rep-cap sequences into adeno- associated virus (AAV) type 2 capsids in the absence of inverted terminal repeats: a model for generation of rep-positive AAV particles, Journal of virology Т. 77, PMID 12477885
- Philpott, NJ; Giraud-Wali, C; Dupuis, C & Gomos, J et al. (2002), Efficient integration of recombinant adeno-associated virus DNA vectors requires a p5-rep sequence in cis, Journal of virology Т. 76 (11), PMID 11991970
- Tullis, GE & Shenk, T (2000), Efficient replication of adeno-associated virus type 2 vectors: a cis-acting element outside of the terminal repeats and a minimal size, Journal of virology Т. 74 (24), PMID 11090148
- Kyostio, SR; Owens, RA; Weitzman, MD & Antoni, BA et al. (1994), Analysis of adeno-associated virus (AAV) wild-type and mutant Rep proteins for their abilities to negatively regulate AAV p5 and p19 mRNA levels, Journal of virology Т. 68 (5): 2947-57, PMID 8151765
- Im, DS & Muzyczka, N (1990), The AAV origin binding protein Rep68 is an ATP-dependent site-specific endonuclease with DNA helicase activity., Cell Т. 61 (3): 447-57, PMID 2159383
- Im, DS & Muzyczka, N (1992), Partial purification of adeno-associated virus Rep78, Rep52, and Rep40 and their biochemical characterization, Journal of virology Т. 66 (2): 1119-28, PMID 1309894
- Samulski, RJ (2003), AAV vectors, the future workhorse of human gene therapy, Ernst Schering Research Foundation workshop (no. 43): 25-40, PMID 12894449
- Trempe, JP & Carter, BJ (1988a), Regulation of adeno-associated virus gene expression in 293 cells: control of mRNA abundance and translation, Journal of virology (no. 1): 68-74, PMID 2824856
- Jay, FT; Laughlin, CA & Carter, BJ (1981), Eukaryotic translational control: adeno-associated virus protein synthesis is affected by a mutation in the adenovirus DNA-binding protein, Proceedings of the National Academy of Sciences of the United States of America Т. 78 (5): 2927-31, PMID 6265925
- Becerra, SP; Rose, JA; Hardy, M & other (1985), Direct mapping of adeno-associated virus capsid proteins B and C: a possible ACG initiation codon, Proceedings of the National Academy of Sciences of the United States of America Т. 82 (23): 7919-23, PMID 2999784
- Cassinotti, P; Weitz, M & Tratschin, JD (1988), Organization of the adeno-associated virus (AAV) capsid gene: mapping of a minor spliced mRNA coding for virus capsid protein 1, Virology Т. 167 (1): 176-84, PMID 2847413
- Muralidhar, S; Becerra, SP & Rose, JA (1994), Site-directed mutagenesis of adeno-associated virus type 2 structural protein initiation codons: effects on regulation of synthesis and biological activity, Journal of virology Т. 68 (1): 170-6, PMID 8254726
- Trempe, JP & Carter, BJ (1988b), Alternate mRNA splicing is required for synthesis of adeno-associated virus VP1 capsid protein, Journal of virology Т. 62 (9): 3356-63, PMID 2841488
- Rabinowitz, JE & Samulski, RJ (2000), Building a better vector: the manipulation of AAV virions, Virology Т. 278 (2): 301-8, PMID 11118354
- Girod, A; Wobus, CE; Zádori, Z & others (2002), The VP1 capsid protein of adeno-associated virus type 2 is carrying a phospholipase A2 domain required for virus infectivity, The Journal of general virology Т. 83 (5): 973-8, PMID 11961250
- Warrington, KH,Jr; Gorbatyuk, OS; Harrison, JK & others (2004), Adeno-associated virus type 2 VP2 capsid protein is nonessential and can tolerate large peptide insertions at its N terminus, Journal of virology Т. 78 (12): 6595-609, PMID 15163751
- Xie, Q; Bu, W; Bhatia, S & others (2002), The atomic structure of adeno-associated virus (AAV-2), a vector for human gene therapy, Proceedings of the National Academy of Sciences of the United States of America Т. 99 (16): 10405-10, PMID 12136130
- Mori, S; Wang, L; Takeuchi, T & Kanda, T (2004), Two novel adeno-associated viruses from cynomolgus monkey: pseudotyping characterization of capsid protein, Virology Т. 330 (2): 375-83, PMID 15567432
- Bartlett, JS; Samulski, RJ; McCown, TJ & others (1998), Selective and rapid uptake of adeno-associated virus type 2 in brain, Human gene therapy Т. 9 (8): 1181-6, PMID 9625257
- Fischer, AC; Beck, SE; Smith, CI & others (2003), Successful transgene expression with serial doses of aerosolized rAAV2 vectors in rhesus macaques, Molecular therapy : the journal of the American Society of Gene Therapy Т. 8 (6): 918-26, PMID 14664794
- Nicklin, SA; Buening, H; Dishart, KL & others (2001), Efficient and selective AAV2-mediated gene transfer directed to human vascular endothelial cells, Molecular therapy : the journal of the American Society of Gene Therapy Т. 4 (3): 174-81, PMID 11545607
- Rabinowitz, JE; Xiao, W & Samulski, RJ (1999), Insertional mutagenesis of AAV2 capsid and the production of recombinant virus, Virology Т. 265 (2): 274-85, PMID 10600599
- Shi, W & Bartlett, JS (2003), RGD inclusion in VP3 provides adeno-associated virus type 2 (AAV2)-based vectors with a heparan sulfate-independent cell entry mechanism, Molecular therapy : the journal of the American Society of Gene Therapy Т. 7 (4): 515-25, PMID 12727115
- Wu, P; Xiao, W; Conlon, T & others (2000), Mutational analysis of the adeno-associated virus type 2 (AAV2) capsid gene and construction of AAV2 vectors with altered tropism, Journal of virology Т. 74 (18): 8635-47, PMID 10954565
- Manno, CS; Chew, AJ; Hutchison, S & others (2003), AAV-mediated factor IX gene transfer to skeletal muscle in patients with severe hemophilia B, Blood Т. 101 (8): 2963-72, PMID 12515715
- Richter, M; Iwata, A; Nyhuis, J & others (2000), Adeno-associated virus vector transduction of vascular smooth muscle cells in vivo, Physiological genomics Т. 2 (3): 117-27, PMID 11015590
- Koeberl, DD; Alexander, IE; Halbert, CL & others (1997), Persistent expression of human clotting factor IX from mouse liver after intravenous injection of adeno-associated virus vectors, Proceedings of the National Academy of Sciences of the United States of America Т. 94 (4): 1426-31, PMID 9037069
- Qing, K; Mah, C; Hansen, J & other (1999), Human fibroblast growth factor receptor 1 is a co-receptor for infection by adeno-associated virus 2, Nature medicine Т. 5 (1): 71-7, PMID 9883842
- Summerford, C & Samulski, RJ (1998), Membrane-associated heparan sulfate proteoglycan is a receptor for adeno-associated virus type 2 virions, Journal of virology Т. 72 (2): 1438-45, PMID 9445046
- Summerford, C; Bartlett, JS & Samulski, RJ (1999), AlphaVbeta5 integrin: a co-receptor for adeno-associated virus type 2 infection, Nature medicine Т. 5 (1): 78-82, PMID 9883843
- Qiu, J; Handa, A; Kirby, M & Brown, KE (2000), The interaction of heparin sulfate and adeno-associated virus 2, Virology Т. 269 (1): 137-47, PMID 10725206
- Pajusola, K; Gruchala, M; Joch, H & other (2002), Cell-type-specific characteristics modulate the transduction efficiency of adeno-associated virus type 2 and restrain infection of endothelial cells, Journal of virology Т. 76 (22): 11530-40, PMID 12388714
- CNN.com (2005), Common virus 'kills cancer', <http://www.cnn.com/2005/HEALTH/06/22/cancer.virus/index.html>
- Gao, GP; Alvira, MR; Wang, L & other (2002), Proceedings of the National Academy of Sciences of the United States of America Т. 99 (18): 11854-9, PMID 12192090
- Halbert, CL; Allen, JM & Miller, AD (2001), Adeno-associated virus type 6 (AAV6) vectors mediate efficient transduction of airway epithelial cells in mouse lungs compared to that of AAV2 vectors, Journal of virology. (J Virol) Jul; (): Т. 75 (14): 6615-24, PMID 11413329
- Rabinowitz, JE; Bowles, DE; Faust, SM & other (2004), Cross-dressing the virion: the transcapsidation of adeno-associated virus serotypes functionally defines subgroups, Journal of virology Т. 78 (9): 4421-32, PMID 15078923
- Chen, S; Kapturczak, M; Loiler, SA & others (2005), Efficient transduction of vascular endothelial cells with recombinant adeno-associated virus serotype 1 and 5 vectors, Human gene therapy Т. 16 (2): 235-47, PMID 15761263
- Kaludov, N; Brown, KE; Walters, RW & others (2001), Adeno-associated virus serotype 4 (AAV4) and AAV5 both require sialic acid binding for hemagglutination and efficient transduction but differ in sialic acid linkage specificity, Journal of virology Т. 75 (15): 6884-93, PMID 11435568
- Di Pasquale, G; Davidson, BL; Stein, CS & others, Identification of PDGFR as a receptor for AAV-5 transduction, Nature medicine Т. 9 (10): 1306-12, PMID 14502277
- Zaiss, AK; Liu, Q; Bowen, GP & others (2002), Differential Activation of Innate Immune Responses by Adenovirus and Adeno-Associated Virus Vectors, Journal of Virology Т. 76 (9): 4580-90, PMID 11932423
- Zaiss, AK & Muruve, DA (2005), Immune responses to adeno-associated virus vectors, Current Gene Therapy Т. 5 (3): 323-31, PMID 15975009
- High, KA; Mannos, CS; Pierce, GF & Others (2006), Successful transduction of liver in hemophilia by AAV-Factor IX and limitations imposed by the host immune response, Nature Medicine Т. 12 (3): 342-47, PMID 16474400
- High, KA; Sabatino, DE; Mingozzi, F & Others (2005), Identification of Mouse AAV Capsid-Specific CD8+ T Cell Epitopes, Molecular Therapy Т. 12 (6): 1023-33, PMID 16263332
- Rohr, UP; Kronenwett, R; Grimm, D & others (2002), Primary human cells differ in their susceptibility to rAAV-2-mediated gene transfer and duration of reporter gene expression, Journal of virological methods Т. 105 (2): 265-75, PMID 12270659
- Matsushita, T; Elliger, S; Elliger, C & others (1998), Adeno-associated virus vectors can be efficiently produced without helper virus, Gene therapy Т. 5 (7): 938-45, PMID 9813665
- Myers, MW; Laughlin, CA; Jay, FT & other (1980), Adenovirus helper function for growth of adeno-associated virus: effect of temperature- sensitive mutations in adenovirus early gene region 2, Journal of virology Т. 35 (1): 65-75, PMID 6251278
- Handa, H & Carter, BJ (1979), Adeno-associated virus DNA replication complexes in herpes simplex virus or adenovirus-infected cells, The Journal of biological chemistry Т. 254 (14): 6603-10, PMID 221504
- Yalkinoglu, AO; Heilbronn, R; Bürkle, A & other (1988), DNA amplification of adeno-associated virus as a response to cellular genotoxic stress, Cancer research Т. 48 (11): 3123-9, PMID 2835153
- Yakobson, B; Koch, T & Winocour, E (1987), Replication of adeno-associated virus in synchronized cells without the addition of a helper virus, Journal of virology Т. 61 (4): 972-81, PMID 3029431
- Yakobson, B; Hrynko, TA; Peak, MJ & Winocour, E (1989), Replication of adeno-associated virus in cells irradiated with UV light at 254 nm, Journal of virology Т. 63 (3): 1023-30, PMID 2536816
- Duan, D; Sharma, P; Yang, J & others (1998), Circular intermediates of recombinant adeno-associated virus have defined structural characteristics responsible for long-term episomal persistence in muscle tissue, Journal of virology Т. 72 (11): 8568-77, PMID 9765395
Литература
- Шахбазов А.В., Северин И.Н., Гончарова Н.В., Гринев В.В., Космачева С.М., Потапнев М.П. Вирусные векторы для стабильной трансдукции мезенхимальных стволовых клеток человека: системы на основе аденоассоциированных вирусов и лентивирусов // Клеточные технологии в биологии и медицине. — 2008. — Т. 4. — С. 216—218.