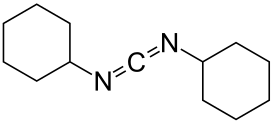
1,3-Дициклогексилкарбодиимид
Дициклогексилкарбодиимид — реагент, широко применяющийся в органическом синтезе. Представляет собой белое твёрдое вещество с тяжёлым сладким запахом и низкой температурой плавления. Используется, в основном, как сшивающий и водоотнимающий реагент в синтезе амидов, эфиров и ангидридов, а также в ряде других превращений.
| Дициклогексилкарбодиимид | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
N,N'-дициклогексилкарбодиимид |
| Сокращения | ДЦК, DCC |
| Хим. формула | C13H22N2 |
| Физические свойства | |
| Состояние | белое твёрдое вещество |
| Молярная масса | 206,33 г/моль |
| Плотность | 1,325 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 34 °C |
| • кипения | 122 (6 мм рт. ст.) °C |
| • вспышки | 113 °C |
| Классификация | |
| Рег. номер CAS | 538-75-0 |
| PubChem | 10868 |
| Рег. номер EINECS | 208-704-1 |
| SMILES | |
| InChI | |
| RTECS | FF2160000 |
| ChEBI | CHEBI:53090 |
| ChemSpider | 10408 |
| Безопасность | |
| Фразы риска (R) | R22, R24, R41, R43 |
| Фразы безопасности (S) | S24, S26, S37/39, S45 |
| Краткие характер. опасности (H) |
H302, H311, H317, H318 |
| Меры предостор. (P) |
P280, P305+P351+P338, P312 |
| Сигнальное слово | Опасно |
| Пиктограммы СГС |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Получение
Дициклогексилкарбодиимид может быть получен из дициклогексилмочевины под действием оксида фосфора(V). Другой метод основан на реакции между циклогексиламином и циклогексилизоцианидом[1].
Физические свойства
Дициклогексилкарбодиимид хорошо растворим в хлористом метилене, тетрагидрофуране, ацетонитриле, диметилформамиде[2].
Применение в органическом синтезе
Основная область применения данного реагента — синтез амидов, эфиров и ангидридов, где он проявляет свойства мощного водоотнимающего агента. Уже после первых сообщений об открытии в 1955 году дициклогексилкарбодиимид стал применяться в синтезе пептидов и других реакциях, где происходит формирование амидной связи. Типичная методика заключается в добавлении реагента (1,1 экв.) к концентрированному (0,1—1,0 М) раствору карбоновой кислоты (1 экв.), амина (1 экв.) и катализатора в хлористом метилене или ацетонитриле при 0 °С. В ходе реакции образуется осадок дициклогексилмочевины (продукта гидратации дициклогексилкарбодиимида). Как правило, реакция заканчивается через час. В качестве растворителей используются также тетрагидрофуран и диметилформамид, однако они уменьшают скорость реакции и вызывают образование побочного продукта N-ацилмочевины, а также рацемизацию хиральных карбоновых кислот. Эти проблемы можно решить путём добавления сшивающих реагентов типа гидроксибензотриазола (HOBt), гидроксисукцинимида (HOSu) и др. Эти добавки необходимы также в тех случаях, когда реагенты являются затруднёнными либо когда нуклеофильные свойства амина понижены[2].
Дициклогексилкарбодиимид применяется в синтезе ангидридов. Среди аналогичных реагентов (уксусный ангидрид, трифторуксусный ангидрид, оксид фосфора и др.) он является одним из самых эффективных, простых и мягких[2].
Также дициклогексилкарбодиимид катализирует реакцию окисления первичных и вторичных спиртов под действием диметилсульфоксида (реакция Моффата)[2].
Хранение и использование
Дициклогексилкарбодиимид вызывает острое раздражение кожи у чувствительных людей. Вещество имеет низкую температуру плавления, поэтому с ним удобно обращаться в жидком состоянии. Работать с дициклогексилкарбодиимидом необходимо под тягой и в перчатках, а хранить его следует вне доступа влаги[2].
Примечания
- Kvasnica M. Dicyclohexylcarbodiimide (DCC) (англ.) // Synlett. — 2007. — No. 14. — P. 2306—2307. — doi:10.1055/s-2007-985575.
- Albert J. S., Hamilton A. D., Hart A. C. 1,3-Dicyclohexylcarbodiimide (англ.) // e-EROS Encyclopedia of Reagents for Organic Synthesis. — Wiley, 2010. — doi:10.1002/047084289X.rd146.pub2.
Ссылки
- Sigma-Aldrich. ИК-спектр дициклогексилкарбодиимида. Дата обращения: 4 января 2015.
- Sigma-Aldrich. КР-спектр дициклогексилкарбодиимида. Дата обращения: 4 января 2015.
- Sigma-Aldrich. ЯМР-спектр дициклогексилкарбодиимида. Дата обращения: 4 января 2015.
