Перхлорат серебра
Перхлора́т серебра́ — неорганическое соединение, соль металла серебра и хлорной кислоты с формулой , бесцветные кристаллы, хорошо растворяется в воде, образует кристаллогидрат.
| Перхлорат серебра | |
|---|---|
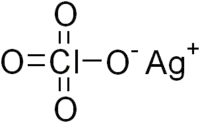 | |
| Общие | |
| Систематическое наименование |
Перхлорат серебра |
| Традиционные названия | Хлорнокислое серебро |
| Хим. формула | |
| Физические свойства | |
| Состояние | бесцветные гигроскопические кристаллы |
| Молярная масса | 207,32 г/моль |
| Плотность | 2,806 г/см³ |
| Термические свойства | |
| Температура | |
| • разложения | 486 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 54525; 792,899 г/100 мл |
| • в бензоле | 58,2 г/л |
| • в толуоле | 1010 г/л |
| Классификация | |
| Рег. номер CAS | 7783-93-9 |
| PubChem | 24562 |
| Рег. номер EINECS | 232-035-4 |
| SMILES | |
| InChI | |
| ChemSpider | 22968 |
| Безопасность | |
| Краткие характер. опасности (H) | H272, H314 |
| Меры предостор. (P) | P210, P220, P221, P260, P264, P280, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P321, P363, P370+378, P405, P501 |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Применяется в органическом синтезе в качестве катализатора.
Получение
- Действие избытка хлорной кислоты на нитрат серебра(I) при нагревании:
-
- .
- Действие перхлората бария на сульфат серебра:
- .
- Растворением серебра в концентрированной хлорной кислоте:
- .
- Растворением оксида серебра(I) в хлорной кислоте.
Физические свойства
Перхлорат серебра образует быстро расплывающиеся на воздухе бесцветные кристаллы, кубической сингонии, пространственная группа F 43m, параметры ячейки a = 0,701 нм, Z = 4.
Очень хорошо растворяется в воде, растворяется в этаноле, диэтиловом эфире, толуоле, бензоле.
Образует кристаллогидрат состава . Из аммиачных растворов выделяются аддукты состава .
Применение
- Катализатор в органической химии.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4. — 639 с. — ISBN 5-82270-092-4.
- Справочник химика / Редкол.: Никольский Б. П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б. П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
