Оксиды иода
Окси́ды ио́да — бинарные химические соединения иода и кислорода. Лишь некоторые из теоретически возможных оксидов иода были выделены в чистом виде. Ряд соединений, вероятно являющихся оксидами иода, был обнаружен в атмосфере; эти соединения считаются важным фактором в обмене иодом между океаном и атмосферой[1].
| Молекулярная формула | I2O | IO[3] | IO2 | I2O4 | I2O5 | I4O9 |
|---|---|---|---|---|---|---|
| Название | монооксид дииода | монооксид иода | диоксид иода | тетраоксид дииода | пентаоксид дииода | нонаоксид тетраиода |
| Структурная формула | I2O | IO | IO2 | (IO2)2 | O(IO2)2 | I(OIO2)3 |
| Регистрационный номер CAS | 39319-71-6 | 14696-98-1 | 13494-92-3 | 1024652-24-1 | 12029-98-0 | 66523-94-2 |
| Состояние при н.у. | Неизвестно | фиолетовый газ | тв., жёлтый | тв., жёлтый | белые кристаллы | тв., тёмно-жёлтый |
| Степень окисления | +1 | +2 | +4 | +3 и +5 | +5 | +3 и +5 |
| Температура плавления | Неизвестно | Неизвестно | Неизвестно | Разл. 100 °C | Разл. 300—350 °C | Разл. 75 °C |
| Плотность, г/см3 | 4,2 | 4,8 | ||||
| Растворимость в воде | реаг. с обр. HIO3 + I2 | 187 г/100 мл | реаг. с обр. HIO3 + I2 |
Монооксид дииода экспериментально не наблюдался, исследовался теоретически[4], однако существуют указания на возможность его синтеза тем же путём, которым синтезируется монооксид дихлора, в реакции оксида ртути(II) HgO с элементным иодом I2[5]. Это соединение крайне нестабильно, однако может галогенировать алкены[6].
Диоксид иода (IO2) и тетраоксид дииода ((IO2)2), а также свободный радикал монооксид иода (IO) участвуют в важных процессах в химии атмосферы. Они образуются в очень малых количествах на поверхности морей при фотоокислении дииодметана, продуцируемого морскими водорослями[7]. Несмотря на малые концентрации (порядка трлн-1), они считаются активными катализаторами разрушения озона[8][9].
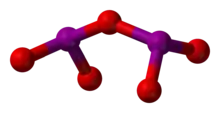
Пентаоксид дииода (I2O5) является ангидридом иодноватой кислоты (HIO3) и единственным стабильным ангидридом иода.
Нонаоксид тетраиода (I4O9 или I(IO3)3) был синтезирован в газофазной реакции I2 с O3[10]. Может рассматриваться как иодат(V) иода(III).
См. также
Примечания
- Kaltsoyannis Nikolas, Plane John M. C. Quantum chemical calculations on a selection of iodine-containing species (IO, OIO, INO3, (IO)2, I2O3, I2O4 and I2O5) of importance in the atmosphere (англ.) // Physical Chemistry Chemical Physics : journal. — 2008. — Vol. 10, no. 13. — P. 1723. — doi:10.1039/B715687C.
- CRC Handbook of Chemistry and Physics / D. R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — 2828 p. — ISBN 1420090844.
- Nikitin I V. Halogen monoxides // Успехи химии. — Российская академия наук, 2008. — Т. 77, № 8. — С. 739—749. — doi:10.1070/RC2008v077n08ABEH003788.
- Novak Igor. Theoretical study of I2O (неопр.) // Heteroatom Chemistry. — 1998. — Т. 9, № 4. — С. 383—385. — doi:10.1002/(SICI)1098-1071(1998)9:4<383::AID-HC6>3.0.CO;2-9.
- Forbes C. P., Goosen A., Laue H. A. H. Hypoiodite reaction: kinetic study of the reaction of 1,1-diphenyl-ethylene with mercury(II) oxide iodine (англ.) // Journal of the Chemical Society : journal. — Chemical Society, 1974. — P. 2350. — doi:10.1039/P19740002350.
- Cambie R. C. et al. Reactions of iodine oxide with alkenes (англ.) // Journal of the Chemical Society : journal. — Chemical Society, 1976. — No. 18. — P. 1961. — doi:10.1039/P19760001961.
- Hoffmann T., O'Dowd C. D. Seinfeld J. H. Iodine oxide homogeneous nucleation: An explanation for coastal new particle production (англ.) // Geophysical Research Letters : journal. — 2001. — Vol. 28, no. 10. — P. 1949—1952. — doi:10.1029/2000GL012399.
- Saiz-Lopez A. et al. Iodine chemistry in the troposphere and its effect on ozone (англ.) // Atmospheric Chemistry and Physics : journal. — 2014. — Vol. 14, no. 23. — P. 13119—13143. — doi:10.5194/acp-14-13119-2014.
- Cox R. A. et al. OIO and the atmospheric cycle of iodine (англ.) // Geophysical Research Letters : journal. — 1999. — Vol. 26, no. 13. — P. 1857—1860. — doi:10.1029/1999GL900439.
- Sunder S., Wren J. C., Vikis A. C. Raman spectra of I4O9 formed by the reaction of iodine with ozone (англ.) // Journal of Raman Spectroscopy : journal. — 1985. — Vol. 16, no. 6. — P. 424—426. — doi:10.1002/jrs.1250160611.
