Киназа Aurora B
Киназа Aurora B (англ. Aurora B kinase) — белок, прикрепляющий митотическое веретено деления к центромере.
Функция
Хромосомная сегрегация во время митоза, а также мейоза регулируется киназами и фосфатазами. Киназа Aurora ассоциирована с микротрубочками во время движения хромосом и их сегрегации. Киназа Aurora B локализуется в микротрубочках вблизи кинетохор, специально для специализированных микротрубочек, называемых K-волокнами, и киназы Aurora А (МИМ 603072) локализующейся в центросомах (Лампсон и др., 2004 г.)[1].
В раковых клетках экспрессия этих ферментов вызывает неравномерное распределение генетической информации, создавая анеуплоидные клетки, являющиеся отличительной чертой рака.
Открытие
В 1998 году киназа Aurora B была обнаружена в организме человека с помощью скрининга полимеразной цепной реакции для киназ, которые сверхэкспрессируются при раке[2]. В том же году киназа Aurora B была идентифицирована у крыс посредством скрининга, разработанным для поиска киназ, которые изменяли пролиферацию S. cerevisiae при сверхэкспрессии[3].
Экспрессия и внутриклеточная локализация
Экспрессия и активность Aurora B регулируются в соответствии с клеточным циклом. Экспрессия Aurora B достигает максимума во время перехода G2-M, в то время как наибольшая активность белка Aurora B наблюдается во время митоза[2].
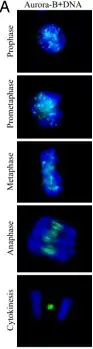
Aurora B является белком хромосомного пассажира. В частности, Aurora В локализуется в хромосомах в профазе, в центромерах в прометафазе и метафазе и центральном митотическом веретене деления в анафазе[4]. Эта локализация была определена путём косвенной иммунофлюоресценции клеток млекопитающих, Caenorhabditis elegans и Drosophila melanogaster. Более детальный анализ локализации белка Aurora B был проведен в клетках млекопитающих, помечая Aurora B зеленым флуоресцентным белком[5]. Этот анализ показал, что объединение Aurora B с центромерой является динамическим (Aurora B около центромер постоянно обмениваясь с пулом цитоплазматической Aurora B). Анализ помеченных Aurora B также предполагает, что они ассоциируют с микротрубочками веретена деления во время анафазы митоза, и эта ассоциация значительно ограничивает её подвижность. Наконец, часть помеченой Aurora B локализована в экваториальной коре клеток, их транспортировка туда осуществляется с помощью астральных микротрубочек.
Регуляция Aurora B
Aurora B образует комплекс с тремя другими белками: сурвивином, бореалином и INCENP. Каждый из четырех компонентов комплекса требуется для надлежащей локализации и функционирования трех других[6]. INCENP стимулирует активность киназы Aurora B. Сурвивин может делать то же самое[7].
Для локализации Aurora B в центромерах в прометафазе и метафазе у млекопитающих требуется фосфорилирование кинетохоро-специфических гистонов — вариант H3 белка центромеры А (CENP-A)[8]. CENP-A связывается с центромерой и необходим для сборки кинетохор, фосфорилирования CENP-А вблизи серина 7 киназой Aurora A, рекрутирующего Aurora B для центромеры[9]. Aurora B, сама по себе, может также фосфорилировать CENP-A до того же остатка, когда будет рекрутирована (смотри ниже).
Кроме того, топоизомераза II была вовлечена в регуляцию локализации Aurora B и ферментативной активности[10]. Эта регулирующая роль может быть непосредственно связана с ролью топоизомеразы II в расклинивании сестринских хроматид до анафазы. В обедненных топоизомеразой II клетках Aurora B и INCENP не перемещаются на центральное веретено деления в конце митоза. Вместо этого они остаются тесно взаимосвязаны с центромерой без отрыва сестринских хроматид. Кроме того, клетки с дефицитом топоизомеразы II представляют значительное снижение активности киназы Aurora B. Ингибирование Aurora B из-за потери топоизомеразы II, кажется, зависит от активности BubR1 (см. ниже)
Aurora B, как было выявлено, связываются с белком связывающего конца 1 (EB1), белком, который регулирует динамику микротрубочек[11]. Непрямая иммунофлуоресценция показала, что Aurora B и EB1 локализуются в анафазе в центральном веретене деления и в середине тела во время цитокинеза. Интересно, что избыточная экспрессия EB1 повышает активность киназы Aurora B, по крайней мере, отчасти потому, что EB1 блокирует дефосфорилирование/инактивация Aurora B с помощью белка фосфатазы 2А.
Роль в хромосомной биориентации
Исследования, проведенные в нескольких организмах, показывают, что у Aurora B регулирует биориентацию хромосом, что гарантирует соответствующие соединения между микротрубочками веретена деления и кинетохорами.
Ингибирование функций Aurora B с помощью РНК-интерференции[12] или микроинъекции блокирующих антител[13] ухудшает выравнивание хромосом по экватору митотического веретена деления. Этот процесс выравнивания определяется как конгрессия хромосомы. Причина этого дефекта является предметом постоянного изучения. Ингибирование Aurora B может привести к увеличению количества синтелических вложений (сестринских хроматидных пар, в которых обе сестры кинетохора прикреплены к микротрубочкам, исходящим из того же полюса веретена)[14]. Интересно, что экспрессия доминантно-негативной и каталитически неактивной формы Aurora В нарушает привязанность микротрубочек к кинетохорам и предотвращает объединение динеинного и центромерного белка Е (CENP-E) с кинетохорами.
Многочисленные кинетохорные цели киназы Aurora были определены в организмах, начиная от дрожжей до человека. В частности, CENP-A это цель Aurora B[8]. Фосфорилирование CENP-А Aurora B достигает максимума в прометафазе. В самом деле, Aurora А нацелена на тот же сайт CENP-фосфорилирования, что и Aurora B и CENP-фосфорилирование с помощью Aurora A, как полагают, предшествуют аналогичному действию Aurora В. Таким образом, была предложена модель, в которой CENP-фосфорилирование с помощью Aurora A рекрутирует Aurora B для центромеры, которая поддерживает фосфорилирования CENP-А в петле положительной обратной связи. Как ни странно, мутация этого фосфорилирования в CENP-А приводит к дефектам в цитокинезе.
Aurora B также взаимодействует с митотическим центромерно-ассоциированным кинезином (MCAK). Как Aurora B, так и MCAK локализуются во внутренней центромере в прометафазе[15]. Aurora B, как было выявлено, рекрутирует MCAK для центромеры и непосредственно фосфорилирует MCAK до различных остатков[16]. Фосфорилирование MCAK Aurora B ограничивает способность MCAK к деполимеризации микротрубочек. Важно отметить, что ингибирование MCAK рядом подходов приводит к неправильному прикреплению к кинетохорам микротрубочек веретена деления[17].
Была выдвинута гипотеза, что напряженность, порожденная амфителической привязанностью (биориентация; привязанность сестринской кинетохоры к противоположным полюсам веретена) тянет сестринские кинетохоры друг от друга, таким образом, нарушая взаимодействие Aurora B в внутренней части центромеры с микротрубочками сайтов связывания волокнистой короны с внешним центромером. В частности, напряжение, генерирующее биориентацию, тянет MCAK вовне зоны локализации Aurora B[16]. Таким образом, митоз протекает на фоне биориентации и диссоциации Aurora B с её субстратами.
Роль в конденсации и когезии хромосом
Aurora B отвечает за фосфорилирование гистона-Н3 в серине 10 в митозе[18]. Эта модификация сохраняется от дрожжей (где известна как киназа Ipl1) до человека. Примечательно, гистоны Н3, фосфорилированные Aurora B, кажется, не несут ответственности за конденсацию хроматина. Хотя Aurora B обогащается в центромерах, она локализует диффузно весь хроматин.
В клетках дрозофилы истощение Aurora B нарушает структуру хромосом и уплотнения[19]. В этих клетках комплекс конденсина не локализуется в хромосомах надлежащим образом. Аналогичным образом, в C. elegans активность конденсина зависит от Aurora B в метафазе[20]. Однако в клеточных экстрактах Xenopus конденсин связывается и конденсация хромосом не зависит от Aurora B. Аналогично, после обработки клеток ингибитором фермента Aurora B (локализация Aurora B не влияет), комплекс конденсина локализуется нормально[21].
Aurora B локализуется в парных плечах гомологичных хромосом в метафазе I мейоза C. elegans и нарушает динамику микротрубочек в митозе[22]. Освобождение этой когезии, которая зависит от Aurora B, необходимо для прогрессирования к анафазе I и сегрегации гомологичных хромосом[23]. В митотических позвоночных B-лимфоцитах для собственной центромерной локализации связывающих партнеров ряда Aurora B требуется когезин[24].
Роль в цитокинезе
Комплекс Aurora B необходим для цитокинеза у позвоночных, Caenorhabditis elegans, Drosophila melanogaster и делящихся дрожжей.
В различных типах клеток избыточная экспрессия каталитически неактивной Aurora B предотвращает цитокинез[3]. Нарушения цитокинеза также могут возникнуть по причине нарушений локализации Aurora B из-за мутации её связывающих партнеров[25].
Aurora B нацелена на ряд белков, которые локализуются в бороздке расщепления, в том числе промежуточных филаментов типа III белков виментина[26], десмина и глиального фибриллярного кислого белка (GFAP)[27]. В целом, фосфорилирование дестабилизирует промежуточные филаменты. Таким образом, было предположено, что фосфорилирование промежуточных филаментов у бороздки расщепления дестабилизирует нити в процессе подготовки к цитокинезу[27]. В соответствии с этой гипотезой, мутация сайтов-мишеней Aurora B в белках промежуточных филаментов приводит к дефектам типа деформации нити и предотвращает заключительный этап цитокинеза.
Aurora B фосфорилирует также миозин II легкой регуляторной цепи в бороздке расщепления. Ингибирование активности Aurora B препятствует нормальному локализации миозина II для бороздки расщепления и разрушает организацию веретена деления в средней зоне[28].
Роль в сборке контрольной точки веретена деления
Сборка контрольной точки веретена деления ингибирует прогрессирование митоза от анафазы к метафазе пока все пары сестринских хроматид обладают двойной ориентацией. Клетки, лишенные Aurora B, не блокируются в метафазе хромосомой, даже когда не хватает привязанности микротрубочек[14]. Следовательно, дефицит Aurora B приводит к прогрессированию перехода через анафазу, несмотря на наличие смещенных хромосом.
Aurora B может быть вовлечена в локализацию MAD2 и BubR1, белков, которые распознают правильность вложения в хромосомы микротрубочек веретена деления. Потеря Aurora B снижает концентрацию Mad2 и BubR1 в кинетохорах. В частности, Aurora B, кажется, отвечает за поддержание локализации Mad2 и BubR1 в кинетохорах после их первоначального рекрутирования, который происходит независимо от Aurora B[29]. Aurora B может быть прямо или косвенно вовлечена в гиперфосфорилирование BubR1 в митозе в клетках дикого типа[30].
Взаимодействия
Киназа B Aurora, как было выявлено, взаимодействует с:
Роль в раке
Аномально повышенные уровни киназы Aurora B вызывают неравное хромосомное разделение во время клеточного деления, приводящие к образованию клеток с аномальным числом хромосом, которые одновременно являются причиной и продвигающей структурой рака.
Ингибирование киназы Aurora B с помощью BI811283 в раковых клетках приводит к образованию клеток с сильно аномальным числом хромосом (полиплоидных клеток). Парадоксально, ингибирование киназы Aurora B на самом деле порождает полиплоидные клетки, образованные для продолжения разделения. Однако, поскольку эти клетки имеют серьезные хромосомные аномалии, они в конечном счете прекращают деление или приводят к гибели клеток[37][38].
Примечания
- Entrez Gene: AURKB aurora kinase B.
- Bischoff J. R., Anderson L., Zhu Y., Mossie K., Ng L., Souza B., Schryver B., Flanagan P., Clairvoyant F., Ginther C., Chan C. S., Novotny M., Slamon D. J., Plowman G. D. A homologue of Drosophila aurora kinase is oncogenic and amplified in human colorectal cancers. (англ.) // The EMBO journal. — 1998. — Vol. 17, no. 11. — P. 3052—3065. — doi:10.1093/emboj/17.11.3052. — PMID 9606188.
- Terada Y., Tatsuka M., Suzuki F., Yasuda Y., Fujita S., Otsu M. AIM-1: a mammalian midbody-associated protein required for cytokinesis. (англ.) // The EMBO journal. — 1998. — Vol. 17, no. 3. — P. 667—676. — doi:10.1093/emboj/17.3.667. — PMID 9450992.
- Adams R. R., Carmena M., Earnshaw W. C. Chromosomal passengers and the (aurora) ABCs of mitosis. (англ.) // Trends in cell biology. — 2001. — Vol. 11, no. 2. — P. 49—54. — PMID 11166196.
- Murata-Hori M., Tatsuka M., Wang Y. L. Probing the dynamics and functions of aurora B kinase in living cells during mitosis and cytokinesis. (англ.) // Molecular biology of the cell. — 2002. — Vol. 13, no. 4. — P. 1099—1108. — doi:10.1091/mbc.01-09-0467. — PMID 11950924.
- Honda R., Körner R., Nigg E. A. Exploring the functional interactions between Aurora B, INCENP, and survivin in mitosis. (англ.) // Molecular biology of the cell. — 2003. — Vol. 14, no. 8. — P. 3325—3341. — doi:10.1091/mbc.E02-11-0769. — PMID 12925766.
- Chen J., Jin S., Tahir S. K., Zhang H., Liu X., Sarthy A. V., McGonigal T. P., Liu Z., Rosenberg S. H., Ng S. C. Survivin enhances Aurora-B kinase activity and localizes Aurora-B in human cells. (англ.) // The Journal of biological chemistry. — 2003. — Vol. 278, no. 1. — P. 486—490. — doi:10.1074/jbc.M211119200. — PMID 12419797.
- Zeitlin S. G., Shelby R. D., Sullivan K. F. CENP-A is phosphorylated by Aurora B kinase and plays an unexpected role in completion of cytokinesis. (англ.) // The Journal of cell biology. — 2001. — Vol. 155, no. 7. — P. 1147—1157. — doi:10.1083/jcb.200108125. — PMID 11756469.
- Kunitoku N., Sasayama T., Marumoto T., Zhang D., Honda S., Kobayashi O., Hatakeyama K., Ushio Y., Saya H., Hirota T. CENP-A phosphorylation by Aurora-A in prophase is required for enrichment of Aurora-B at inner centromeres and for kinetochore function. (англ.) // Developmental cell. — 2003. — Vol. 5, no. 6. — P. 853—864. — PMID 14667408.
- Coelho P. A., Queiroz-Machado J., Carmo A. M., Moutinho-Pereira S., Maiato H., Sunkel C. E. Dual role of topoisomerase II in centromere resolution and aurora B activity. (англ.) // Public Library of Science Biology. — 2008. — Vol. 6, no. 8. — P. e207. — doi:10.1371/journal.pbio.0060207. — PMID 18752348.
- Sun L., Gao J., Dong X., Liu M., Li D., Shi X., Dong J. T., Lu X., Liu C., Zhou J. EB1 promotes Aurora-B kinase activity through blocking its inactivation by protein phosphatase 2A. (англ.) // Proceedings of the National Academy of Sciences of the United States of America. — 2008. — Vol. 105, no. 20. — P. 7153—7158. — doi:10.1073/pnas.0710018105. — PMID 18477699.
- Adams R. R., Maiato H., Earnshaw W. C., Carmena M. Essential roles of Drosophila inner centromere protein (INCENP) and aurora B in histone H3 phosphorylation, metaphase chromosome alignment, kinetochore disjunction, and chromosome segregation. (англ.) // The Journal of cell biology. — 2001. — Vol. 153, no. 4. — P. 865—880. — PMID 11352945.
- Kallio M. J., McCleland M. L., Stukenberg P. T., Gorbsky G. J. Inhibition of aurora B kinase blocks chromosome segregation, overrides the spindle checkpoint, and perturbs microtubule dynamics in mitosis. (англ.) // Current biology : CB. — 2002. — Vol. 12, no. 11. — P. 900—905. — PMID 12062053.
- Hauf S., Cole R. W., LaTerra S., Zimmer C., Schnapp G., Walter R., Heckel A., van Meel J., Rieder C. L., Peters J. M. The small molecule Hesperadin reveals a role for Aurora B in correcting kinetochore-microtubule attachment and in maintaining the spindle assembly checkpoint. (англ.) // The Journal of cell biology. — 2003. — Vol. 161, no. 2. — P. 281—294. — doi:10.1083/jcb.200208092. — PMID 12707311.
- Wordeman L., Wagenbach M., Maney T. Mutations in the ATP-binding domain affect the subcellular distribution of mitotic centromere-associated kinesin (MCAK). (англ.) // Cell biology international. — 1999. — Vol. 23, no. 4. — P. 275—286. — doi:10.1006/cbir.1999.0359. — PMID 10600236.
- Andrews P. D., Ovechkina Y., Morrice N., Wagenbach M., Duncan K., Wordeman L., Swedlow J. R. Aurora B regulates MCAK at the mitotic centromere. (англ.) // Developmental cell. — 2004. — Vol. 6, no. 2. — P. 253—268. — PMID 14960279.
- Kline-Smith S. L., Khodjakov A., Hergert P., Walczak C. E. Depletion of centromeric MCAK leads to chromosome congression and segregation defects due to improper kinetochore attachments. (англ.) // Molecular biology of the cell. — 2004. — Vol. 15, no. 3. — P. 1146—1159. — doi:10.1091/mbc.E03-08-0581. — PMID 14699064.
- Hsu J. Y., Sun Z. W., Li X., Reuben M., Tatchell K., Bishop D. K., Grushcow J. M., Brame C. J., Caldwell J. A., Hunt D. F., Lin R., Smith M. M., Allis C. D. Mitotic phosphorylation of histone H3 is governed by Ipl1/aurora kinase and Glc7/PP1 phosphatase in budding yeast and nematodes. (англ.) // Cell. — 2000. — Vol. 102, no. 3. — P. 279—291. — PMID 10975519.
- Giet R., Glover D. M. Drosophila aurora B kinase is required for histone H3 phosphorylation and condensin recruitment during chromosome condensation and to organize the central spindle during cytokinesis. (англ.) // The Journal of cell biology. — 2001. — Vol. 152, no. 4. — P. 669—682. — PMID 11266459.
- Crosio C., Fimia G. M., Loury R., Kimura M., Okano Y., Zhou H., Sen S., Allis C. D., Sassone-Corsi P. Mitotic phosphorylation of histone H3: spatio-temporal regulation by mammalian Aurora kinases. (англ.) // Molecular and cellular biology. — 2002. — Vol. 22, no. 3. — P. 874—885. — PMID 11784863.
- MacCallum D. E., Losada A., Kobayashi R., Hirano T. ISWI remodeling complexes in Xenopus egg extracts: identification as major chromosomal components that are regulated by INCENP-aurora B. (англ.) // Molecular biology of the cell. — 2002. — Vol. 13, no. 1. — P. 25—39. — doi:10.1091/mbc.01-09-0441. — PMID 11809820.
- Kaitna S., Pasierbek P., Jantsch M., Loidl J., Glotzer M. The aurora B kinase AIR-2 regulates kinetochores during mitosis and is required for separation of homologous Chromosomes during meiosis. (англ.) // Current biology : CB. — 2002. — Vol. 12, no. 10. — P. 798—812. — PMID 12015116.
- Rogers E., Bishop J. D., Waddle J. A., Schumacher J. M., Lin R. The aurora kinase AIR-2 functions in the release of chromosome cohesion in Caenorhabditis elegans meiosis. (англ.) // The Journal of cell biology. — 2002. — Vol. 157, no. 2. — P. 219—229. — doi:10.1083/jcb.200110045. — PMID 11940606.
- Sonoda E., Matsusaka T., Morrison C., Vagnarelli P., Hoshi O., Ushiki T., Nojima K., Fukagawa T., Waizenegger I. C., Peters J. M., Earnshaw W. C., Takeda S. Scc1/Rad21/Mcd1 is required for sister chromatid cohesion and kinetochore function in vertebrate cells. (англ.) // Developmental cell. — 2001. — Vol. 1, no. 6. — P. 759—770. — PMID 11740938.
- Mackay A. M., Ainsztein A. M., Eckley D. M., Earnshaw W. C. A dominant mutant of inner centromere protein (INCENP), a chromosomal protein, disrupts prometaphase congression and cytokinesis. (англ.) // The Journal of cell biology. — 1998. — Vol. 140, no. 5. — P. 991—1002. — PMID 9490714.
- Goto H., Yasui Y., Kawajiri A., Nigg E. A., Terada Y., Tatsuka M., Nagata K., Inagaki M. Aurora-B regulates the cleavage furrow-specific vimentin phosphorylation in the cytokinetic process. (англ.) // The Journal of biological chemistry. — 2003. — Vol. 278, no. 10. — P. 8526—8530. — doi:10.1074/jbc.M210892200. — PMID 12458200.
- Kawajiri A., Yasui Y., Goto H., Tatsuka M., Takahashi M., Nagata K., Inagaki M. Functional significance of the specific sites phosphorylated in desmin at cleavage furrow: Aurora-B may phosphorylate and regulate type III intermediate filaments during cytokinesis coordinatedly with Rho-kinase. (англ.) // Molecular biology of the cell. — 2003. — Vol. 14, no. 4. — P. 1489—1500. — doi:10.1091/mbc.E02-09-0612. — PMID 12686604.
- Murata-Hori M., Fumoto K., Fukuta Y., Iwasaki T., Kikuchi A., Tatsuka M., Hosoya H. Myosin II regulatory light chain as a novel substrate for AIM-1, an aurora/Ipl1p-related kinase from rat. (англ.) // Journal of biochemistry. — 2000. — Vol. 128, no. 6. — P. 903—907. — PMID 11098131.
- Lens S. M., Wolthuis R. M., Klompmaker R., Kauw J., Agami R., Brummelkamp T., Kops G., Medema R. H. Survivin is required for a sustained spindle checkpoint arrest in response to lack of tension. (англ.) // The EMBO journal. — 2003. — Vol. 22, no. 12. — P. 2934—2947. — doi:10.1093/emboj/cdg307. — PMID 12805209.
- Ditchfield C., Johnson V. L., Tighe A., Ellston R., Haworth C., Johnson T., Mortlock A., Keen N., Taylor S. S. Aurora B couples chromosome alignment with anaphase by targeting BubR1, Mad2, and Cenp-E to kinetochores. (англ.) // The Journal of cell biology. — 2003. — Vol. 161, no. 2. — P. 267—280. — doi:10.1083/jcb.200208091. — PMID 12719470.
- Ryser S., Dizin E., Jefford C.E., Delaval B., Gagos S., Christodoulidou A., Krause K.H., Birnbaum D., Irminger-Finger I. Distinct roles of BARD1 isoforms in mitosis: full-length BARD1 mediates Aurora B degradation, cancer-associated BARD1beta scaffolds Aurora B and BRCA2 (англ.) // Cancer Res. : journal. — 2009. — February (vol. 69, no. 3). — P. 1125—1134. — doi:10.1158/0008-5472.CAN-08-2134. — PMID 19176389.
- Wheatley S.P., Carvalho A., Vagnarelli P., Earnshaw W.C. INCENP is required for proper targeting of Survivin to the centromeres and the anaphase spindle during mitosis (англ.) // Curr. Biol. : journal. — 2001. — June (vol. 11, no. 11). — P. 886—890. — doi:10.1016/S0960-9822(01)00238-X. — PMID 11516652.
- Chen J., Jin S., Tahir S.K., Zhang H., Liu X., Sarthy A.V., McGonigal T.P., Liu Z., Rosenberg S.H., Ng S.C. Survivin enhances Aurora-B kinase activity and localizes Aurora-B in human cells (англ.) // J. Biol. Chem. : journal. — 2003. — January (vol. 278, no. 1). — P. 486—490. — doi:10.1074/jbc.M211119200. — PMID 12419797.
- Sampath S.C., Ohi R., Leismann O., Salic A., Pozniakovski A., Funabiki H. The chromosomal passenger complex is required for chromatin-induced microtubule stabilization and spindle assembly (англ.) // Cell : journal. — Cell Press, 2004. — July (vol. 118, no. 2). — P. 187—202. — doi:10.1016/j.cell.2004.06.026. — PMID 15260989.
- Gassmann R., Carvalho A., Henzing A.J., Ruchaud S., Hudson D.F., Honda R., Nigg E.A., Gerloff D.L., Earnshaw W.C. Borealin: a novel chromosomal passenger required for stability of the bipolar mitotic spindle (англ.) // J. Cell Biol. : journal. — 2004. — July (vol. 166, no. 2). — P. 179—191. — doi:10.1083/jcb.200404001. — PMID 15249581.
- Delaval B., Ferrand A., Conte N., Larroque C., Hernandez-Verdun D., Prigent C., Birnbaum D. Aurora B -TACC1 protein complex in cytokinesis (англ.) // Oncogene. — 2004. — June (vol. 23, no. 26). — P. 4516—4522. — doi:10.1038/sj.onc.1207593. — PMID 15064709.
- Gürtler U., Tontsch-Grunt U., Jarvis M., Zahn S.K., Boehmelt G., Quant J., Adolf G.R., Solca F. Effect of BI 811283, a novel inhibitor of Aurora B kinase, on tumor senescence and apoptosis (англ.) // J. Clin. Oncol. : journal. — 2010. — Vol. 28, no. 15 Suppl e13632.
- Sorrentino R., Libertini S., Pallante P.L., Troncone G., Palombini L., Bavetsias V., Spalletti-Cernia D., Laccetti P., Linardopoulos S., Chieffi P., Fusco A., Portella G. Aurora B overexpression associates with the thyroid carcinoma undifferentiated phenotype and is required for thyroid carcinoma cell proliferation (англ.) // J. Clin. Endocrinol. Metab. : journal. — 2005. — Vol. 90, no. 2. — P. 928—935. — doi:10.1210/jc.2004-1518. — PMID 15562011.
Литература
- Nigg E.A. Mitotic kinases as regulators of cell division and its checkpoints (англ.) // Nat. Rev. Mol. Cell Biol. : journal. — 2001. — Vol. 2, no. 1. — P. 21—32. — doi:10.1038/35048096. — PMID 11413462.
- Shindo M., Nakano H., Kuroyanagi H. et al. cDNA cloning, expression, subcellular localization, and chromosomal assignment of mammalian aurora homologues, aurora-related kinase (ARK) 1 and 2 (англ.) // Biochem. Biophys. Res. Commun. : journal. — 1998. — Vol. 244, no. 1. — P. 285—292. — doi:10.1006/bbrc.1998.8250. — PMID 9514916.
- Tatsuka M., Katayama H., Ota T. et al. Multinuclearity and increased ploidy caused by overexpression of the aurora- and Ipl1-like midbody-associated protein mitotic kinase in human cancer cells (англ.) // Cancer Res. : journal. — 1998. — Vol. 58, no. 21. — P. 4811—4816. — PMID 9809983.
- Kimura M., Matsuda Y., Yoshioka T. et al. Identification and characterization of STK12/Aik2: a human gene related to aurora of Drosophila and yeast IPL1 (англ.) // Cytogenet. Cell Genet. : journal. — 1999. — Vol. 82, no. 3—4. — P. 147—152. — doi:10.1159/000015089. — PMID 9858806.
- Katayama H., Ota T., Morita K. et al. Human AIM-1: cDNA cloning and reduced expression during endomitosis in megakaryocyte-lineage cells (англ.) // Gene : journal. — Elsevier, 1999. — Vol. 224, no. 1—2. — P. 1—7. — doi:10.1016/S0378-1119(98)00522-8. — PMID 9931403.
- Prigent C., Gill R., Trower M., Sanseau P. In silico cloning of a new protein kinase, Aik2, related to Drosophila Aurora using the new tool: EST Blast (англ.) // In Silico Biol. (Gedrukt) : journal. — 2001. — Vol. 1, no. 2. — P. 123—128. — PMID 11471245.
- Wheatley S.P., Carvalho A., Vagnarelli P., Earnshaw W.C. INCENP is required for proper targeting of Survivin to the centromeres and the anaphase spindle during mitosis (англ.) // Curr. Biol. : journal. — 2001. — Vol. 11, no. 11. — P. 886—890. — doi:10.1016/S0960-9822(01)00238-X. — PMID 11516652.
- Zeitlin S.G., Shelby R.D., Sullivan K.F. CENP-A is phosphorylated by Aurora B kinase and plays an unexpected role in completion of cytokinesis (англ.) // J. Cell Biol. : journal. — 2002. — Vol. 155, no. 7. — P. 1147—1157. — doi:10.1083/jcb.200108125. — PMID 11756469.
- Crosio C., Fimia G.M., Loury R. et al. Mitotic Phosphorylation of Histone H3: Spatio-Temporal Regulation by Mammalian Aurora Kinases (англ.) // Mol. Cell. Biol. : journal. — 2002. — Vol. 22, no. 3. — P. 874—885. — doi:10.1128/MCB.22.3.874-885.2002. — PMID 11784863.
- Goto H., Yasui Y., Nigg E.A., Inagaki M. Aurora-B phosphorylates Histone H3 at serine28 with regard to the mitotic chromosome condensation (англ.) // Genes Cells : journal. — 2002. — Vol. 7, no. 1. — P. 11—7. — doi:10.1046/j.1356-9597.2001.00498.x. — PMID 11856369.
- Gigoux V., L'Hoste S., Raynaud F. et al. Identification of Aurora kinases as RasGAP Src homology 3 domain-binding proteins (англ.) // J. Biol. Chem. : journal. — 2002. — Vol. 277, no. 26. — P. 23742—23746. — doi:10.1074/jbc.C200121200. — PMID 11976319.
- Sugiyama K., Sugiura K., Hara T. et al. Aurora-B associated protein phosphatases as negative regulators of kinase activation (англ.) // Oncogene : journal. — 2002. — Vol. 21, no. 20. — P. 3103—3111. — doi:10.1038/sj.onc.1205432. — PMID 12082625.
- Chen J., Jin S., Tahir S.K. et al. Survivin enhances Aurora-B kinase activity and localizes Aurora-B in human cells (англ.) // J. Biol. Chem. : journal. — 2003. — Vol. 278, no. 1. — P. 486—490. — doi:10.1074/jbc.M211119200. — PMID 12419797.
- Morrison C., Henzing A.J., Jensen O.N. et al. Proteomic analysis of human metaphase chromosomes reveals topoisomerase II alpha as an Aurora B substrate (англ.) // Nucleic Acids Res. : journal. — 2002. — Vol. 30, no. 23. — P. 5318—5327. — doi:10.1093/nar/gkf665. — PMID 12466558.
- Strausberg R.L., Feingold E.A., Grouse L.H. et al. Generation and initial analysis of more than 15,000 full-length human and mouse cDNA sequences (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2003. — Vol. 99, no. 26. — P. 16899—16903. — doi:10.1073/pnas.242603899. — PMID 12477932.
- Kawajiri A., Yasui Y., Goto H. et al. Functional Significance of the Specific Sites Phosphorylated in Desmin at Cleavage Furrow: Aurora-B May Phosphorylate and Regulate Type III Intermediate Filaments during Cytokinesis Coordinatedly with Rho-kinase (англ.) // Molecular Biology of the Cell : journal. — 2003. — Vol. 14, no. 4. — P. 1489—1500. — doi:10.1091/mbc.E02-09-0612. — PMID 12686604.
- Minoshima Y., Kawashima T., Hirose K. et al. Phosphorylation by aurora B converts MgcRacGAP to a RhoGAP during cytokinesis (англ.) // Dev. Cell : journal. — 2003. — Vol. 4, no. 4. — P. 549—560. — doi:10.1016/S1534-5807(03)00089-3. — PMID 12689593.
- Honda R., Körner R., Nigg E.A. Exploring the Functional Interactions between Aurora B, INCENP, and Survivin in Mitosis (англ.) // Molecular Biology of the Cell : journal. — 2004. — Vol. 14, no. 8. — P. 3325—3341. — doi:10.1091/mbc.E02-11-0769. — PMID 12925766.
- Tien A.C., Lin M.H., Su L.J. et al. Identification of the substrates and interaction proteins of aurora kinases from a protein-protein interaction model (англ.) // Mol. Cell Proteomics : journal. — 2004. — Vol. 3, no. 1. — P. 93—104. — doi:10.1074/mcp.M300072-MCP200. — PMID 14602875.