Гистоны
Гисто́ны (от греч. ἱστός «ткань») — обширный класс ядерных белков, выполняющих две основные функции: они участвуют в упаковке нитей ДНК в ядре и в эпигенетической регуляции таких ядерных процессов, как транскрипция, репликация и репарация. Существует пять различных типов гистонов H1/Н5, H2A, H2B, H3, H4. Гистоны H2A, H2B, H3, H4, называемые кóровыми гистонами (от англ. core «сердцевина; ядро»), формируют нуклеосому, представляющую собой белковую глобулу, вокруг которой накручена нить ДНК. Гистон H1/H5, называемый линкерным гистоном (от англ. link «связь»), связывается с внешней стороной нуклеосомы, фиксируя на ней нить ДНК. В хроматине гистоны составляют 25—40 % сухого веса[1]. Благодаря высокому содержанию лизина и аргинина гистоны проявляют сильно оснóвные свойства. Гистоны непосредственно контактируют с ДНК и способны нейтрализовать отрицательный заряд фосфатных групп ДНК за счёт положительных зарядов аминокислотных остатков. Последовательность аминокислот в этих белках является консервативной и практически не различается в организмах различных таксонов. Гистоны присутствуют в ядрах эукариотических клеток; у бактерий гистонов нет, но они выявлены у архей группы Euryarchaea[2].

Гистоны обнаружены в 1884 году немецким биохимиком Альбрехтом Косселем[3].
Структура нуклеосомы и гистоновых белков

По две молекулы каждого из гистонов Н2А, Н2В, Н3 и Н4 составляют октамер, обвитый сегментом ДНК длиной 146 пар оснований (п.о.), образующим 1,8 витка спирали поверх белковой структуры. Эта частица диаметром 7 нм называется нуклеосомой. Участок ДНК, соединяющий соседние нуклеосомы и непосредственно не контактирующий с гистоновым октамером, взаимодействует с линкерным гистоном Н1. Длина фрагмента ДНК, приходящегося на одну нуклеосому, варьирует и составляет в среднем 200 п.о. При этом непосредственно с нуклеосомой связаны 146 п.о., а остальные несколько десятков соединяют две соседние нуклеосомы[4].
ДНК и нуклеосомные гистоны прочно соединены: в каждой нуклеосоме между ДНК и гистонами, входящими в её состав, образуется 142 водородные связи. Почти половина этих связей возникает между основной цепью аминокислот гистонов и фосфодиэфирными группами сахарнофосфатного остова ДНК. Помимо водородных связей ДНК с белками, нуклеосомы скрепляют многочисленные гидрофобные взаимодействия и солевые мостики. Например, положительные заряды аминокислот лизина и аргинина, которыми обогащены гистоны, могут эффективно нейтрализовать отрицательный заряд остова ДНК. Эти многочисленные взаимодействия отчасти объясняют, почему ДНК практически любой последовательности может быть связана с нуклеосомным октамером[5].
Структура кóровых гистонов
Кóровые гистоны Н2А, Н2В, Н3 и Н4 являются небольшими белками с молекулярными массами 10—15 кДа, состав которых чрезвычайно обогащён положительно заряженными аминокислотами лизином и аргинином[6]. Положительно заряженные аминокислоты сосредоточены в основном в аминных (N-) и карбоксильных (C-) (см. Пептидная связь) концевых частях молекул коровых гистонов, называемых хвостами. Гистоновые хвосты длиной около 15—30 аминокислотных остатков не организованы в какие-либо выраженные вторичные структуры. Гистоновые хвосты, прежде всего N-хвост, играют ключевую роль в эпигенетических механизмах, в которых участвуют эти белки. В центральных, самых консервативных, участках полипептидной цепи кóровых гистонов преобладают остатки гидрофобных аминокислот. Именно эти центральные области участвуют в образовании нуклеосомного октамера, на который навивается ДНК[3]. Центральная область всех нуклеосомных гистонов имеет характерную вторичную структуру с протяжённым α-спиральным доменом, который с обеих сторон фланкируется доменами, содержащими по одной петле и по одной короткой α-спирали. Эта пространственная структура называется гистоновой складкой (англ. histone fold domain, HFD)[7]. Таким образом, нуклеосомные гистоны содержат центральный структурированный трехспиральный HFD-домен и неструктурированные N- и C-хвосты.

Гистоны H3 и H4, Н2А и H2B попарно узнают друг друга. Спиральные домены взаимодействуют между собой, образуя структуры, названные рукопожатием, в результате чего возникают гетеродимеры — Н3-Н4 и Н2А-Н2В. Из первого димера, в свою очередь, образуется тетрамер (Н3-Н4)2. Тетрамер (Н3-Н4)2 и два димера Н2А-Н2В составляют гистоновый октамер, сердцевину нуклеосомы[3]. Нуклеосома имеет клиновидную форму. Её узкую часть составляет (Н3-Н4)2, а широкая часть состоит из двух димеров Н2А-Н2В, которые расположены по бокам тетрамера (Н3-Н4)2 и не взаимодействуют друг с другом. Из всей ДНК, что намотана на нуклеосомный октамер, примерно 80 пар оснований связаны с тетрамером (Н3-Н4)2 и около 40 пар с димерами Н2А-Н2В[7].
Структура линкерного гистона H1/Н5
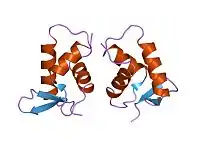
С внешней стороной нуклеосомы в районе тетрамера (Н3-Н4)2 связывается линкерный гистон H1, фиксирующий тем самым на нуклеосоме нить ДНК. В эритроцитах птиц и рептилий в неактивном хроматине вместо гистона Н1 присутствует близкородственный гистон Н5[7]. Гистон Н1/Н5 существенно отличается от четырёх коровых гистонов. Он имеет молекулярную массу более 20 кДа. В его составе значительно больше остатков лизина, чем аргинина, причём все положительно заряженные аминокислотные остатки сконцентрированы на С-конце молекулы Н1. С-конец молекулы Н1 характеризуется неупорядоченной структурой и имеет длину около 100 аминокислотных остатков. Центральная часть молекулы Н1 богата гидрофобными аминокислотными остатками и в растворе образует глобулу. N-конец не имеет упорядоченной структуры и является относительно коротким[6].
Варианты гистонов
Каждый тип гистонов, кроме гистона H4, представляет собой группу, состоящую из канонических гистонов и гистоновых вариантов.
Роль гистоновых вариантов состоит в том, чтобы сохраняя нуклеосомную укладку хроматина, увеличивать или уменьшать её устойчивость, создавать особый контекст в каждом конкретном участке хроматина и тем самым управлять процессами транскрипции, репликации и репарации[7].
Гены гистонов
Гены классических гистонов присутствуют в геноме в нескольких копиях и собраны в тандемно повторённые кластеры. Кластерная организация генов канонических гистонов характерна для всех многоклеточных. У человека самый большой кластер этих генов, называемый HIST1 и состоящий из 55 генов, находится на хромосоме 6 в участке 6p21-p22. Два кластера меньших размеров находятся на хромосоме 1: в бэнде 1q21 находится кластер HIST2, содержащий 6 гистоновых генов, а в бэнде 1q42 находится кластер HIST3, состоящий из трёх генов. Вне трёх вышеописанных кластеров на хромосоме 12 в бэнде 12p13.1 находится единственный ген, кодирующий канонический коровый гистон, — ген HIST4H4, кодирующий гистон H4[8].
Характерной чертой генов канонических гистонов является отсутствие интронов. Транскрипция этих генов происходит строго во время S-фазы клеточного цикла. Матричная РНК этих генов не полиаденилируется, 3'-некодирующая часть мРНК уложена во вторичную структуру типа «стебель-петля»[9].
В противоположность генам канонических гистонов гены вариантных гистонов не образуют кластеров, они разбросаны по всему геному, нередко содержат интроны, транскрибируемая с них РНК полиаденируется, транскрипция происходит во время всего клеточного цикла.
| Суперсемейство | Семейство | Подсемейство | Гены |
|---|---|---|---|
| Линкерный гистон | |||
| Гистон Н1 | |||
| Вариантные гистоны H1 (подсемейство H1F) | H1F0, H1FNT, H1FOO, H1FX, HILS1 | ||
| Гены канонического гистона H1 в кластере HIST1 (H1H1) | HIST1H1A, HIST1H1B, HIST1H1C, HIST1H1D, HIST1H1E, HIST1H1T | ||
| Коровые гистоны | |||
| Гистон H2A | |||
| Вариантные гистоны H2A (H2AF) | H2AFB1, H2AFB2, H2AFB3, H2AFJ, H2AFV, H2AFX, H2AFY, H2AFY2, H2AFZ | ||
| Гены канонического гистона H2A в кластере HIST1 (H2A1) | HIST1H2AA, HIST1H2AB, HIST1H2AC, HIST1H2AD, HIST1H2AE, HIST1H2AG, HIST1H2AI, HIST1H2AJ, HIST1H2AK, HIST1H2AL, HIST1H2AM | ||
| Гены канонического гистона H2A в кластере HIST2 (H2A2) | HIST2H2AA3, HIST2H2AC | ||
| Гистон H2B | |||
| Вариантные гистоны H2B (H2BF) | H2BFM, H2BFS, H2BFWT | ||
| Гены канонического гистона H2B в кластере HIST1 (H2B1) | HIST1H2BA, HIST1H2BB, HIST1H2BC, HIST1H2BD, HIST1H2BE, HIST1H2BF, HIST1H2BG, HIST1H2BH, HIST1H2BI, HIST1H2BJ, HIST1H2BK, HIST1H2BL, HIST1H2BM, HIST1H2BN, HIST1H2BO | ||
| Ген канонического гистона H2A в кластере HIST2 (H2B2) | HIST2H2BE | ||
| Гистон H3 | |||
| Гены канонического гистона H3 в кластере HIST1 (H3A1) | HIST1H3A, HIST1H3B, HIST1H3C, HIST1H3D, HIST1H3E, HIST1H3F, HIST1H3G, HIST1H3H, HIST1H3I, HIST1H3J | ||
| Гены канонического гистона H3 в кластере HIST2 (H3A2) | HIST2H3C | ||
| Гены канонического гистона H3 в кластере HIST3 (H3A3) | HIST3H3 | ||
| Гистон H4 | |||
| Гены канонического гистона H4 в кластере HIST1 (H41) | HIST1H4A, HIST1H4B, HIST1H4C, HIST1H4D, HIST1H4E, HIST1H4F, HIST1H4G, HIST1H4H, HIST1H4I, HIST1H4J, HIST1H4K, HIST1H4L | ||
| Ген канонического гистона H4 вне кластеров | HIST4H4 |
Модификации гистонов
Гистоны в октамере имеют подвижный N-концевой фрагмент («хвост») из 20 аминокислот, который выступает из нуклеосом и важен для поддержания структуры хроматина и контроля над генной экспрессией. Так, например, некоторые модификации гистонов (фосфорилирование и ацетилирование), как известно, локализованы преимущественно на участках хроматина с активными генами[10][11], тогда как их деацетилирование[12] и метилирование репрессорным комплексом поликомб играют важную роль в поддержании плюрипотентности и дифференцировке[13].
Детали механизма регуляции до конца не выяснены[14][15][16].
Консервативность гистонов
Последовательность аминокислот гистонов, то есть их первичная структура, мало изменилась в процессе эволюции. Это хорошо видно при сравнении аминокислотной последовательности гистонов млекопитающих, растений и дрожжей. Так, Н4 человека и пшеницы отличаются лишь несколькими аминокислотами. К тому же размер молекулы белка и её полярность довольно постоянны. Из этого можно заключить, что гистоны были оптимизированы ещё в эпоху общего предшественника животных, растений и грибов (более 700 млн лет назад). Хотя с тех пор в гистоновых генах происходили бесчисленные точечные мутации, все они, очевидно, приводили к вымиранию мутантных организмов.
См. также
Примечания
- Биологический энциклопедический словарь / Гл.ред. М.С.Гиляров. — М.: Сов. энциклопедия, 1986. — 831 с.
- Нуклеиновые кислоты: от А до Я / Б. Аппель [и др.]. — М.: Бином: Лаборатория знаний, 2013. — 413 с. — 700 экз. — ISBN 978-5-9963-0376-2.
- Карпов В.Л. От чего зависит судьба гена // Природа. — Наука, 2005. — № 3. — С. 34—43.
- Коряков Д. Е. Модификации гистонов и регуляция работы хроматина // Генетика. — 2006. — Т. 42, № 9. — С. 1170—1185.
- Молекулярная биология клетки: в 3-х томах / Б. Альбертс, А. Джонсон, Д. Льюис и др. — М.-Ижевск: НИЦ «Регулярная и хаотическая динамика», Институт компьютерных исследований, 2013. — Т. I. — С. 325—359. — 808 с. — ISBN 978-5-4344-0112-8.
- Разин С. В. Хроматин: упакованный геном / С. В. Разин, А. А. Быстрицкий. — М.: БИНОМ: Лаборатория знаний, 2009. — С. 4-8. — 176 с. — ISBN 978-5-9963-0087-7.
- Коряков Д. Е. Нуклеосомная организация хроматина // Эпигенетика / С. М. Закиян, В.В. Власов, Е. В. Дементьева. — Новосибирск: Изд-во СО РАН, 2012. — С. 7—30. — 592 с. — 300 экз. — ISBN 978-5-7692-1227-7.
- Marzluff W. F., Gongidi P., Woods K. R., Jin J., Maltais L. J. The human and mouse replication-dependent histone genes (англ.) // Genomics : journal. — Academic Press, 2002. — November (vol. 80, no. 5). — P. 487—498. — PMID 12408966. Архивировано 5 марта 2016 года. Архивированная копия (недоступная ссылка). Дата обращения: 14 июля 2013. Архивировано 5 марта 2016 года.
- Marzluff W. F., Wagner E. J., Duronio R. J. Metabolism and regulation of canonical histone mRNAs: life without a poly(A) tail (англ.) // Nat. Rev. Genet. : journal. — 2008. — November (vol. 9, no. 11). — P. 843—854. — doi:10.1038/nrg2438. — PMID 18927579.
- Zheng Y. et al. Histone H1 phosphorylation is associated with transcription by RNA polymerases I and II (англ.) // The Journal of Cell Biology. — 2010. — Vol. 189, iss. 3. — P. 407. — doi:10.1083/jcb.201001148.
- Creyghton M. P. et al. Histone H3K27ac separates active from poised enhancers and predicts developmental state (англ.) // Proc Natl Acad Sci U S A. — 2010. — Vol. 107, iss. 50. — P. 21931—21936. — doi:10.1073/pnas.1016071107.
- Guang Hu, Paul A. Wade. NuRD and Pluripotency: A Complex Balancing Act (англ.) // Cell Stem Cell. — 2012. — Vol. 10, iss. 5. — P. 497—503. — doi:10.1016/j.stem.2012.04.011.
- Gerasimova A. et al. Predicting Cell Types and Genetic Variations Contributing to Disease by Combining GWAS and Epigenetic Data (англ.) // PLOS One. — Public Library of Science, 2013. — Vol. 8, iss. 1. — P. e54359. — doi:10.1371/journal.pone.0054359.
- Pengelly A. R. et al. A Histone Mutant Reproduces the Phenotype Caused by Loss of Histone-Modifying Factor Polycomb (англ.) // Science. — 2013. — Vol. 339, iss. 6120. — P. 698. — doi:10.1126/science.1231382.
- Histone Modification Controls Development: Chemical Tags On Histones Regulate Gene Activity
- Moyra Lawrence, Sylvain Daujat, Robert Schneider. How Histone Modifications Regulate Gene Expression (англ.) // Trends in Genetics. — Cell Press, 2015. — Vol. 32, iss. 1. — P. 42—56. — doi:10.1016/j.tig.2015.10.007.
Ссылки
- HistoneDB 2.0 — Database of histones and variants at NCBI (англ.)
- Chromatin, Histones & Cathepsin; the proteolysis map (PMAP) — animation (англ.)
