Бактериохлорофиллы
Бактериохлорофи́ллы — гетерогенная группа фотосинтетических тетрапиррольных пигментов, которые синтезируются различными аноксигенными фототрофными бактериями, осуществляющими фотосинтез без выделения кислорода.
Спектральные свойства бактериохлорофиллов в клетках значительно отличаются от растворов, и определяются нековалентными взаимодействиями их молекул с содержащими их белками, а также друг с другом.
Химическая структура бактериохлорофиллов
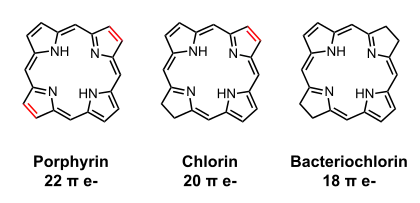
Бактериохлорофиллы a, b и g являются бактериохлоринами, то есть содержат в своём составе бактериохлориновый макроцикл с двумя восстановленными пиррольными кольцами (II и IV).
Бактериохлорофиллы с-f, как и хлорофиллы, имеют хлориновое макроцикловое кольцо с единственным полностью восстановленным пиррольным кольцом IV. В отличие от всех остальных хлорофиллов и бактериохлорофиллов, у них отсутствует остаток -COOCH3 в положении R5, характерный для всех прочих хлорофиллов и бактериохлорофиллов. Каждый из этих бактериохлорофиллов имеет несколько форм, отличающихся радикалами R3 и R4, a также этерифицирующим спиртом R5[1][2].
| Название | Структура | R1 | R2 | R3 | Связь С7-С8 | R4 | R5 | R6 | R7 |
|---|---|---|---|---|---|---|---|---|---|
| Бактериохлорофилл a |  |
–CO–CH3 | –CH3a | –CH2CH3 | одинарная | -CH3 | -CO-O-CH3 | -фитил
-геранилгеранил |
-H |
| Бактериохлорофилл b | -CO-CH3 | -CH3a | =CH-CH3 | одинарная | –CH3 | –CO–O–CH3 | –фитил | –H | |
| Бактериохлорофилл c | –CHOH–CH3 | –CH3 | –C2H5b –C3H7 –C4H9 |
двойная | –CH3 –C2H5 |
–H | –фарнезил и др. | –CH3 | |
| Бактериохлорофилл d | –CHOH–CH3 | –CH3 | –C2H5b –C3H7 –C4H9 |
двойная | –CH3 –C2H5 |
–H | –фарнезил и др. | –H | |
| Бактериохлорофилл e | –CHOH–CH3 | –CHO | –C2H5b –C3H7 –C4H9 |
двойная | –CH3 –C2H5 |
–H | –фарнезил и др. | –CH3 | |
| Бактериохлорофилл f | –CHOH–CH3 | –CHO | –C2H5b –C3H7 –C4H9 |
двойная | ––CH3 –C2H5 |
–H | –фарнезил и др. | –H | |
| Бактериохлорофилл g | –CH=CH2 | –CH3a | =СH-CH2 | одинарная | –CH3 | –CO–O–CH3 | –геранилгеранил | –H | |
Химические свойства
Бактериохлорофиллы неустойчивы к действию света, кислот и окислителей. В полярных растворителях (например, в метаноле) они легко подвергаются алломеризации; в присутствии кислот – теряют центральный атом магния (феофитинизируются) и/или этерифицирующий остаток (фитол/фарнезол/геранилгериниол и др.)[3].
Бактериохлорофиллы b и g, имеющие этилиденовый остаток при С-8, в слабокислой среде изомеризуются с образованием хлоринов. Особенно легко изомеризуется бактериохлорофилл g, превращающийся в результате в хлорофилл аG[4].
Под действием кислорода в молекулах бактериохлорофиллов происходит окислительный разрыв пятичленного кольца V; в дальнейшем образовавшиеся кислотные остатки у атомов с-13 и С-14 могут вновь замкнуться в шестичленное ангидридное кольцо с образованием бактериопурпуринов или пурпуринов[3][5].
Биосинтез
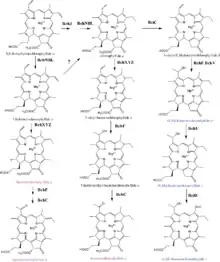
Упрощенная схема биосинтеза бактериохлорофиллидов a, b и g, а также (E,M)-бактериохлорофиллидов с-e[6][7], показана на рисунке.
Ранее предполагалось, что первая стадия биосинтеза бактериохлорофиллов с-e, образование кольца V без карбоксиметильного заместителя при С132, может происходить еще до образования 3,8-дивинил-протохлорофиллида a[8]. В настоящее время это считается маловероятным[6][9].
Последняя ступень биосинтеза, превращение бактериохлорофиллидов в бактериохлорофиллы, осуществляется с помощью эстераз, кодируемых генами BchG у бактериохлорофиллов a, b и g и BchK у хлоробиум-хлорофиллов. В синтезе метилированных форм бактериохлорофиллов с-e принимают участие также метилаза С121-углерода BchR и С82-метилаза BchQ. Их субстратами, по-видимому, служат любые хлорофиллиды с гидроксиметильным остатком при С3, то есть метилирование может происходить на любом этапе после образования 8-этил-12-метил-бактериохлорофиллида d.
Распространение
Наиболее широко распространенный пигмент аноксигенных фототрофных бактерий - бактериохлорофилл а. Он является преобладающим хлориновым пигментом в реакционных центрах большинства фототрофных протеобактерий, у всех зеленых серобактерий (Сhlorobiaceae) и нитчатых аноксигенных фототрофов (Chloroflexiа). У немногих фототрофных протеобактерий бактериохлорофилл а полностью замещается бактериохлорофиллом b. Бактериохлорофилл g обнаружен только у одной небольшой по количеству видов и распространению группы бактерий, гелиобактерий.
Бактериохлорофиллы с-f присутствуют исключительно в хлоросомах, особых фотосинтетических антенных комплексах, имеющихся у всех зелёных серных бактерий (Chlorobiales), некоторых нитчатых аноксигенных фототрофов (Chloroflexia), а также у недавно обнаруженной фотогетеротрофной ацидобактерии Chloracidobacterium thermophilum[10].
| Пигмент | Группа бактерий | Максимум инфракрасного поглощения in vivo (нм) |
|---|---|---|
| Бактериохлорофилл a | Пурпурные бактерии (большинство),Chlorobiaceae, Chloroflexales и Chloracidobacterium thermophilum | 805-815, 830—890 |
| Бактериохлорофилл b | Пурпурные бактерии (некоторые) | 835-850, 1020—1040 |
| Бактериохлорофилл c | Chlorobiaceae (зеленые штаммы) большинство Chloroflexia, Chloracidibacterium thermophilum | 745-755 |
| Бактериохлорофилл d | зеленые штаммы Chlorobiaceae, Chloronema (Chloroflexia) | 705-740 |
| Бактериохлорофилл e | коричневые штаммы Chlorobiaceae | 719-726 |
| Бактериохлорофилл f | некоторые лабораторные штаммы Chlorobiaceae | ~705-707 |
| Бактериохлорофилл g | Гелиобактерии | 670-788 |
Примечания
- Scheer, H. (2006). An overview of chlorophylls and bacteriochlorophylls: biochemistry, biophysics, functions and applications In: B. Grimm et al. (eds): Chlorophylls and Bacteriochlorophylls. Springer Netherlands. (pp. 1-26)
- Orf, G. S., Blankenship, R. E. (2013). Chlorosome antenna complexes from green photosynthetic bacteria. Photosynthesis research, 116 (2-3), p. 15-331.
- Keely, B. J. (2006). Geochemistry of chlorophylls. In Chlorophylls and Bacteriochlorophylls (pp. 535-561). Springer Netherlands.
- Kobayashi, M., Hamano, T., Akiyama, M., Watanabe, T., Inoue, K., Oh-oka, H., Amesz J., Yamamura M., Kise, H. (1998). Light-independent isomerization of bacteriochlorophyll g to chlorophyll a catalyzed by weak acid in vitro. Analytica chimica acta, 365(1), 199-203.
- Grin, M. A., & Mironov, A. F. (2008). Synthetic and Natural Bacteriochlorins: Synthesis, Properties and Applications. In: Chemical Processes with Participation of Biological and Related Compounds: Biophysical and Chemical Aspects of Porphyrins, Pigments, Drugs, Biodegradable Polymers and Nanofibers, 5.
- Liu, Z., & Bryant, D. A. (2011). Identification of a gene essential for the first committed step in the biosynthesis of bacteriochlorophyll c. Journal of Biological Chemistry, 286(25), 22393-22402.
- Tsukatani Y., Yamamoto H., Harada J., Yoshitomi T., Nomata J., Kasahara M., Mizoguchi T., Fujita Y., Tamiaki H. (2013). An unexpectedly branched biosynthetic pathway for bacteriochlorophyll b capable of absorbing near-infrared light. Scientific reports, 3.
- Frigaard, N. U., Chew, A. G. M., Maresca, J. A., & Bryant, D. A. (2006). Bacteriochlorophyll biosynthesis in green bacteria. In Chlorophylls and Bacteriochlorophylls (pp. 201-221). Springer Netherlands.
- Harada, J., Teramura, M., Mizoguchi, T., Tsukatani, Y., Yamamoto, K., & Tamiaki, H. (2015). Stereochemical conversion of C3‐vinyl group to 1‐hydroxyethyl group in bacteriochlorophyll c by the hydratases BchF and BchV: adaptation of green sulfur bacteria to limited‐light environments. Molecular microbiology, 98(6), 1184-1198.
- Bryant, Donald A.; Costas, AM; Maresca, JA & Chew, AG (2007-07-27), Candidatus Chloracidobacterium thermophilum: An Airobic Phototrophic Acidobacterium, Science Т. 317 (5837): 523–526, PMID 17656724, doi:10.1126/science.1143236, <http://www.sciencemag.org/cgi/content/abstract/317/5837/523>