GLUT4
GLUT4 (ГЛЮТ-4, глюкозный транспортёр тип 4) — инсулинзависимый белок-переносчик глюкозы, осуществляет перенос глюкозы, посредством облегчённой диффузии через клеточную мембрану под контролем инсулина. Содержится в отсутствии инсулина почти полностью в цитоплазме[1]. Впервые был обнаружен в клетках жировой ткани и мышечной ткани (скелетные мышцы и миокард). Свидетельство об открытии нового глюкозного транспортёра принадлежит цитологу Дэвиду Джеймсу, который предоставил его в 1988 году[2]. Ген, кодирующий GLUT4 был клонирован[3][4] и картирован в 1989[5]. Ген, кодирующий данный белок у человека — SLC2A4, расположен в 17 хромосоме.
GLUT4 — единственный инсулинзависимый глюкозный транспортёр.
Недавние сообщения показали наличие гена GLUT4 в некоторых участках центральной нервной системы, таких как гиппокамп. Кроме того, ухудшение в инсулинстимулированном обороте GLUT4 в гиппокампе, может привести к снижению метаболической активности и пластичности нейронов гиппокампа, проявляющихся в депрессивных, поведенческих и когнитивных дисфункциях[6][7][8].
Локализация в органах
GLUT4 локализован в следующих органах:
- жировая ткань
- скелетные мышцы
- сердечная мышца (миокард)
Доменная структура
GLUT4 представляет собой трансмембранный белок, состоящий из 509 аминокислотных остатков. Четвертичная структура включает в себя 12 трансмембранных доменов. N- и С-концевая части располагаются внутри цитоплазмы.
Выполняемые функции
Перенос глюкозы во внутриклеточное пространство, посредством инсулинстимулированного сигнала.
Регуляция
Осуществляется непосредственно инсулином.
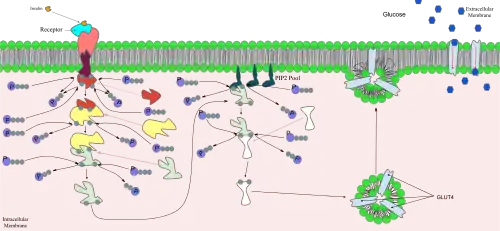
В условиях низкого инсулина в клетках жировой и мышечной ткани большинство молекул GLUT4 (более 90 %) отделены от цитоплазматической мембраны в виде внутриклеточных везикул, состоящих из белков, таких как инсулинзависимая аминопептидаза, везикулярного белка — синаптобревина (известный ещё как v-SNARE) и небольшого ГТФ-связывающего белка — Rab-4. При воздействии инсулина начинается процесс быстрой транслокации (перемещения) везикул ГЛЮТ-4 к цитоплазматической мембране, где они закрепляются, образуя комплексы, включающие трансмембранный белок синтаксин-4 (известный как t-SNARE) и синаптобревин. Происходит процесс сливания везикул с цитоплазматической мембраной, увеличивая количество молекул ГЛЮТ-4 в ней и тем самым увеличивается скорость процесса переноса глюкозы внутрь клетки. ГТФ-связывающий белок Rab-4 покидает везикулу и движется в цитоплазму в ответ на стимуляцию инсулином. Как только происходит устранение инсулинового сигнала ГЛЮТ-4 интернализуется (передвигается внутрь), отпочковываясь в виде везикул окаймлённых клатрином, от цитоплазматической мембраны. ГЛЮТ-4 сравнительно легко проникают внутрь эндосомы, где происходит их ресортировка во внутриклеточные ГЛЮТ-4 содержащие везикулы.
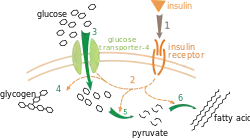
Инсулин связывается с инсулиновым рецептором, который представляет собой тирозиновую протеинкиназу, то есть протеинкиназу, которая фосфорилирует как внутриклеточные домены рецептора по гидроксильной ОН-группе остатков тирозина (происходит так называемое аутофосфорилирование субстрата инсулинового рецептора IRS-1), так и внутриклеточные белки. Аутофосфорилирование субстрата инсулинового рецептора IRS-1 ведёт к усилению первичного сигнала. Эти субстраты образуют комплексы например с фосфоинозитид-3-киназой (ФИ-3-киназа, КФ 2.7.1), точнее с одной из регуляторных субъединиц (p85α), посредством SH2-доменов. Затем субъединица p85α связывается с каталитической субъединицой p110. Активация ФИ-3-киназы является звеном сигнального пути, стимулирующего транслокацию ГЛЮТ-4 из цитоплазмы в плазматическую мембрану, а следовательно — и трансмембранный перенос глюкозы в мышечные и жировые клетки.
На поверхности клетки, GLUT4 позволяет глюкозе, посредством облегчённой диффузии по градиенту концентрации проникать в мышечные и жировые клетки. После того, как глюкоза окажется внутри клетки, она быстро фосфорилируется глюкокиназами в печени или гексокиназами в других тканях, с образованием глюкозо-6-фосфата, который затем участвует либо в процессе гликолиза либо полимеризуется в гликоген. Глюкозо-6-фосфат не может диффундировать обратно из клеток, что также служит для поддержания градиента концентрации по отношению к глюкозе, чтобы она смогла диффундировать внутрь клетки, посредством пассивного транспорта[9].
Нарушения
Существуют несколько видов нарушений. Это генетические, связанные с мутациями в гене SLC2A4 и, последующей его экспрессией мутантного белка, и функциональные, связанные с нарушениями выполняемых функций.
Нарушения функции ГЛЮТ-4 возможны на следующих этапах:
- передача сигнала инсулина о перемещении этого транспортёра к мембране;
- перемещение транспортёра в цитоплазме;
- включение в состав мембраны;
- отшнуровывание от мембраны и другие.
Все они могут привести к развитию инсулиновой резистентности и, последующим развитием сахарного диабета 2 типа.
Взаимодействия с другими белками
Недавние исследования показали, что GLUT4 взаимодействует с так называемым Death-ассоциированным протеином 6 — DAXX[10].
Примечания
- Е.С. Северин. Биология. — М.: ГЭОТАР-МЕД, 2004. — 779 с. — ISBN 5-9231-0254-4.
- James D.E., Brown R., Navarro J., Pilch P.F. Insulin-regulatable tissues express a unique insulin-sensitive glucose transport protein (фр.) // Nature : magazine. — 1988. — Mai (vol. 333, no 6169). — P. 183—185. — doi:10.1038/333183a0. — PMID 3285221.
- James D.E., Strube M., Mueckler M. Molecular cloning and characterization of an insulin-regulatable glucose transporter (англ.) // Nature : journal. — 1989. — March (vol. 338, no. 6210). — P. 83—7. — doi:10.1038/338083a0. — PMID 2645527.
- Birnbaum M.J. Identification of a novel gene encoding an insulin-responsive glucose transporter protein (англ.) // Cell. — Cell Press, 1989. — April (vol. 57, no. 2). — P. 305—315. — doi:10.1016/0092-8674(89)90968-9. — PMID 2649253.
- Bell G.I., Murray J.C., Nakamura Y., Kayano T., Eddy R.L., Fan Y.S., Byers M.G., Shows T.B. Polymorphic human insulin-responsive glucose-transporter gene on chromosome 17p13 (англ.) // Diabetes : journal. — 1989. — August (vol. 38, no. 8). — P. 1072—1075. — doi:10.2337/diabetes.38.8.1072. — PMID 2568955.
- Patel S.S., Udayabanu M. Urtica dioica extract attenuates depressive like behavior and associative memory dysfunction in dexamethasone induced diabetic mice (англ.) // Metabolic Brain Disease : journal. — 2014. — March (vol. 29, no. 1). — P. 121—130. — doi:10.1007/s11011-014-9480-0. — PMID 24435938.
- Piroli G.G., Grillo C.A., Reznikov L.R., Adams S., McEwen B.S., Charron M.J., Reagan L.P. Corticosterone impairs insulin-stimulated translocation of GLUT4 in the rat hippocampus (англ.) // Neuroendocrinology : journal. — 2007. — Vol. 85, no. 2. — P. 71—80. — doi:10.1159/000101694. — PMID 17426391.
- Huang C.C., Lee C.C., Hsu K.S. The role of insulin receptor signaling in synaptic plasticity and cognitive function (англ.) // Chang Gung Medical Journal : journal. — 2010. — Vol. 33, no. 2. — P. 115—125. — PMID 20438663.
- Watson R.T., Kanzaki M., Pessin J.E. Regulated membrane trafficking of the insulin-responsive glucose transporter 4 in adipocytes (англ.) // Endocrine Reviews : journal. — Endocrine Society, 2004. — April (vol. 25, no. 2). — P. 177—204. — doi:10.1210/er.2003-0011. — PMID 15082519.
- Lalioti V.S., Vergarajauregui S., Pulido D., Sandoval I.V. The insulin-sensitive glucose transporter, GLUT4, interacts physically with Daxx. Two proteins with capacity to bind Ubc9 and conjugated to SUMO1 (англ.) // Journal of Biological Chemistry : journal. — 2002. — May (vol. 277, no. 22). — P. 19783—19791. — doi:10.1074/jbc.M110294200. — PMID 11842083.