Фенолокислоты
Фенолокислоты — производные ароматических углеводородов, в молекулах которых атомы водорода бензольного ядра замещены на карбоксильные (-СООН) и гидроксильные (-ОН) группы. Их иногда рассматривают как ароматические кислоты, в молекулах которых атом водорода бензольного ядра замещен на гидроксильные группы. Фенолокислоты одновременно обладают свойствами карбоновых кислот и фенолов. Кроме того для них характерны свойства, обусловленные наличием в молекуле обоих видов функциональных групп и бензольного ядра.
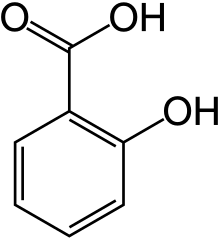
Фенолокислоты представляют собой твердые кристаллические вещества. Фенолокислоты, которые имеют в своем составе один фенольный гидроксил, сравнительно малорастворимые в холодной воде, но хорошо растворяются в горячей воде и многих органических растворителях. С увеличением числа фенольных гидроксилов растворимость фенолокислот увеличивается.
Распространение в природе
Фенолокислоты очень распространены в природе, поэтому их можно извлечь из природного сырья (такого, например, как боярышник кроваво-красный, рябина черноплодная, прополис). Фенолокислоты является основным компонентом (55—85 %) остатка от перегонки древесной смолы пек древесный.
Синтез
Нередко для получения фенолокислот применяют синтетические способы. В частности, 2-оксибензойную (салициловую) кислоту добывают из фенолята натрия и углекислого газа в автоклавах при 180 °C с последующей обработкой продукта реакции соляной кислотой синтез Кольбе:
C6H5ONa + С02 180 С → С6Н4 ( ONa ) COOH ;
С6Н4 ( ONa ) COOH + НС1 → С6Н4 ( ОН ) СООН + NaCl
Химические свойства
Фенолокислоты одновременно обладают свойствами карбоновых кислот и фенолов. Кроме того, для них характерны свойства, обусловленные наличием в молекуле обоих видов функциональных групп и бензольного ядра.
Разложение при нагревании
Фенолокислоты при нагревании разлагаются с образованием фенольных соединений и углекислого газа. Например, при нагревании салициловая кислота разлагается на фенол и углекислый газ:
НОС6Н4СООН → С6Н5ОН + СО2 салициловая кислота фенол углекислый газ
Галловая кислота при нагревании теряет карбоксильную группу и превращается в трехатомный фенол — пирогаллол.
Реакция этерификации (по карбоксильной группе)
Фенолокислоты как и карбоновые кислоты, благодаря наличию карбоксильной и гидроксильной групп способны образовывать эфиры.
Например, образование эфира салициловой кислоты — ацетилсалициловой кислоты:
НОС6Н4СООН + Н3С-С(=О)-О-(О=)С-СН3 → С6Н4(СООН)-О-СО-СН3 + СН3СООН салициловая кислота уксусный эфир ацетилсалициловая кислота уксусная кислота
и образовании эфира галловой кислоты одна молекула галловой кислоты реагирует своим карбоксилом, другая — фенильным гидроксилом. Китайский танин является глюкозидом дигалловой кислоты и глюкозы.
Образование солей
Фенолокислоты, как и карбоновые кислоты, образуют соли. Например, образование салицилата натрия при взаимодействии салициловой кислоты и едкого натрия:
НОС6Н4СООН + NaOH → НОС6Н4СООNa + Н2О салициловая кислота салицилат натрия
Реакция с хлоридом железа(III)(по фенольной группе)
Нередко возникает необходимость в выявлении наличия салициловой кислоты и других фенолокислот в консервированных продуктах. Тогда в пробирку помещают 2—3 мл исследуемого раствора и добавляют несколько капель 1 % раствора хлорида железа(III). Возникает фиолетовая окраска. В отличие от фенола, она может появиться и в спиртовом растворе кислоты. Окраска возникает в результате образования комплексных солей при взаимодействии фенольных групп шести молекул фенолокислоты с молекулой FeCl3.
Галловая кислота легко взаимодействует с хлоридом железа(III) и образует продукт реакции сине-чёрного цвета (чернила).
Реакция нуклеофильного замещения с галогенами
Наличие в молекуле фенолокислот фенольных групп (-ОН) позволяет им вступать в реакции замещения атомов водорода бензольного ядра на галогены при обычных условиях. Бензойная кислота и обычные ароматические кислоты в такие реакции не вступают.
Например, бромирование салициловой кислоты:
НОС6Н4СООН + Br2 → НО(Br)С6Н3СООН + НОС6Н3(Br)СООН + 2НBr салициловая кислота п-бромсалицилова кислота о-бромсалицилова кислота
Фенольная группа в молекуле салициловой кислоты действует как заместитель первого рода — направляет атомные группы и отдельные атомы на замещение атомом водорода бензольного ядра в о- и п-положении относительно себя.
Типичные представители и их производные, использование фенолокислот в медицине и промышленности
2-оксибензойная или салициловая кислота — типичная фенолокислотa, её иногда называют оксибензойной кислотой НОС6Н4СООН. Соли и эфиры салициловой кислоты — салицилаты. Впервые была добыта с эфиров, содержащихся в тканях некоторых растений, — гаультеровои эфирного масла Gaultheria procumbers. Салициловая кислота — твердое кристаллическое вещество. Обладает бактерицидным действием . Её соли и эфиры широко используют в медицине и ветеринарии как лекарственные препараты. Салициловую кислоту широко используют для производства лекарственных средств (например, ацетилсалициловой кислоты, фенилсалицилата), протравных красителей, фунгицидов (например, салициланилида), пахучих веществ (метилсалицилат, бензилсалицилат), антисептиков в пищевой промышленности, при консервировании, как реагент для колориметрического определения в растворах железа и меди, как кислотно — основной индикатор при люминесцентном анализе (при рН = 2,5…4,6 и при наличии кислоты появляется синяя люминесценция) и т. д.
3,4,5-триоксибензойная, или галловая кислота — фенолокислота, содержащая в составе молекулы одну карбоксильную (-СООН) и три гидроксильные (-ОН) группы. Имеет вяжущий вкус и является составной частью молекул дубильных веществ, в частности главного из них — таннина, которого много в коре дуба и особенно в чернильных орешках. В состав молекулы таннина галловая кислота входит в виде дигалловои кислоты, которая является эфиром, образованным двумя молекулами галловой кислоты.
Таннин — аморфный порошок желтоватого цвета, хорошо растворяется в воде, сильно вяжущий на вкус. В медицине и ветеринарии его используют как вяжущий препарат. Он используется также в кожевенной промышленности для дубления кож и меховых изделий. В химическом анализе его применяют как алкалоидный реактив.
Салицилат натрия — кристаллическое вещество, соль салициловой кислоты, хорошо растворяется в воде и органических растворителях, используется в медицине и ветеринарии как противоревматическое и жаропонижающее средство, сырье для получения других лекарственных средств.
Ацетилсалициловая кислота — белое кристаллическое вещество, эфир салициловой кислоты. Применяется в медицине и ветеринарии как жаропонижающее, противовоспалительное, антиревматическое и антиневралгическое средство. В тканях организма происходит постепенный гидролиз ацетилсалициловой кислоты, с образованием салициловой и ацетатной кислот, что и лежит в основе механизма действия медикамента.
Фенилсалицилат или салол (мусолим) НОС6Н4(СО)ОС6Н5, — кристаллическое вещество, производное салициловой кислоты. Используется в медицине и ветеринарии как дезинфицирующее средство при лечении некоторых кишечных заболеваний, а также при суставном ревматизме.
См. также
Литература
Тюкавкин Н. А. Биоорганическая химия. — М., 2004
