Тетраиодомеркурат(II) калия
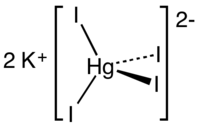
Тетраиодомеркура́т(II) ка́лия — неорганическое соединение, комплексная соль калия, ртути и иодистоводородной кислоты с формулой K2[HgI4], светло-жёлтые кристаллы, растворимые в воде, образует кристаллогидрат.
| Тетраиодомеркурат(II) калия | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Тетраиодомеркурат(II) калия |
| Традиционные названия | Тетраиодомеркуроат калия |
| Хим. формула | K2[HgI4] |
| Физические свойства | |
| Состояние | светло-жёлтые кристаллы |
| Молярная масса | 786,40 г/моль |
| Плотность | 4,29 г/см³ |
| Классификация | |
| Рег. номер CAS | 7783-33-7 |
| PubChem | 24542 |
| Рег. номер EINECS | 231-990-4 |
| SMILES | |
| InChI | |
| ChEBI | 51568 |
| Номер ООН | 3287 |
| ChemSpider | 22948 и 30780120 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Получение
- Реакция между концентрированными растворами хлорида ртути и иодида калия:
- Реакция между концентрированными растворами иодидов ртути и калия:
Физические свойства
Тетраиодомеркурат(II) калия образует светло-жёлтые кристаллы.
Образует кристаллогидрат состава K2[HgI4]•2H2O.
Хорошо растворяется в небольшом количестве воды, при разбавлении разлагается.
Химические свойства
- Безводную соль получают сушкой кристаллогидрата в вакууме:
- Разлагается при нагревании:
- В разбавленных водных растворах разлагается:
- Реагирует с концентрированными кислотами:
- и щелочами:
- Реагирует с раствором аммиака:
Применение
Приготовление реактива Несслера, щелочного водного раствора дигидрата тетраиодомеркурата(II) калия K2[HgI4]•2H2O.
При взаимодействии с аммиаком NH3 и гуанидинами реактив образует красно-коричневый осадок йодида оксодимеркураммония [OHg2NH2]I или йодида дийоддимеркураммония [I2Hg2NH2]I, с органическими восстановителями (например с первичными и вторичными спиртами, альдегидами) — чёрный осадок металлической ртути (ртуть получается в мелкодисперсном состоянии).
Применяется для качественного обнаружения вышеуказанных соединений, а также для колориметрического определения небольших количеств (около 0,001 % по объёму) аммиака. Предложен к применению немецким химиком Юлиусом Несслером в 1868 году.
Реактив Несслера хранят в тёмной склянке с притёртой пробкой в холодном месте. Реактив должен быть бесцветным. Реактив Несслера содержит ртуть и потому ядовит. Он не должен попадать на пищевые продукты и кожу.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4. — 639 с. — ISBN 5-82270-092-4.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.