Соль Шлиппе
Тиоантимона́т на́трия (Соль Шли́ппе, химическая формула — Na3SbS4 · 9H2O) — неорганическая соль, названная в честь своего изобретателя — Карла Шлиппе.
| Соль Шлиппе | |
|---|---|
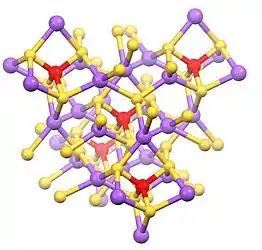 | |
| Общие | |
| Систематическое наименование |
Тетратиоантимонат натрия (нонагидрат) |
| Традиционные названия | Соль Шлиппе |
| Хим. формула | Na3SbS4·9H2O |
| Физические свойства | |
| Состояние | Твёрдое |
| Молярная масса | 481,13 г/моль |
| Плотность | 1,806 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 87 °C |
| • разложения | 234 °C |
| Классификация | |
| Рег. номер CAS | 10101-91-4 |
| PubChem | 71312650 |
| Рег. номер EINECS | 682-752-5 |
| SMILES | |
| InChI | |
| ChemSpider | 34995828 |
| Безопасность | |
| Краткие характер. опасности (H) |
H302, H332, H411 |
| Меры предостор. (P) |
P261, P264, P270, P271, P273, P301+P312, P304+P312, P304+P340, P312, P330, P391, P501 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
При стандартных условиях, тиоантимонат натрия — жёлтые кристаллы, хорошо растворимые в воде.
Название
Соль была названа в честь своего изобретателя — российского химика Карла Шлиппе
Физические свойства
Представляет собой жёлтые кристаллы кубической сингонии, пространственная группа P 213, параметры ячейки a = 1,1957 нм, Z = 4 [1].
- Жёлтые кристаллы
- плотность 1,806 г/см3;
- Тпл. = 87 °C;
- Ткип. = 234 °C (с разложением);
- хорошо растворим в воде;
На воздухе, соль разрушается, покрываясь красной плёнкой сульфида сурьмы.
Химические свойства
- При нагревании разлагается с потерей кристаллизационной воды:
- Разлагается в кислой среде с образованием осадка сульфида сурьмы(V)
Получение
- Сплавление сульфида натрия с серой и сульфидом сурьмы(III):
- Растворение сульфида сурьмы(V) в растворе сульфида натрия:
Ссылки
- K. Mereiter, A. Preisinger and H. Guth,. Hydrogen bonds in Schlippe's salt: refinement of the crystal structures of Na3SbS4.9H2O by X-ray diffraction and Na3SbS4.9D2O by neutron diffraction at room temperature // Acta Crystallographica Section B. — 1979. — Т. B35, № 1. — С. 19-25. — doi:10.1107/S0567740879002442.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.