Нанопоровое секвенирование
Нанопо́ровое секвени́рование — семейство высокоэффективных методов секвенирования ДНК или РНК третьего поколения[1]. Метод основан на использовании белковых, твердотельных или иных пор диаметром в несколько нанометров, чувствительных к нуклеиновым кислотам.
Нанопоровое секвенирование позволяет избежать стадий ПЦР-амплификации и химического мечения образца ДНК или РНК[2]. Это является существенным преимуществом по сравнению с другими методами секвенирования, которые используют хотя бы одну из этих стадий. Возможности метода включают относительно дешёвое генотипирование, высокую мобильность, быстрый анализ и отображение результатов в реальном времени. Было описано использование метода в быстром выявлении вирусных патогенов[3], отслеживании бактериальной резистентности[4], секвенировании генома человека[5][6] и растений[7], гаплотипировании[8], отслеживании вируса эболы[9] и других областях.
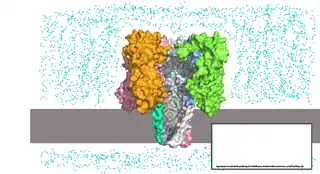 Нанопора альфа-гемолизина в мембране, напряжение отсутствует |
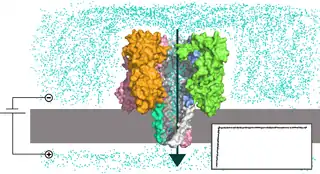 Под действием приложенного напряжения возникает ток ионов |
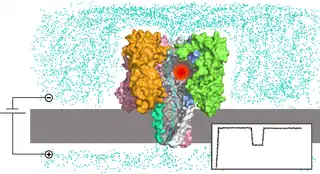 При прохождении большой молекулы через пору (показана красным) ток ионов уменьшается |
История
В 1989 году было продемонстрировано создание альфа-токсином, синтезируемым золотистым стафилококком, каналов (нанопор) в искусственной фосфолипидной мембране[10][11]. В 1995 году впервые была предложена идея нанопорового секвенирования — определение свойств линейного полимера при его протаскивании через пору в мембране. При прохождении через пору полимер определённым образом с ней взаимодействует, что позволяет определить его свойства[12]. Спустя год — в 1996 году — появилась первая работа, описывающая возможность применения нанопор (в качестве нанопоры был использован альфа-гемолизин) для определения характеристик нуклеиновых кислот[13].
В 1999—2000 годах была показано, что, используя в качестве нанопоры альфа-гемолизин стафилококка, можно отличить одноцепочечную РНК от одноцепочечной ДНК[14][15].
В 2001 году впервые была проведена работа, в которой с помощью нанопор определяли наличие коротких последовательностей ДНК[16]. Только к 2009 году удалось показать необходимую для создания методов секвенирования возможность различать нанопорами все основания в последовательности ДНК[17].
В 2012 году компанией Oxford Nanopore Technologies были продемонстрированы первые нанопоровые секвенаторы: GridION и MinION[18].
Тогда же была показана принципиальная возможность применения данного метода — был секвенирован геном бактериофага phiX длиной 5,4 тысячи пар оснований (п. о.)[19].
Принцип работы
Нанопоровая система представляет собой реакционную камеру, разделённую на две части мембраной, содержащей отверстие нанометрового размера — нанопору. К частям камеры прикладывают напряжение, вследствие чего исследуемые молекулы проходят через пору по направлению действия электрического поля. При прохождении молекулы нуклеиновой кислоты через пору отдельные нуклеотиды влияют на тот или иной измеряемый параметр системы, что позволяет определить последовательность нуклеотидов[2]. В практически используемом варианте нанопорового секвенирования камера заполнена электролитическим раствором, и измеряют силу тока ионов, протекающего через пору под действием поля; при прохождении нуклеотидов через пору они уменьшают сечение, доступное для ионов, и сила тока падает[20].
Варианты нанопорового секвенирования
В зависимости от того, сохраняют ли секвенируемые молекулы нуклеиновых кислот свою химическую целостность, выделяют два варианта — секвенирование целых цепочек и экзонуклеазное секвенирование[21].
Секвенирование целых цепочек
В данном методе цепи нуклеиновых кислот не расщепляются. Перенос целых молекул ДНК и РНК через пору может осуществляться следующими способами:
- Транспорт под действием напряжения. Так как ДНК и РНК несут на себе отрицательный заряд, то самым простым способом транспорта молекулы нуклеиновой кислоты через пору является их электрофоретический перенос вместе с ионами. Проблемой данного метода является то, что для измерения падения тока ионов через пору изначально требуется большой ток, чтобы получить хорошее соотношение сигнал/шум. Но при увеличении приложенного напряжения увеличивается и скорость, с которой молекула нуклеиновой кислоты преодолевает пору, а значит уменьшается время распознавания каждого отдельного основания, из-за чего качество распознавания падает[21].
- Транспорт под действием напряжения с расплетанием дуплексов. Уменьшить скорость прохождения одноцепочечной ДНК через пору можно, образуя с ней двухцепочечные участки с помощью комплементарных фрагментов ДНК. Тогда в ходе транспорта будет происходить расплетание данного участка, что и позволит дольше задерживать отдельные нуклеотиды в поре. Тем не менее, поскольку расплетание происходит не понуклеотидно, то время задержки нуклеотида в поре не является постоянным для всей последовательности[21].
- Транспорт с использованием ферментов. Для того, чтобы каждый нуклеотид задерживался в поре на фиксированное время, можно использовать различные ферменты, которые будут пропускать нуклеотиды через пору по одному. Примером такого фермента является ДНК-полимераза. За счёт приложенного напряжения комплекс ДНК-фермент изначально притянут к поре. Но теперь, прежде, чем очередной нуклеотид молекулы ДНК пройдёт через пору, должен произойти один шаг синтеза второй цепи ДНК. Возникающая задержка оснований внутри поры позволяет более точно различать их[21].
Экзонуклеазное секвенирование
В данном методе цепь нуклеиновой кислоты нарезается на единичные нуклеотиды экзонуклеазой, расположенной в непосредственной близости от поры. Под действием поля отрицательно заряженные нуклеотиды самостоятельно попадают в пору, где происходит определение оснований[21].
Типы нанопор
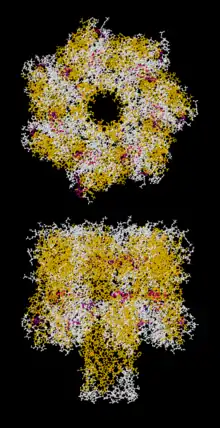
Для секвенирования используют белковые нанопоры и синтетические твердотельные нанопоры[21].
Альфа-гемолизин
Альфа-гемолизин Staphylococcus aureus — это водорастворимый мономер, который в мембране самопроизвольно образует гептамер. Трансмембранный домен состоит из ствола и головки поры. Головка поры содержит полость диаметром около 4,5 нм. В месте соединения ствола и головки находится сужение канала шириной 1,5 нм. Ствол поры состоит из 14 антипараллельных бета-тяжей, формирующих сквозной канал шириной около 2 нм. При нейтральном pH многие аминокислотные остатки в поре заряжены (например, положительно заряженный остаток лизина K147 и отрицательно заряженный остаток глутамата E111). В 1 М растворе KCl на поре держится потенциал в 120 мВ (от ствола к головке), что обуславливает ток 120 пА[22]. Внутри ствола находится три сайта распознавания нуклеотидов, что в теории делает возможным распознавание одного нуклеотида более чем одним сайтом (что увеличит точность прочтения)[23].
MspA
Порин A Mycobacterium smegmatis (англ. Mycobacterium smegmatis porin A, MspA) — нанопора диаметром 1,2 нм. Обладает структурными особенностями (формой и диаметром поры), которые улучшают соотношение сигнал/шум при секвенировании ДНК по сравнению с альфа-гемолизином[24]. Однако у MspA есть и существенный недостаток: отрицательно заряженное ядро мешает продвижению одноцепочечной ДНК внутри поры. Поэтому для секвенирования в изначальном белке три отрицательно заряженных остатка аспартата были заменены на нейтральные остатки аспарагина[25].
Моторный белок упаковки ДНК бактериофага phi29
Моторный белок упаковки ДНК бактериофага phi29 участвует в упаковке ДНК в капсид вирусов, а также в выходе ДНК из капсида при инфицировании. Ключевым отличием от вышеупомянутых белков является то, что имея больший диаметр канала (от 3,6 нм до 6 нм), он способен пропускать двухцепочечную ДНК. Из-за своей природы моторный белок phi29, в отличие от других пор, в своей исходной форме не встраивается в мембрану, однако эта проблема решается модификацией белка[26]. Другие модификации позволяют белку пропускать одноцепочечную ДНК или одноцепочечную РНК[27].
Твердотельные нанопоры
Помимо белковых нанопор также используются твердотельные нанопоры небиологической природы. Для анализа нуклеиновых кислот используют нанопоры в подложках из кремния, нитрида кремния и полиэтиленимина[27]. Обычно поры формируются пучками ионов или электронов, что позволяет легко варьировать их размер[28]. Отдельно стоит выделить материалы, формирующие очень тонкие — «2D»-поры: графен, дисульфид молибдена и другие[27]. Графен обладает и предельно маленькой толщиной, что способствует увеличению пространственного разрешения вдоль ДНК, и одновременно с этим прочностью, химической инертностью и электропроводимостью. Эти свойства способствуют применению данных материалом в нанопоровом секвенировании[28].
Графен
Являясь тонкой и ион-непроницаемая структурой, графен представляет собой хороший материал для секвенирования на основе нанопор. Так, было продемонстрировано, что нанопоры графена можно использовать в качестве электрода для измерения тока, протекающего через нанопоры между двумя камерами, содержащими ионные растворы[28].
Флуоресцентная детекция
В 2010 году был разработан метод твердотельного наносеквенирования, основанный на детекции флуоресцентного сигнала. Сначала нужная ДНК конвертируется в ДНК, в которой каждому изначальному основанию соответствует короткая последовательность. На эти короткие последовательности гибридизуются флуоресцентные зонды (молекулярные маяки), при этом конец одного зонда гасит флуоресценцию флуорофора на начале другого зонда. При этом для кодирования четырёх оснований нужно всего два типа зондов: каждому основанию (а точнее, соответствующей ему короткой последовательности) соответствует два флуоресцентных сигнала (00, 01, 10 или 11, где 0 соответствует одному цвету, а 1 — другому). При прохождении через пору получившаяся двухцепочечная ДНК расплетается, зонд отделяется, соответственно флуорофор на следующем зонде начинает светиться[29][30].
К преимуществам метода относится точность сигнала — камеры регистрирует сигнал гораздо точнее других имеющихся техник. Однако метод требует предварительной обработки образца: конвертации каждого нуклеотида в примерно 12 нуклеотидов (что также удлиняет саму ДНК)[29].
Сравнение твердотельных и биологических нанопор
Твердотельные нанопоры лишены некоторых недостатков биологических нанопор: чувствительности к pH, температуре, концентрациям электролита, механическим воздействиям и т. д. Помимо этого, они стабильнее, дольше служат, получить разнообразие форм и размеров таких пор значительно проще, а технология производства сходна с производством полупроводников, что сильно облегчает процесс получения таких пор и делает потенциально возможным совмещение с другими наноустройствами. К преимуществам биологических нанопор можно отнести возможность химической или генетической модификации, химическую специфичность к ДНК или РНК и относительно низкую скорость прохождения ДНК или РНК сквозь пору[28][31].
Прочие нанопоры
Для получения нанопор может быть использована технология ДНК-оригами. Впервые такая возможность была продемонстрирована в 2012 году, когда с помощью ДНК-оригами была получена структура, похожая на альфа-гемолизин. Полученная структура самопроизвольно встраивалась в мембраны[27].
В 2010 году было показано, что однослойные углеродные нанотрубки также могут встраиваться в мембраны и пропускать ДНК[27].
На 2020 год твердотельные нанопоры не обладают химической специфичностью белков, поэтому активно изучается возможность интеграции белковых нанопор в твердотельных подложках[28].
Другим перспективным направлением является использование твердотельных нанопор с сенсорами (ёмкостными датчиками, туннельными электронными и другими детекторами)[28].
Преимущества и недостатки
По сравнению с уже существовавшими методами секвенирования, применение такого метода секвенирования обладает преимуществами[2], такими как дешевизна и простота использования (за счёт отсутствия необходимости приготовления образца и использования реактивов), высокая чувствительность (вплоть до секвенирования без амплификации ДНК из крови и слюны), высокая длина прочтений (вплоть до десятков тысяч оснований), высокая мобильность, быстрый анализ и отображение результатов в реальном времени[2].
К недостаткам можно отнести такие свойства, как низкое качество прочтений по сравнению с технологиями секвенирования с короткими прочтениями (однако данная ситуация меняется в лучшую сторону при появлении новых алгоритмов), потеря функциональных свойств биологических пор с течением времени (поры надёжно работают лишь в течение определённого количества прогонов) и влияние факторов среды на скорость прочтения последовательности и, следовательно, на его качество (моторный белок может работать только с достаточной скоростью в определенном диапазоне pH, при этом недостаточно быстро работая за пределами диапазона)[32].
Коммерческое применение
Oxford Nanopore Technologies
В феврале 2012 года на конференции AGBT во Флориде компания Oxford Nanopore Technologies представила прототипы двух платформ для высокопроизводительного секвенирования длинных фрагментов, основанных на нанопоровом секвенировании целых цепочек: GridION и MinION. В качестве демонстрации был секвенирован геном бактериофага PhiX длиной 5386 п. о.[19] На 2020 год компания выпускает несколько устройств. Все они позволяют анализировать данные в реальном времени[33]
MinION
MinION — секвенатор небольшого размера с одноразовой ячейкой, спроектированный для использования в домашних условиях, с запланированной ценой около 900$. Секвенатор имеет разъём USB 3.0 для подключения к компьютеру. Содержит 512 нанопор со сходными характеристиками[2]. Ячейка позволяет отсеквенировать до 30 миллионов п. о. ДНК (примерно за двое суток можно оцифровать 10—20 миллионов п. о. ДНК)[34]. В 2019 году компания начала выпускать Flongle — адаптор к MinION или GridION, который позволяет работать с менее производительными (~1 Gb, 126 нанопор вместо 512), но существенно более дешёвыми ($90) ячейками[35] .
GridION
GridION — устройство, спроектированное для полногеномного секвенирования (по сути своей — MinION с увеличенной производительностью). Прототип имел 2000 отдельных нанопор, каждая из которых способна получать прочтения длиной до 5100 п. о. со скоростью 150 миллионов п. о./ч в течение 6 часов[2]. GridION Mk1 стоит $49,955 и содержит 5 независимых ячеек. С помощью него за один эксперимент можно отсеквенировать до 150 миллионов п. о. ДНК[36].
PromethION
Самый высокопроизводительный секвенатор этой компании, позволяет секвенировать за один эксперимент несколько триллионов п. о. ДНК. PromethION 24 содержит 24 ячейки и способен за трое суток оцифровать 3,8 триллионов п. о. ДНК, PromethION 48 содержит 48 ячеек и способен за трое суток оцифровать 7,6 триллионов п. о. ДНК. Ячейки секвенатора содержат 3000 нанопор[37]. Поток данных с такого количества нанопор не может анализироваться обычным компьютером, поэтому для использования этого секвенатора необходим суперкомпьютер (впрочем, если запускать только одну ячейку, то справится и обычный компьютер)[37][38].
Другие разработки
Компания планирует выпустить ещё два устройства: SmidgION — секвенатор, который подключается к смартфону, и Plongle — секвенатор, который содержит 96 независимых, но малопроизводительных ячеек, и, соответственно, рассчитан на частые секвенирования большого объёма коротких ДНК[39].
Пост-обработка данных, полученных с помощью Oxford Nanopore
После использования продукции Oxford Nanopore на выходе имеются сырые данные формата FAST5. Формат FAST5, используемый Oxford Nanopore, — это вариант стандарта HDF5 с иерархической внутренней структурой, предназначенной для хранения метаданных, связанных с последовательностью ДНК и событий (агрегированные измерения общего тока), предварительно обработанных рабочим устройством. Результаты обработки отображаются в реальном времени в графическом интерфейсе MinKNOW, а данные записываются в формате файлов FASTQ или .fast5[40]. Далее нужно произвести распознавание нуклеотидов (англ. base calling). Этот процесс обработает сырые данные формата FAST5 в формат FASTQ (в программе MinKNOW этот процесс можно запустить во время прочтения ридов). Также можно использовать такие программы, как poreTools[41], Guppy[42][43].
Далее нужно очистить полученные последовательности, чтобы избавиться от данных со слишком большим шумом. Для этой задачи используется, например, программа NanoFilt[44][45]. Как только данные будут очищены, полученные данные дальше можно использовать для последующей сборки и анализа данных[43].
Примечания
- Niedringhaus Thomas P., Milanova Denitsa, Kerby Matthew B., Snyder Michael P., Barron Annelise E. Landscape of Next-Generation Sequencing Technologies (англ.) // Analytical Chemistry. — 2011. — 15 June (vol. 83, no. 12). — P. 4327—4341. — ISSN 0003-2700. — doi:10.1021/ac2010857.
- Maitra R. D., Kim J., Dunbar W. B. Recent advances in nanopore sequencing. (англ.) // Electrophoresis. — 2012. — December (vol. 33, no. 23). — P. 3418—3428. — doi:10.1002/elps.201200272. — PMID 23138639.
- Greninger Alexander L., Naccache Samia N., Federman Scot, Yu Guixia, Mbala Placide, Bres Vanessa, Stryke Doug, Bouquet Jerome, Somasekar Sneha, Linnen Jeffrey M., Dodd Roger, Mulembakani Prime, Schneider Bradley S., Muyembe-Tamfum Jean-Jacques, Stramer Susan L., Chiu Charles Y. Rapid metagenomic identification of viral pathogens in clinical samples by real-time nanopore sequencing analysis (англ.) // Genome Medicine. — 2015. — 29 September (vol. 7, no. 1). — ISSN 1756-994X. — doi:10.1186/s13073-015-0220-9.
- Cao Minh Duc, Ganesamoorthy Devika, Elliott Alysha G., Zhang Huihui, Cooper Matthew A., Coin Lachlan J.M. Streaming algorithms for identification of pathogens and antibiotic resistance potential from real-time MinIONTM sequencing (англ.) // GigaScience. — 2016. — 26 July (vol. 5, no. 1). — ISSN 2047-217X. — doi:10.1186/s13742-016-0137-2.
- nanopore-wgs-consortium/NA12878. — 2020-03-01.
- Human Genome on a MinION (англ.). Oxford Nanopore Technologies (20 октября 2016). Дата обращения: 12 марта 2020.
- Solanum pennellii (acc. LA5240) - PlabiPD. www.plabipd.de. Дата обращения: 12 марта 2020.
- Ammar Ron, Paton Tara A., Torti Dax, Shlien Adam, Bader Gary D. Long read nanopore sequencing for detection of HLA and CYP2D6 variants and haplotypes (англ.) // F1000Research. — 2015. — 20 May (vol. 4). — P. 17. — ISSN 2046-1402. — doi:10.12688/f1000research.6037.2.
- Nick Loman. How a small backpack for fast genomic sequencing is helping combat Ebola (англ.). The Conversation. Дата обращения: 12 марта 2020.
- О. В. Красильников. Белковые каналы в липидном бислое. Автореферат диссертации на соискание учёной степени доктора биологических наук: 03.00.02. МГУ. М.: 1989, 30 с.
- К. Г. Родригес, Л. Юлдашева. Наносчётчик для «наноовец» // Наука и жизнь. — 2021. — № 3. — С. 68.
- Characterization of individual polymer molecules based on monomer-interface interactions (англ.). Дата обращения: 12 марта 2020.
- Kasianowicz J. J., Brandin E., Branton D., Deamer D. W. Characterization of individual polynucleotide molecules using a membrane channel (англ.) // Proceedings of the National Academy of Sciences. — 1996. — 26 November (vol. 93, no. 24). — P. 13770—13773. — ISSN 0027-8424. — doi:10.1073/pnas.93.24.13770.
- Akeson M., Branton D., Kasianowicz J. J., Brandin E., Deamer D. W. Microsecond time-scale discrimination among polycytidylic acid, polyadenylic acid, and polyuridylic acid as homopolymers or as segments within single RNA molecules. (англ.) // Biophysical Journal. — 1999. — December (vol. 77, no. 6). — P. 3227—3233. — doi:10.1016/S0006-3495(99)77153-5. — PMID 10585944.
- Meller A., Nivon L., Brandin E., Golovchenko J., Branton D. Rapid nanopore discrimination between single polynucleotide molecules. (англ.) // Proceedings Of The National Academy Of Sciences Of The United States Of America. — 2000. — 1 February (vol. 97, no. 3). — P. 1079—1084. — doi:10.1073/pnas.97.3.1079. — PMID 10655487.
- Howorka Stefan, Cheley Stephen, Bayley Hagan. Sequence-specific detection of individual DNA strands using engineered nanopores (англ.) // Nature Biotechnology. — 2001. — July (vol. 19, no. 7). — P. 636—639. — ISSN 1087-0156. — doi:10.1038/90236.
- Stoddart D., Heron A. J., Mikhailova E., Maglia G., Bayley H. Single-nucleotide discrimination in immobilized DNA oligonucleotides with a biological nanopore (англ.) // Proceedings of the National Academy of Sciences. — 2009. — 20 April (vol. 106, no. 19). — P. 7702—7707. — ISSN 0027-8424. — doi:10.1073/pnas.0901054106.
- Oxford Nanopore introduces DNA 'strand sequencing' on the high-throughput GridION platform and presents MinION, a sequencer the size of a USB memory stick (англ.). Oxford Nanopore Technologies (17 февраля 2012). Дата обращения: 12 марта 2020.
- Eisenstein Michael. Oxford Nanopore announcement sets sequencing sector abuzz (англ.) // Nature Biotechnology. — 2012. — April (vol. 30, no. 4). — P. 295—296. — ISSN 1087-0156. — doi:10.1038/nbt0412-295.
- Stephanie J. Heerema, Cees Dekker. Graphene nanodevices for DNA sequencing (англ.) // Nature Nanotechnology. — 2016-02. — Vol. 11, iss. 2. — P. 127–136. — ISSN 1748-3395 1748-3387, 1748-3395. — doi:10.1038/nnano.2015.307.
- Wanunu Meni. Nanopores: A journey towards DNA sequencing (англ.) // Physics of Life Reviews. — 2012. — June (vol. 9, no. 2). — P. 125—158. — ISSN 1571-0645. — doi:10.1016/j.plrev.2012.05.010.
- Nakane Jonathan J, Akeson Mark, Marziali Andre. Nanopore sensors for nucleic acid analysis (англ.) // Journal of Physics: Condensed Matter. — 2003. — 1 August (vol. 15, no. 32). — P. R1365—R1393. — ISSN 0953-8984. — doi:10.1088/0953-8984/15/32/203.
- Stoddart David, Maglia Giovanni, Mikhailova Ellina, Heron Andrew J., Bayley Hagan. Multiple Base-Recognition Sites in a Biological Nanopore: Two Heads are Better than One (англ.) // Angewandte Chemie International Edition. — 2009. — 11 December (vol. 49, no. 3). — P. 556—559. — ISSN 1433-7851. — doi:10.1002/anie.200905483.
- Manrao Elizabeth A., Derrington Ian M., Pavlenok Mikhail, Niederweis Michael, Gundlach Jens H. Nucleotide Discrimination with DNA Immobilized in the MspA Nanopore (англ.) // PLoS ONE. — 2011. — 4 October (vol. 6, no. 10). — P. e25723. — ISSN 1932-6203. — doi:10.1371/journal.pone.0025723.
- Butler T. Z., Pavlenok M., Derrington I. M., Niederweis M., Gundlach J. H. Single-molecule DNA detection with an engineered MspA protein nanopore (англ.) // Proceedings of the National Academy of Sciences. — 2008. — 19 December (vol. 105, no. 52). — P. 20647—20652. — ISSN 0027-8424. — doi:10.1073/pnas.0807514106.
- Wendell David, Jing Peng, Geng Jia, Subramaniam Varuni, Lee Tae Jin, Montemagno Carlo, Guo Peixuan. Translocation of double-stranded DNA through membrane-adapted phi29 motor protein nanopores (англ.) // Nature Nanotechnology. — 2009. — 27 September (vol. 4, no. 11). — P. 765—772. — ISSN 1748-3387. — doi:10.1038/nnano.2009.259.
- Guo Bing-Yuan, Zeng Tao, Wu Hai-Chen. Recent advances of DNA sequencing via nanopore-based technologies (англ.) // Science Bulletin. — 2015. — February (vol. 60, no. 3). — P. 287—295. — ISSN 2095-9273. — doi:10.1007/s11434-014-0707-6.
- Types of nanopores (англ.). Oxford Nanopore Technologies. Дата обращения: 12 марта 2020.
- McNally Ben, Singer Alon, Yu Zhiliang, Sun Yingjie, Weng Zhiping, Meller Amit. Optical Recognition of Converted DNA Nucleotides for Single-Molecule DNA Sequencing Using Nanopore Arrays (англ.) // Nano Letters. — 2010. — 9 June (vol. 10, no. 6). — P. 2237—2244. — ISSN 1530-6984. — doi:10.1021/nl1012147.
- Soni Gautam V., Singer Alon, Yu Zhiliang, Sun Yingjie, McNally Ben, Meller Amit. Synchronous optical and electrical detection of biomolecules traversing through solid-state nanopores (англ.) // Review of Scientific Instruments. — 2010. — January (vol. 81, no. 1). — P. 014301. — ISSN 0034-6748. — doi:10.1063/1.3277116.
- Liu Zewen, Wang Yifan, Deng Tao, Chen Qi. Solid-State Nanopore-Based DNA Sequencing Technology (англ.) // Journal of Nanomaterials. — 2016. — Vol. 2016. — P. 1—13. — ISSN 1687-4110. — doi:10.1155/2016/5284786.
- Zewen Liu, Yifan Wang, Tao Deng, Qi Chen. Solid-State Nanopore-Based DNA Sequencing Technology (англ.) // Journal of Nanomaterials. — 2016. — Vol. 2016. — P. 1–13. — ISSN 1687-4129 1687-4110, 1687-4129. — doi:10.1155/2016/5284786.
- Products (англ.). Oxford Nanopore Technologies. Дата обращения: 14 мая 2020.
- MinION (англ.). Oxford Nanopore Technologies. Дата обращения: 13 апреля 2020.
- Flongle adapter (англ.). Oxford Nanopore Technologies. Дата обращения: 13 апреля 2020.
- GridION Mk1 (англ.). Oxford Nanopore Technologies. Дата обращения: 13 апреля 2020.
- PromethION (англ.). Oxford Nanopore Technologies. Дата обращения: 13 апреля 2020.
- Arne De Roeck, Wouter De Coster, Liene Bossaerts, Rita Cacace, Tim De Pooter. NanoSatellite: accurate characterization of expanded tandem repeat length and sequence through whole genome long-read sequencing on PromethION (англ.) // Genome Biology. — 2019-12. — Vol. 20, iss. 1. — P. 239. — ISSN 1474-760X. — doi:10.1186/s13059-019-1856-3.
- Products (англ.). Oxford Nanopore Technologies. Дата обращения: 13 апреля 2020.
- Camilla L.C. Ip, Matthew Loose, John R. Tyson, Mariateresa de Cesare, Bonnie L. Brown. MinION Analysis and Reference Consortium: Phase 1 data release and analysis (англ.) // F1000Research. — 2015-10-15. — Vol. 4. — P. 1075. — ISSN 2046-1402. — doi:10.12688/f1000research.7201.1.
- arq5x/poretools (англ.). GitHub. Дата обращения: 14 мая 2020.
- nanoporetech/pyguppyclient. — 2020-05-07.
- Goldstein Sarah, Beka Lidia, Graf Joerg, Klassen Jonathan L. Evaluation of strategies for the assembly of diverse bacterial genomes using MinION long-read sequencing (англ.) // BMC Genomics. — 2019. — 9 January (vol. 20, no. 1). — ISSN 1471-2164. — doi:10.1186/s12864-018-5381-7.
- Wouter De Coster. NanoFilt: Filtering and trimming of Oxford Nanopore Sequencing data.
- Stein Maria, Brinks Erik, Rathje Jana, Cho Gyu-Sung, Franz Charles M. A. P. Complete Genome Sequence of Tetracycline-Resistant Serratia liquefaciens S1, Isolated from Mixed Greens, Obtained Using Illumina MiSeq and Oxford Nanopore MinION Sequencing (англ.) // Microbiology Resource Announcements. — 2020. — 7 May (vol. 9, no. 19). — ISSN 2576-098X. — doi:10.1128/MRA.00156-20.
Литература
- Kovaka, S., Fan, Y., Ni, B. et al. Targeted nanopore sequencing by real-time mapping of raw electrical signal with UNCALLED. Nat Biotechnol (2020). https://doi.org/10.1038/s41587-020-0731-9
Программа (https://github.com/skovaka/UNCALLED)