Диэтилфталат
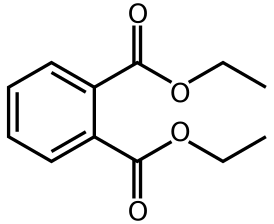
Диэтилфталат — сложный эфир фталевой кислоты.
| Диэтилфталат | |
|---|---|
  | |
| Общие | |
| Систематическое наименование |
Диэтиловый эфир о-фталевой кислоты |
| Традиционные названия | Диэтилфталат |
| Хим. формула | C12H14O4 |
| Рац. формула | о-С6Н4(СООС2Н5)2 |
| Физические свойства | |
| Состояние | жидкое |
| Молярная масса | 222,24 г/моль |
| Плотность | 1,117 (20 °C) |
| Динамическая вязкость | 1010 Па·с |
| Термические свойства | |
| Температура | |
| • плавления | -3 °C |
| • кипения |
298 — 299 (1013 гПа) °С 156 (14 гПа) °C |
| • вспышки | 125 °C |
| Пределы взрываемости | 0,7 ± 0,1 об.%[1] |
| Давление пара | 0,002 ± 0,001 мм рт.ст.[1] |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,1 (20 °C) |
| • в | Эфир, Этанол Растворимо |
| Оптические свойства | |
| Показатель преломления | 1,500 |
| Классификация | |
| Рег. номер CAS | 84-66-2 |
| PubChem | 6781 |
| Рег. номер EINECS | 201-550-6 |
| SMILES | |
| InChI | |
| RTECS | TI1050000 |
| ChEBI | 34698 |
| ChemSpider | 13837303 |
| Безопасность | |
| ЛД50 |
крысы (перорально) 8600 мг/кг |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Получение
Диэтилфталат в химической промышленности получают нагреванием этилового спирта с фталевым ангидридом в присутствии небольших количеств серной кислоты в качестве катализатора. После нейтрализации кислоты водным раствором гидроксидов или карбонатов металлов, смесь разделяют вакуумной перегонкой на этанол и диэтилфталат.
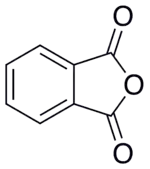 |
H2SO4 |  | ||
Применение
Диэтилфталат применяют как пластификатор полимеров и фиксатор запаха в парфюмерии. Применяется в качестве денатурирующей добавки для этилового спирта и спиртосодержащей продукции.
Токсичность
Диэтилфталат относится к категории среднетоксичных соединений со слабо выраженным кумулятивным действием. Обладает раздражающим, кожно-резорбтивным, сенсибилизирующим, гонадотропным, тератогенным и мутагенным действием.
В образцах нелегальной водки диэтилфталат обнаруживался в концентрациях 850—1284 мг/л.
