BUB3
Белок митотической контрольной точки BUB3 — белок, кодируемый у человека геном BUB3[2][3].
Bub3 участвует в регуляции контрольной точки сборки веретена деления (SAC) (англ. spindle assembly checkpoint, SAC). Он не является необходимым для дрожжей, но необходим для высших эукариот. В качестве одного из белков контрольных точек Bub3 задерживает наступление необратимой анафазы путём направления локализации кинетохор в прометафазу[2], чтобы достичь двойной ориентации. Направление взаимодействия кинетохор и микротрубочек обеспечивает надлежащее (и разумеется, с двойной ориентацией) прикрепление хромосом к анафазе. Bub3 и связанные белки, которые формируют контрольные точки сборки веретена деления (SAC) ингибируют действие комплекса стимуляции анафазы (APC), предотвращая раннее вступление митоза в анафазу и выход; это служит в качестве механизма для правильности хромосомной сегрегации[4].
Функция
Bub3 является важным компонентом в формировании митотического комплекса сборки веретена, который образует комплекс с другими важными белками[5]. Для правильной сегрегации клеток необходимо для всех митотических веретен правильно приложить к кинетохорам каждую хромосому. Это контролируется комплексом митотической контрольной точки веретена, который действует в качестве ответной обратной связи[5]. Если приходит сигнал о дефекте приложения, митоз будет остановлен для того, чтобы все хромосомы получили амфителическую привязку к веретену. После исправления ошибки ячейка может приступить к анафазе. Комплекс белков, которые регулируют остановку клеточного цикла — BUB1, BUB2, BUB3 (этот белок), MAD1, MAD2, MAD3 и MPS1[5].
Роль в контрольной точке сборки веретена деления
В одиноких кинетохорах комплекс, состоящий из BubR1, Bub3 и Cdc20 взаимодействует с комплексом Mad2-CDC20 ингибируя APC, таким образом, препятствуя образованию активного APCCdc20[6][7]. Bub3 связывается конститутивно с BubR1; в этом положении Bub3 действует в качестве ключевого компонента SAC в формировании ингибиторного комплекса[8]. Секурин и циклин B также стабилизируют до наступления анафазы переходы одиноких кинетохор[9]. Стабилизация циклина и секурина предотвращает деградацию, приводящую к необратимому и быстрому разделению сестринских хроматид .
Формирование этих «ингибиторных комплексов» и сигнала «ждать» — ступени перед активацией сепаразы; на этапе до наступления анафазы, секурин ингибирует активность сепаразы и поддерживает скреплённость комплекса[4].
Структура
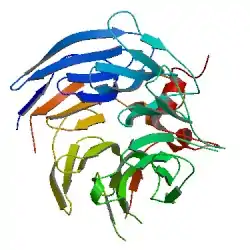
Кристаллическая структура представляет белок Bub3 в виде структуры из семи-лопастного бета-пропеллера с наличием повторов Wd40 в каждом лезвии, образованных с помощью четырёх антипараллельных бета-листовых нитей, которые расположены вокруг конического канала. Данные мутаций представляют несколько важных поверхностей взаимодействия для формирования SAC, особо консервативных триптофанов (в лезвиях 1 и 3) и консервативных последовательностей VAVE в лезвии 5.
Rae1 (экспортный фактор мРНК), ещё один член семейства белков WD40, представляет высококонсервативную последовательность подобно Bub3. Оба связываются с Gle2p-связывающей последовательностью (GLEBS) мотивов; в то время как Bub3 специфически связывается Mad3 и Bub1, Rae1 имеет более беспорядочные связывания, связываясь как с комплексом ядерных пор, так и Bub1. Это указывает на сходство взаимодействия Bub3 и Rae1 с Bub1[10].
Взаимодействия
BUB3, как было выявлено, взаимодействует с BUB1B[2][11][12], HDAC1[13] и гистондеацетилазой 2[13].
Bub3, как было выявлено, образуют комплексы с MAD1-Bub1 и с Cdc20 (взаимодействие которых не требует свободных кинетохор). Кроме того, было выявлено связывание с MAD2 и Mad3[14][8].
Bub3 управляет локализацией Bub1 в кинетохорах для активации SAC[2]. Как в Saccharomyces cerevisiae, так и имногоклеточных, Bub3 была предназначена для связывания BubR1 и Bub1[4].
Компоненты, которые необходимы для контрольной точки сборки веретена деления в дрожжах были определены как Bub1, Bub3, MAD1, Mad2, Mad3 и более важный Mps1 (протеинкиназа).
Регуляция
Когда SAC активирована, производство комплекса Bub3-CDC20 также активируется. Когда прикрепление кинетохор завершено, в комплексах контрольных точек веретена (в том числе BubR1-Bub3) наблюдается снижение концентрации[15][16]. Bub3 также действует в качестве регулятора, влияя на связывание Mad3 с Mad2[8].
Структурный и последовательный анализ показал существование трех консервативных областей, которые называют повторами WD40. Мутация одного из этих мотивов указывает на нарушение способности Bub3 взаимодействовать с MAD2, Mad3 и Cdc20. Структурные данные предполагают, что Bub3 действует в качестве платформы, опосредующей взаимодействие комплексов белковых SAC[10][8].
Клиническое значение
BUB3 образует комплекс с BUB1 (BUB1/BUB3-комплекс) ингибирующий комплекс стимуляции анафазы или циклосомы (APC / C), как только активируется контрольная точка сборки веретена деления. BUB3 также фосфорилирует:
- Cdc20 (активатор) и, таким образом, ингибирует деятельность убиквитинлигазы APC/C.
- MAD1L1, который обычно взаимодействует с BUB1 и BUBR1 и в свою очередь комплекс BUB1/BUB3 взаимодействует с MAD1L1.
Ещё одной функцией BUB3 является содействие правильному вложению микротрубочек в кинетохоры (К-МТ), когда контрольная точка сборки веретена активна. Он играет важную роль в локализации кинетохор BUB1.
BUB3 служит в мейозных ооцитах как регулятор хромосом.
Дефекты клеточного цикла в BUB3 может способствовать следующих заболеваниям[5]:
- гепатоцеллюлярной карциномы
- раку желудка
- раку молочной железы
- раку шейки матки
- аденоматозному полипозу
- наследственной остеосаркоме рака груди
- глиобластомы цервицита
- карциномы рака легких
- Коли-полипоза
Примечания
- PDB 2I3S: Larsen N.A., Al-Bassam J., Wei R.R., Harrison S.C. Structural analysis of Bub3 interactions in the mitotic spindle checkpoint (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2007. — January (vol. 104, no. 4). — P. 1201—1206. — doi:10.1073/pnas.0610358104. — PMID 17227844.
- Taylor S.S., Ha E., McKeon F. The human homologue of Bub3 is required for kinetochore localization of Bub1 and a Mad3/Bub1-related protein kinase (англ.) // J Cell Biol : journal. — 1998. — August (vol. 142, no. 1). — P. 1—11. — doi:10.1083/jcb.142.1.1. — PMID 9660858.
- Entrez Gene: BUB3 BUB3 budding uninhibited by benzimidazoles 3 homolog (yeast).
- Morgan, David O. The cell cycle: principles of control (англ.). — London: Published by New Science Press in association with Oxford University Press, 2007. — ISBN 0-87893-508-8.
- Kalitsis P., Earle E., Fowler K.J., Choo K.H. Bub3 gene disruption in mice reveals essential mitotic spindle checkpoint function during early embryogenesis (англ.) // Genes Dev. : journal. — 2000. — September (vol. 14, no. 18). — P. 2277—2282. — doi:10.1101/gad.827500. — PMID 10995385.
- Eytan, E., Braunstein, I., Ganoth, D. et al. Two different mitotic checkpoint inhibitors of the anaphase-promoting complex/cyclosome antagonize the action of the activator Cdc20 (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2008. — Vol. 105, no. 7. — P. 9181—9185. — doi:10.1073/pnas.0804069105. — PMID 18591651.
- Fang G., Yu H and Kirschner M.W. Direct binding of CDC20 protein family members activates the anaphase-promoting complex in mitosis and G1 (англ.) // Mol Cell : journal. — 1998. — Vol. 2, no. 2. — P. 163—171. — doi:10.1016/S1097-2765(00)80126-4. — PMID 9734353.
- Fraschini, R., Beretta, A., Sironi, L., Musacchio, A. et al. Bub3 interaction with Mad2, Mad3 and Cdc20 is mediated by WD40 repeats and does not require intact kinetochores (англ.) // The EMBO Journal : journal. — 2001. — Vol. 20, no. 23. — P. 6648—6659. — doi:10.1093/emboj/20.23.6648. — PMID 11726501.
- Li, M., Li, S., Yuan, J., Wang, Z-B, Sun, S-C et al. Bub3 Is a Spindle Assembly Checkpoint Protein Regulating Chromosome Segregation during Mouse Oocyte Meiosis (англ.) // PLoS ONE : journal / Jin, Dong-Yan. — 2009. — Vol. 4, no. 11. — P. e7701. — doi:10.1371/journal.pone.0007701. — PMID 19888327.
- Larsen, N.A., Harrison, S.C. Crystal structure of the spindle assembly checkpoint protein Bub3 (англ.) // J Mol Biol : journal. — 2004. — Vol. 344, no. 4. — P. 885—892. — doi:10.1016/j.jmb.2004.09.094. — PMID 15544799.
- Sudakin, V; Chan G K., Yen T J. Checkpoint inhibition of the APC/C in HeLa cells is mediated by a complex of BUBR1, BUB3, CDC20, and MAD2 (англ.) // J. Cell Biol. : journal. — 2001. — Vol. 154, no. 5. — P. 925—936. — doi:10.1083/jcb.200102093. — PMID 11535616.
- Cayrol, C., Cougoule, C., Wright, M. The beta2-adaptin clathrin adaptor interacts with the mitotic checkpoint kinase BubR1 (англ.) // Biochem. Biophys. Res. Commun. : journal. — 2002. — Vol. 298, no. 5. — P. 720—730. — doi:10.1016/S0006-291X(02)02522-6. — PMID 12419313.
- Yoon, Y-M, Baek, K-H, Jeong, S-J et al. WD repeat-containing mitotic checkpoint proteins act as transcriptional repressors during interphase (англ.) // FEBS Lett. : journal. — 2004. — Vol. 575, no. 1—3. — P. 23—9. — doi:10.1016/j.febslet.2004.07.089. — PMID 15388328.
- Logarinho, E., Bousbaa, H. Kinetochore-microtubule interactions "in check" by Bub1, Bub3 and BubR1: The dual task of attaching and signalling (англ.) // Cell Cycle : journal. — 2008. — Vol. 7, no. 12. — P. 1763—1768. — doi:10.4161/cc.7.12.6180. — PMID 18594200.
- Yu, H. Regulation of APC–Cdc20 by the spindle checkpoint (англ.) // Current Opinion in Cell Biology. — Elsevier, 2002. — Vol. 14, no. 6. — P. 706—714. — doi:10.1016/S0955-0674(02)00382-4. — PMID 12473343.
- Doncic, A., Ben-Jacob, E., Einav, S., Barkai, N. Reverse Engineering of the Spindle Assembly Checkpoint (англ.) // PLoS ONE : journal / Khanin, Raya. — 2009. — Vol. 4, no. 8. — P. e6495. — doi:10.1371/journal.pone.0006495. — PMID 19652707.
Литература
- Cahill D.P., da Costa L.T., Carson-Walter E.B. et al. Characterization of MAD2B and other mitotic spindle checkpoint genes (англ.) // Genomics : journal. — Academic Press, 1999. — Vol. 58, no. 2. — P. 181—187. — doi:10.1006/geno.1999.5831. — PMID 10366450.
- Kwon T.K., Hawkins A.L., Griffin C.A., Gabrielson E. Assignment of BUB3 to human chromosome band 10q26 by in situ hybridization (англ.) // Cytogenetic and Genome Research : journal. — Karger Publishers, 2000. — Vol. 88, no. 3—4. — P. 202—203. — doi:10.1159/000015547. — PMID 10828586.
- Saffery R., Irvine D.V., Griffiths B. et al. Components of the human spindle checkpoint control mechanism localize specifically to the active centromere on dicentric chromosomes (англ.) // Hum. Genet. : journal. — 2001. — Vol. 107, no. 4. — P. 376—384. — doi:10.1007/s004390000386. — PMID 11129339.
- Kaplan K.B., Burds A.A., Swedlow J.R. et al. A role for the Adenomatous Polyposis Coli protein in chromosome segregation (англ.) // Nat. Cell Biol. : journal. — 2001. — Vol. 3, no. 4. — P. 429—432. — doi:10.1038/35070123. — PMID 11283619.
- Sudakin V., Chan G.K., Yen T.J. Checkpoint inhibition of the APC/C in HeLa cells is mediated by a complex of BUBR1, BUB3, CDC20, and MAD2 (англ.) // J. Cell Biol. : journal. — 2001. — Vol. 154, no. 5. — P. 925—936. — doi:10.1083/jcb.200102093. — PMID 11535616.
- Saxena A., Saffery R., Wong L.H. et al. Centromere proteins Cenpa, Cenpb, and Bub3 interact with poly(ADP-ribose) polymerase-1 protein and are poly(ADP-ribosyl)ated (англ.) // J. Biol. Chem. : journal. — 2002. — Vol. 277, no. 30. — P. 26921—26926. — doi:10.1074/jbc.M200620200. — PMID 12011073.
- Saxena A., Wong L.H., Kalitsis P. et al. Poly(ADP-ribose) polymerase 2 localizes to mammalian active centromeres and interacts with PARP-1, Cenpa, Cenpb and Bub3, but not Cenpc (англ.) // Human Molecular Genetics : journal. — Oxford University Press, 2003. — Vol. 11, no. 19. — P. 2319—2329. — doi:10.1093/hmg/11.19.2319. — PMID 12217960.
- Baek W.K., Park J.W., Lim J.H. et al. Molecular cloning and characterization of the human budding uninhibited by benomyl (BUB3) promoter (англ.) // Gene : journal. — Elsevier, 2003. — Vol. 295, no. 1. — P. 117—123. — doi:10.1016/S0378-1119(02)00827-2. — PMID 12242018.
- Strausberg R.L., Feingold E.A., Grouse L.H. et al. Generation and initial analysis of more than 15,000 full-length human and mouse cDNA sequences (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2003. — Vol. 99, no. 26. — P. 16899—16903. — doi:10.1073/pnas.242603899. — PMID 12477932.
- Liu L., Amy V., Liu G., McKeehan W.L. Novel complex integrating mitochondria and the microtubular cytoskeleton with chromosome remodeling and tumor suppressor RASSF1 deduced by in silico homology analysis, interaction cloning in yeast, and colocalization in cultured cells (англ.) // In Vitro Cell. Dev. Biol. Anim. : journal. — 2003. — Vol. 38, no. 10. — P. 582—594. — doi:10.1290/1543-706X(2002)38<582:NCIMAT>2.0.CO;2. — PMID 12762840.
- Beausoleil S.A., Jedrychowski M., Schwartz D. et al. Large-scale characterization of HeLa cell nuclear phosphoproteins (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2004. — Vol. 101, no. 33. — P. 12130—12135. — doi:10.1073/pnas.0404720101. — PMID 15302935.
- Yoon Y.M., Baek K.H., Jeong S.J. et al. WD repeat-containing mitotic checkpoint proteins act as transcriptional repressors during interphase (англ.) // FEBS Lett. : journal. — 2004. — Vol. 575, no. 1—3. — P. 23—9. — doi:10.1016/j.febslet.2004.07.089. — PMID 15388328.
- Gerhard D.S., Wagner L., Feingold E.A. et al. The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC) (англ.) // Genome Res. : journal. — 2004. — Vol. 14, no. 10B. — P. 2121—2127. — doi:10.1101/gr.2596504. — PMID 15489334.
- Tang Z., Shu H., Oncel D. et al. Phosphorylation of Cdc20 by Bub1 provides a catalytic mechanism for APC/C inhibition by the spindle checkpoint (англ.) // Mol. Cell : journal. — 2004. — Vol. 16, no. 3. — P. 387—397. — doi:10.1016/j.molcel.2004.09.031. — PMID 15525512.
- Andersen J.S., Lam Y.W., Leung A.K. et al. Nucleolar proteome dynamics (англ.) // Nature. — 2005. — Vol. 433, no. 7021. — P. 77—83. — doi:10.1038/nature03207. — PMID 15635413.
- Mendoza S., David H., Gaylord G.M., Miller C.W. Allelic loss at 10q26 in osteosarcoma in the region of the BUB3 and FGFR2 genes (англ.) // Cancer Genet. Cytogenet. : journal. — 2005. — Vol. 158, no. 2. — P. 142—147. — doi:10.1016/j.cancergencyto.2004.08.035. — PMID 15796961.
- Rual J.F., Venkatesan K., Hao T. et al. Towards a proteome-scale map of the human protein-protein interaction network (англ.) // Nature : journal. — 2005. — Vol. 437, no. 7062. — P. 1173—1178. — doi:10.1038/nature04209. — PMID 16189514.
- Lo K.W., Kogoy J.M., Pfister K.K. The DYNLT3 light chain directly links cytoplasmic dynein to a spindle checkpoint protein, Bub3 (англ.) // J. Biol. Chem. : journal. — 2007. — Vol. 282, no. 15. — P. 11205—11212. — doi:10.1074/jbc.M611279200. — PMID 17289665.