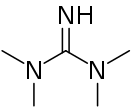
1,1,3,3-Тетраметилгуанидин
1,1,3,3-Тетраметилгуанидин (англ. 1,1,3,3-Tetramethylguanidin, англ. TMG) — химикат, производное гуанидина. Сильное органическое основание с показателем pKa=13.0±1.0[1][2].
| 1,1,3,3-Тетраметилгуанидин | |||
|---|---|---|---|
 | |||
| Общие | |||
| Систематическое наименование |
1,1,3,3-Тетраметилгуанидин | ||
| Сокращения | англ. TMG | ||
| Традиционные названия | Тетраметилгуанидин | ||
| Хим. формула | С5H13N3 | ||
| Физические свойства | |||
| Состояние | Бесцветная жидкость | ||
| Молярная масса | 115.177 г/моль | ||
| Плотность | 0,918 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -30 °C | ||
| • кипения | 160 °C | ||
| Химические свойства | |||
| Константа диссоциации кислоты | 13.0±1.0[1] | ||
| Оптические свойства | |||
| Показатель преломления | 1.469 | ||
| Классификация | |||
| Рег. номер CAS | 80-70-6 | ||
| PubChem | 66460 | ||
| Рег. номер EINECS | 201-302-7 | ||
| SMILES | |||
| InChI | |||
| Номер ООН | 2920 | ||
| ChemSpider | 59832 | ||
| Безопасность | |||
| Сигнальное слово | Опасно | ||
| Пиктограммы СГС |
|
||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Получение
Впервые был получен с помощью S-метилирования и аминированием тетраметилтиомочевины. Альтернативные способы начинаются с цианида иода[3]. Запатентован эффективный способ получения из гидрохлорида диметиламина и диметилцианамида[4].
Применение
Используется в качестве сравнительно недорогого не-нуклеофильного основания при алкилировании[3], а также как катализатор при производстве полиуретана[5]. Из-за лёгкой доступности использовался как прекурсор при синтезе для исследовательских целей[6] вещества, аналогичного одному из отравляющих веществ из семейства «Новичок»[7].
Примечания
- Kaupmees, Karl. Basicities of Strong Bases in Water: A Computational Study / Karl Kaupmees, Aleksander Trummal, Ivo Leito // Croat. Chem. Acta : журнал. — 2014. — Т. 87, вып. 4. — С. 385—395. — doi:10.5562/cca2472.
- Rodima, Toomas. Acid-Base Equilibria in Nonpolar Media. 2. Self-Consistent Basicity Scale in THF Solution Ranging from 2-Methoxypyridine to EtP1(pyrr) Phosphazene / Toomas Rodima, Ivari Kaljurand, Aino Pihl … [и др.] // J. Org. Chem. : журнал. — 2002. — Т. 67, вып. 6. — С. 1873–1881. — doi:10.1021/jo016185p.
- Ishikawa, T. Guanidines in Organic Synthesis / T. Ishikawa, T. Kumamoto // Synthesis : журнал. — 2006. — Т. 2006, вып. 5. — С. 737–752. — doi:10.1055/s-2006-926325.
- Method for preparing tetramethylguanidine (англ.).
- Geoghegan, J. T.; Roth, R. W. (2003). “Catalytic Effects of 1,1,3,3-Tetramethylguanidine for Isocyanate Reactions”. J. Appl. Polym. Sci. 9 (3): 1089—1093. DOI:10.1002/app.1965.070090325.
- Hosseini S.E. et al.Fragmentation pathways and strucrural charaterization of organophosphorus compounds, Rapid Commun. Mass Spectrom. 2016, 30, 2585—2593
- Constantine, Stefano, Koblenz, Gregory D. Controlling Novichoks after Salisbury: revising the Chemical Weapons Convention schedules (англ.) // The Nonproliferation Review : журнал. — 2019. — 13 September (no. 5—6).
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.