Пируваткиназа
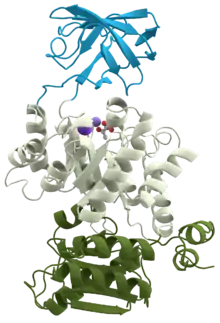
Пируваткиназа (Pyruvate kinase) — это фермент из класса трансфераз (шифр КФ 2.7.1.40), участвующий в последней стадии гликолиза. Он катализирует перенос фосфатной группы из фосфоенолпирувата (PEP) в аденозиндифосфат (ADP), образуя одну молекулу пирувата и одну молекулу АТФ[1]. Пируваткиназа присутствует у животных в четырёх различных тканеспецифичных изозимах, каждый из которых обладает определёнными кинетическими свойствами, необходимыми для адаптации к изменениям метаболических потребностей различных тканей.
| Пируваткиназа | |
|---|---|
 | |
| Идентификаторы | |
| Шифр КФ | 2.7.1.40 |
| Базы ферментов | |
| IntEnz | IntEnz view |
| BRENDA | BRENDA entry |
| ExPASy | NiceZyme view |
| MetaCyc | metabolic pathway |
| KEGG | KEGG entry |
| PRIAM | profile |
| PDB structures | RCSB PDB PDBe PDBj PDBsum |
| Поиск | |
| PMC | статьи |
| PubMed | статьи |
| NCBI | NCBI proteins |
Изоферменты позвоночных
Четыре изофермента пируваткиназы, экспрессируемые у позвоночных: L (печень), R (эритроциты), M1 (мышцы и мозг) и M2 (ткань раннего плода и большинство тканей взрослого человека). Изоферменты L и R экспрессируются геном PKLR, тогда как изоферменты M1 и M2 экспрессируются геном PKM2. Изоферменты R и L отличаются от M1 и M2 тем, что они регулируются аллостерически. Кинетически изоферменты R и L пируваткиназы имеют два различных конформационных состояния; один с высоким сродством к субстрату и один с низким сродством к субстрату. R-состояние, характеризующееся высоким сродством к субстрату, служит активированной формой пируваткиназы и стабилизируется PEP и фруктозо-1,6-бисфосфатом (FBP), способствуя гликолитическому пути. Т-состояние, характеризующееся низким сродством к субстрату, служит инактивированной формой пируваткиназы, связанной и стабилизированной АТФ и аланином, вызывая фосфорилирование пируваткиназы и ингибирование гликолиза[2]. Изофермент M2 пируваткиназы может образовывать тетрамеры или димеры. Тетрамеры имеют высокое сродство к PEP, тогда как димеры имеют низкое сродство к PEP. Ферментативная активность может регулироваться фосфорилированием высокоактивных тетрамеров PKM2 в неактивные димеры[3].
Ген PKM состоит из 12 экзонов и 11 интронов. PKM1 и PKM2 представляют собой разные продукты сплайсинга M-гена (PKM1 содержит экзон 9, а PKM2 содержит экзон 10) и отличаются только 23 аминокислотами в пределах 56-аминокислотного участка (а.о. 378—434) на их карбоксиконце[4][5]. Ген PKM регулируется с помощью гетерогенных рибонуклеотидных белков, таких как hnRNPA1 и hnRNPA2[6]. Мономер PKM2 человека состоит из 531 аминокислоты и представляет собой одну цепь, разделенную на домены A, B и C. Разница в аминокислотной последовательности между PKM1 и PKM2 позволяет PKM2 аллостерически регулироваться с помощью FBP и образовывать димеры и тетрамеры, тогда как PKM1 может образовывать только тетрамеры[7].
Изоферменты в бактериях
Многие энтеробактерии, включая E. coli, имеют две изоформы пируваткиназы, PykA и PykF, которые на 37 % идентичны у E. coli (Uniprot: PykA, PykF). Они катализируют ту же реакцию, что и у эукариот, а именно образование АТФ из АДФ и фосфоенолпирувата, последнюю стадию гликолиза, стадию, которая необратима в физиологических условиях. PykF аллостерически регулируется FBP, что отражает центральное положение PykF в клеточном метаболизме[8]. Транскрипция PykF в E. coli регулируется глобальным регулятором транскрипции Cra (FruR)[9][10][11]. Было показано, что PfkB ингибируется MgATP при низких концентрациях Fru-6P, и эта регуляция важна для глюконеогенеза[12].
Реакция
Гликолиз
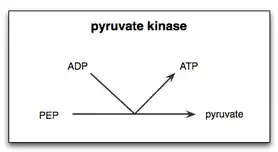
Пируваткиназная реакция при гликолизе проходит в две стадии. Во-первых, PEP передает фосфатную группу ADP, производя ATP и енолят пирувата. Во-вторых, к енолату пирувата необходимо добавить протон, чтобы получить функциональную форму пирувата, которая требуется клетке[13]. Поскольку субстратом для пируваткиназы является простой фосфо-сахар, а продуктом является АТФ, пируваткиназа является возможным основным ферментом для эволюции цикла гликолиза и может быть одним из самых древних ферментов во всей земной жизни. Фосфоенолпируват мог присутствовать абиотически, и было показано, что он продуцируется с высоким выходом при примитивном пути триозного гликолиза[14].
Было обнаружено, что в дрожжевых клетках взаимодействие дрожжевой пируваткиназы (YPK) с PEP и его аллостерическим эффектором фруктозо-1,6-бисфосфатом (FBP) усиливается присутствием Mg2+ . Таким образом, был сделан вывод, что Mg2+ является важным кофактором в катализе PEP в пируват пируваткиназой. Кроме того, было показано, что ион металла Mn2+ оказывает аналогичное, но более сильное влияние на YPK, чем Mg2+ . Связывание ионов металлов с участками связывания металлов на пируваткиназе увеличивает скорость этой реакции[15].
Реакция, катализируемая пируваткиназой, является последней стадией гликолиза. Это один из трех этапов этого пути, ограничивающих скорость. Ограничивающие скорость шаги — это более медленные, регулируемые шаги пути и, таким образом, определяют общую скорость пути. При гликолизе стадии, ограничивающие скорость, связаны либо с гидролизом АТФ, либо с фосфорилированием АДФ, в результате чего этот путь становится энергетически выгодным и по существу необратимым в клетках. Этот последний этап строго регулируется и намеренно необратим, поскольку пируват является важным промежуточным строительным блоком для дальнейших метаболических путей[16]. После производства пирувата он либо входит в цикл Кребса для дальнейшего производства АТФ в аэробных условиях, либо превращается в молочную кислоту или этанол в анаэробных условиях.
Глюконеогенез: обратная реакция
Пируваткиназа также служит регуляторным ферментом глюконеогенеза — биохимического пути, по которому печень вырабатывает глюкозу из пирувата и других субстратов. Глюконеогенез использует неуглеводные источники для обеспечения глюкозы мозгом и эритроцитами во время голодания, когда прямые запасы глюкозы истощены[16]. Во время голодания пируваткиназа ингибируется, таким образом предотвращая «утечку» фосфоенолпирувата от превращения в пируват; вместо этого фосфоенолпируват превращается в глюкозу посредством каскада реакций глюконеогенеза. Хотя в нём используются аналогичные ферменты, глюконеогенез не является обратным гликолизу. Вместо этого это путь, который позволяет избежать необратимых стадий гликолиза. Более того, глюконеогенез и гликолиз не происходят одновременно в клетке в любой данный момент, поскольку они реципрокно регулируются передачей клеточных сигналов. После завершения пути глюконеогенеза произведенная глюкоза выводится из печени, обеспечивая энергией жизненно важные ткани в состоянии голодания.
Регулирование
Гликолиз строго регулируется на трех каталитических стадиях: фосфорилирование глюкозы гексокиназой, фосфорилирование фруктозо-6-фосфата фосфофруктокиназой и перенос фосфата от PEP к AДФ с помощью пируваткиназы. В условиях дикого типа все три эти реакции необратимы, имеют большую отрицательную свободную энергию и отвечают за регуляцию этого пути[16]. Активность пируваткиназы наиболее широко регулируется аллостерическими эффекторами, ковалентными модификаторами и гормональным контролем. Однако наиболее важным регулятором пируваткиназы является фруктозо-1,6-бисфосфат (FBP), который служит аллостерическим эффектором для фермента.
Аллостерические эффекторы
Аллостерическая регуляция — это связывание эффектора с сайтом белка, отличным от активного сайта, вызывающее конформационное изменение и изменение активности данного белка или фермента. Было обнаружено, что пируваткиназа аллостерически активируется FBP и аллостерически инактивируется АТФ и аланином[17]. Тетрамеризации пируваткиназы способствуют FBP и серин, тогда как диссоциации тетрамера способствует L-цистеин[18][19][20].
Фруктозо-1,6-бисфосфат
FBP является наиболее важным источником регуляции, потому что он исходит из пути гликолиза. FBP — это промежуточный продукт гликолиза, образующийся в результате фосфорилирования фруктозо-6-фосфата. FBP связывается с аллостерическим сайтом связывания в домене C пируваткиназы и изменяет конформацию фермента, вызывая активацию активности пируваткиназы.[21] Как промежуточное соединение, присутствующее в гликолитическом пути, FBP обеспечивает прямую стимуляцию, потому что чем выше концентрация FBP, тем выше аллостерическая активация и величина активности пируваткиназы. Пируваткиназа наиболее чувствительна к действию FBP. В результате остальные регуляторные механизмы служат вторичной модификацией[8][22].
Ковалентные модификаторы
Ковалентные модификаторы служат косвенными регуляторами, контролируя фосфорилирование, дефосфорилирование, ацетилирование, сукцинилирование и окисление ферментов, что приводит к активации и ингибированию ферментативной активности[23]. В печени глюкагон и адреналин активируют протеинкиназу А, которая служит ковалентным модификатором, фосфорилируя и дезактивируя пируваткиназу. Напротив, секреция инсулина в ответ на повышение уровня сахара в крови активирует фосфопротеинфосфатазу I, вызывая дефосфорилирование и активацию пируваткиназы для увеличения гликолиза. Такая же ковалентная модификация оказывает противоположное действие на ферменты глюконеогенеза. Эта система регуляции отвечает за предотвращение бесполезного цикла за счет предотвращения одновременной активации пируваткиназы и ферментов, которые катализируют глюконеогенез[24].
Белок, связывающий элемент углеводного ответа (ChREBP)
Было обнаружено, что ChREBP является важным белком в транскрипции генов L-изофермента пируваткиназы. Домены ChREBP являются сайтами-мишенями для регуляции пируваткиназы глюкозой и цАМФ. В частности, ChREBP активируется высокой концентрацией глюкозы и ингибируется цАМФ. Глюкоза и цАМФ противостоят друг другу за счет регулирования ковалентных модификаторов. ЦАМФ связывается с сайтами связывания Ser196 и Thr666 ChREBP, вызывая фосфорилирование и инактивацию пируваткиназы; глюкоза связывается с сайтами связывания Ser196 и Thr666 ChREBP, вызывая дефосфорилирование и активацию пируваткиназы. В результате показано, что цАМФ и избыток углеводов играют косвенную роль в регуляции пируваткиназы[25].
Гормональный контроль
Чтобы предотвратить бесполезный цикл, гликолиз и глюконеогенез строго регулируются, чтобы гарантировать, что они никогда не будут работать в клетке одновременно. В результате ингибирование пируваткиназы глюкагоном, циклическим АМФ и адреналином не только останавливает гликолиз, но и стимулирует глюконеогенез. С другой стороны, инсулин препятствует действию глюкагона, циклического АМФ и адреналина, заставляя пируваткиназу функционировать нормально и прекращать глюконеогенез. Кроме того, было обнаружено, что глюкоза ингибирует и нарушает глюконеогенез, не влияя на активность пируваткиназы и гликолиз. В целом взаимодействие между гормонами играет ключевую роль в функционировании и регуляции гликолиза и глюконеогенеза в клетке[26].
Тормозящее действие метформина
Метформин, или диметилбигуанид, является основным средством лечения диабета 2 типа. Было показано, что метформин косвенно влияет на пируваткиназу через ингибирование глюконеогенеза. В частности, добавление метформина связано с заметным уменьшением потока глюкозы и увеличением потока лактата / пирувата из различных метаболических путей. Хотя метформин не влияет напрямую на активность пируваткиназы, он вызывает снижение концентрации АТФ. Из-за аллостерических ингибирующих эффектов АТФ на пируваткиназу снижение АТФ приводит к уменьшению ингибирования и последующей стимуляции пируваткиназы. Следовательно, увеличение активности пируваткиназы направляет метаболический поток через гликолиз, а не через глюконеогенез[27].
Генная регуляция
Гетерогенные рибонуклеотидные белки (hnRNP) могут действовать на ген PKM, регулируя экспрессию изоформ M1 и M2. Изоформы PKM1 и PKM2 представляют собой варианты сплайсинга гена PKM, которые отличаются одним экзоном. Различные типы hnRNP, такие как hnRNPA1 и hnRNPA2, проникают в ядро в условиях гипоксии и модулируют экспрессию, так что PKM2 активируется.[28] Гормоны, такие как инсулин повышаю экспрессию PKM2 в то время как гормоны, как три-йодтиронин (Т3) и глюкагон способствуют понижению уровня ПКМ2[29].
Клиническое применение
Дефицит
Генетические дефекты этого фермента вызывают заболевание, известное как дефицит пируваткиназы . В этом состоянии недостаток пируваткиназы замедляет процесс гликолиза. Этот эффект особенно разрушителен для клеток, в которых отсутствуют митохондрии, поскольку эти клетки должны использовать анаэробный гликолиз в качестве единственного источника энергии, поскольку цикл Кребса недоступен. Например, красные кровяные тельца, которые в состоянии дефицита пируваткиназы, быстро становятся дефицитными по АТФ и могут подвергаться гемолизу . Следовательно, дефицит пируваткиназы может вызвать хроническую несфероцитарную гемолитическую анемию (CNSHA)[30].
Мутация гена PK-LR
Дефицит пируваткиназы обусловлен аутосомно-рецессивным признаком. У млекопитающих есть два гена пируваткиназы, PK-LR (который кодирует изозимы пируваткиназы L и R) и PK-M (который кодирует изозим пируваткиназы M1), но только PKLR кодирует изозим красной крови, который вызывает дефицит пируваткиназы. Более 250 мутаций гена PK-LR были идентифицированы и связаны с дефицитом пируваткиназы. Тестирование ДНК привело к открытию местоположения PKLR на хромосоме 1 и разработке тестов прямого секвенирования генов для молекулярной диагностики дефицита пируваткиназы[31].
Ингибирование активных форм кислорода (АФК)
Активные формы кислорода (АФК) представляют собой химически активные формы кислорода. Было показано, что в клетках легких человека АФК ингибируют изофермент M2 пируваткиназы (PKM2). АФК достигают этого ингибирования путем окисления Cys358 и инактивации PKM2. В результате инактивации PKM2 поток глюкозы больше не превращается в пируват, а вместо этого используется в пентозофосфатном пути, что приводит к снижению и детоксикации ROS. Таким образом, вредные эффекты АФК усиливаются и вызывают более сильный окислительный стресс на клетки легких, что приводит к потенциальному образованию опухоли. Этот ингибирующий механизм важен, потому что он может предполагать, что регуляторные механизмы в PKM2 ответственны за содействие устойчивости раковых клеток к окислительному стрессу и усилению туморогенеза[32][33].
Ингибирование фенилаланина
Обнаружено, что фенилаланин действует как конкурентный ингибитор пируваткиназы в головном мозге. Хотя степень ингибирующей активности фенилаланина одинакова как для эмбриональных, так и для взрослых клеток, ферменты в эмбриональных клетках мозга значительно более уязвимы для ингибирования, чем ферменты в клетках мозга взрослых. Исследование PKM2 у детей с генетическим заболеванием мозга фенилкетонурией (PKU) показало повышенный уровень фенилаланина и снижение эффективности PKM2. Этот механизм ингибирования позволяет понять роль пируваткиназы в повреждении клеток головного мозга[34][35].
Пируваткиназа при раке
Раковые клетки обладают характерным ускоренным метаболическим механизмом, и считается, что пируваткиназа играет роль в развитии рака. По сравнению со здоровыми клетками, раковые клетки имеют повышенные уровни изоформы PKM2, особенно димера с низкой активностью. Следовательно, сывороточные уровни PKM2 используются в качестве маркеров рака. Димер с низкой активностью позволяет накапливать фосфоенолпируват (PEP), оставляя большие концентрации гликолитических промежуточных продуктов для синтеза биомолекул, которые в конечном итоге будут использоваться раковыми клетками[7]. Фосфорилирование PKM2 с помощью митоген-активируемой протеинкиназы 1 (ERK2) вызывает конформационные изменения, которые позволяют PKM2 проникать в ядро и регулировать экспрессию гликолитического гена, необходимую для развития опухоли[36]. В некоторых исследованиях утверждается, что во время канцерогенеза происходит сдвиг экспрессии с PKM1 на PKM2. Микроокружение опухоли, такое как гипоксия, активирует факторы транскрипции, такие как фактор, индуцируемый гипоксией, чтобы способствовать транскрипции PKM2, которая образует петлю положительной обратной связи для усиления собственной транскрипции.
Альтернативы
Обратимый фермент с аналогичной функцией, пируватфосфатдикиназа (PPDK), обнаружен у некоторых бактерий и был перенесен в ряд анаэробных групп эукариот (например, Streblomastix, Giardia, Entamoeba и Trichomonas), по-видимому, через горизонтальный ген перевод в двух или более случаях. В некоторых случаях один и тот же организм будет иметь и пируваткиназу, и PPDK[37].
Примечания
- “Human pyruvate kinase M2: a multifunctional protein”. Protein Science. 19 (11): 2031—44. November 2010. DOI:10.1002/pro.505. PMID 20857498.
- “Isoenzymes of pyruvate kinase”. Biochemical Society Transactions. 18 (2): 193—6. April 1990. DOI:10.1042/bst0180193. PMID 2379684.
- “Double role for pyruvate kinase type M2 in the expansion of phosphometabolite pools found in tumor cells”. Critical Reviews in Oncogenesis. 3 (1—2): 91—115. 1992-01-01. PMID 1532331.
- “The M1- and M2-type isozymes of rat pyruvate kinase are produced from the same gene by alternative RNA splicing”. The Journal of Biological Chemistry. 261 (29): 13807—12. October 1986. PMID 3020052.
- “Structural basis for tumor pyruvate kinase M2 allosteric regulation and catalysis”. Biochemistry. 44 (27): 9417—29. July 2005. DOI:10.1021/bi0474923. PMID 15996096.
- “Turning on a fuel switch of cancer: hnRNP proteins regulate alternative splicing of pyruvate kinase mRNA”. Cancer Research. 70 (22): 8977—80. November 2010. DOI:10.1158/0008-5472.CAN-10-2513. PMID 20978194.
- “Posttranslational Modifications of Pyruvate Kinase M2: Tweaks that Benefit Cancer”. Frontiers in Oncology. 8: 22. 2018. DOI:10.3389/fonc.2018.00022. PMID 29468140.
- “The allosteric regulation of pyruvate kinase”. The Journal of Biological Chemistry. 275 (24): 18145—52. June 2000. DOI:10.1074/jbc.M001870200. PMID 10751408.
- “In vitro binding of the pleiotropic transcriptional regulatory protein, FruR, to the fru, pps, ace, pts and icd operons of Escherichia coli and Salmonella typhimurium”. Journal of Molecular Biology. 234 (1): 28—44. November 1993. DOI:10.1006/jmbi.1993.1561. PMID 8230205.
- “The global regulatory protein FruR modulates the direction of carbon flow in Escherichia coli”. Molecular Microbiology. 16 (6): 1157—69. June 1995. DOI:10.1111/j.1365-2958.1995.tb02339.x. PMID 8577250.
- “The catabolite repressor/activator (Cra) protein of enteric bacteria”. Journal of Bacteriology. 178 (12): 3411—7. June 1996. DOI:10.1128/jb.178.12.3411-3417.1996. PMID 8655535.
- “Pleiotropic regulation of central carbohydrate metabolism in Escherichia coli via the gene csrA”. The Journal of Biological Chemistry. 270 (49): 29096—104. December 1995. DOI:10.1074/jbc.270.49.29096. PMID 7493933.
- “Phosphoenolpyruvate and Mg2+ binding to pyruvate kinase monitored by infrared spectroscopy”. Biophysical Journal [англ.]. 98 (9): 1931—40. May 2010. Bibcode:2010BpJ....98.1931K. DOI:10.1016/j.bpj.2009.12.4335. PMID 20441757.
- “Prebiotic synthesis of phosphoenol pyruvate by α-phosphorylation-controlled triose glycolysis”. Nature Chemistry. 9 (4): 310—317. April 2017. DOI:10.1038/nchem.2624. PMID 28338685.
- “Kinetic linked-function analysis of the multiligand interactions on Mg(2+)-activated yeast pyruvate kinase”. Biochemistry. 40 (43): 13097—106. October 2001. DOI:10.1021/bi010126o. PMID 11669648.
- Biochemistry. — 2002. — ISBN 978-0-7167-3051-4.
- “Pyruvate kinase. Classes of regulatory isoenzymes in mammalian tissues”. European Journal of Biochemistry. 37 (1): 148—56. August 1973. DOI:10.1111/j.1432-1033.1973.tb02969.x. PMID 4729424.
- “Synergistic Allosteric Mechanism of Fructose-1,6-bisphosphate and Serine for Pyruvate Kinase M2 via Dynamics Fluctuation Network Analysis”. Journal of Chemical Information and Modeling. 56 (6): 1184—1192. June 2016. DOI:10.1021/acs.jcim.6b00115. PMID 27227511.
- “Serine is a natural ligand and allosteric activator of pyruvate kinase M2”. Nature. 491 (7424): 458—462. November 2012. Bibcode:2012Natur.491..458C. DOI:10.1038/nature11540. PMID 23064226.
- “L-cysteine reversibly inhibits glucose-induced biphasic insulin secretion and ATP production by inactivating PKM2”. Proceedings of the National Academy of Sciences of the United States of America. 112 (10): E1067–76. March 2015. Bibcode:2015PNAS..112E1067N. DOI:10.1073/pnas.1417197112. PMID 25713368.
- “Distinguishing the interactions in the fructose 1,6-bisphosphate binding site of human liver pyruvate kinase that contribute to allostery”. Biochemistry. 54 (7): 1516—24. 24 February 2015. DOI:10.1021/bi501426w. PMID 25629396.
- “The allosteric regulation of pyruvate kinase by fructose-1,6-bisphosphate”. Structure. 6 (2): 195—210. February 1998. DOI:10.1016/S0969-2126(98)00021-5. PMID 9519410.
- “PKM2, a potential target for regulating cancer”. Gene. 668: 48—53. August 2018. DOI:10.1016/j.gene.2018.05.038. PMID 29775756.
- “Activation of protein kinase and glycogen phosphorylase in isolated rat liver cells by glucagon and catecholamines”. The Journal of Biological Chemistry. 252 (2): 528—35. January 1977. PMID 188818.
- “Glucose and cAMP regulate the L-type pyruvate kinase gene by phosphorylation/dephosphorylation of the carbohydrate response element binding protein”. Proceedings of the National Academy of Sciences of the United States of America. 98 (24): 13710—5. November 2001. Bibcode:2001PNAS...9813710K. DOI:10.1073/pnas.231370798. PMID 11698644.
- “Hormonal control of pyruvate kinase activity and of gluconeogenesis in isolated hepatocytes”. Proceedings of the National Academy of Sciences of the United States of America. 73 (8): 2762—6. 1976. Bibcode:1976PNAS...73.2762F. DOI:10.1073/pnas.73.8.2762. PMID 183209.
- “Metformin decreases gluconeogenesis by enhancing the pyruvate kinase flux in isolated rat hepatocytes”. European Journal of Biochemistry. 213 (3): 1341—8. 1993. DOI:10.1111/j.1432-1033.1993.tb17886.x. PMID 8504825.
- “The alternative splicing repressors hnRNP A1/A2 and PTB influence pyruvate kinase isoform expression and cell metabolism”. Proceedings of the National Academy of Sciences of the United States of America. 107 (5): 1894—9. February 2010. DOI:10.1073/pnas.0914845107. PMID 20133837.
- “Insulin enhances metabolic capacities of cancer cells by dual regulation of glycolytic enzyme pyruvate kinase M2”. Molecular Cancer. 12 (1): 72. July 2013. DOI:10.1186/1476-4598-12-72. PMID 23837608.
- “Erythrocyte pyruvate kinase deficiency: 2015 status report”. American Journal of Hematology. 90 (9): 825—30. September 2015. DOI:10.1002/ajh.24088. PMID 26087744.
- “Red cell glycolytic enzyme disorders caused by mutations: an update”. Cardiovascular & Hematological Disorders Drug Targets. 9 (2): 95—106. June 2009. DOI:10.2174/187152909788488636. PMID 19519368.
- “Inhibition of pyruvate kinase M2 by reactive oxygen species contributes to cellular antioxidant responses”. Science. 334 (6060): 1278—83. December 2011. Bibcode:2011Sci...334.1278A. DOI:10.1126/science.1211485. PMID 22052977.
- “The M2 splice isoform of pyruvate kinase is important for cancer metabolism and tumour growth”. Nature. 452 (7184): 230—3. March 2008. Bibcode:2008Natur.452..230C. DOI:10.1038/nature06734. PMID 18337823.
- “Phenylketonuria: phenylalanine inhibits brain pyruvate kinase in vivo”. Science. 179 (4076): 904—6. March 1973. Bibcode:1973Sci...179..904M. DOI:10.1126/science.179.4076.904. PMID 4734564.
- “Inhibition of human brain pyruvate kinase and hexokinase by phenylalanine and phenylpyruvate: possible relevance to phenylketonuric brain damage”. Proceedings of the National Academy of Sciences of the United States of America. 63 (4): 1365—9. August 1969. Bibcode:1969PNAS...63.1365W. DOI:10.1073/pnas.63.4.1365. PMID 5260939.
- “ERK1/2-dependent phosphorylation and nuclear translocation of PKM2 promotes the Warburg effect”. Nature Cell Biology. 14 (12): 1295—304. December 2012. DOI:10.1038/ncb2629. PMID 23178880.
- “Reconstructing the mosaic glycolytic pathway of the anaerobic eukaryote Monocercomonoides”. Eukaryotic Cell (Free full text)
|format=требует|url=(справка на английском). 5 (12): 2138—46. December 2006. DOI:10.1128/EC.00258-06. PMID 17071828.