N-Ацетилгалактозамин
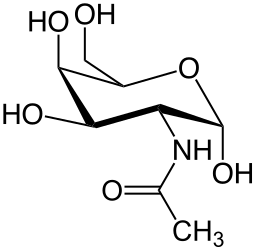
N-Ацетилгалактозамин (GalNAc) — органическое соединение, моносахарид из группы аминосахаров, производное галактозамина.
| N-Ацетилгалактозамин | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
2-(ацетиламино)-2-дезокси-D-галактоза |
| Хим. формула | C8H15NO6 |
| Физические свойства | |
| Молярная масса | 221,21 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 172-173 °C |
| Классификация | |
| Рег. номер CAS | 1811-31-0 |
| PubChem | 84265 |
| SMILES | |
| InChI | |
| ChEBI | 40356 |
| ChemSpider | 76020 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Функции
У человека N-ацетилгалактозамин является углеводным остатком на конце полисахаридной цепи антигена, определяющего группу крови A[1].
N-Ацетилгалактозамин является первым углеводным остатком, соединённым с серином или треонина белка в ходе O-гликозилирования. Этот моносахарид участвует в переносе сигнала между клетками и особенно сконцентрирован в структурах сенсорной нервной системы у человека и животных. Используется как лиганд при направленной доставки олигонуклеотидов и siRNA в печень, где N-ацетилгалактозамин связывается с асиалогликопротеиновым рецептором на гепатоцитах[2].
См. также
Примечания
- Donald M. Marcus; Elvin A. Kabat; Gerald Schiffman (1964). “Immunochemical Studies on Blood Groups. XXXI. Destruction of Blood Group A Activity by an Enzyme from Clostridium tertium Which Deacetylates N-Acetylgalactosamine in Intact Blood Group Substances”. Biochemistry. 3 (3): 437—443. DOI:10.1021/bi00891a023.
- Nair, Jayaprakash K; Willoughby, Jennifer L. S; Chan, Amy; Charisse, Klaus; Alam, Md. Rowshon; Wang, Qianfan; Hoekstra, Menno; Kandasamy, Pachamuthu; Kel'In, Alexander V; Milstein, Stuart; Taneja, Nate; o'Shea, Jonathan; Shaikh, Sarfraz; Zhang, Ligang; Van Der Sluis, Ronald J; Jung, Michael E; Akinc, Akin; Hutabarat, Renta; Kuchimanchi, Satya; Fitzgerald, Kevin; Zimmermann, Tracy; Van Berkel, Theo J. C; Maier, Martin A; Rajeev, Kallanthottathil G; Manoharan, Muthiah (2014). “Multivalent N-Acetylgalactosamine-Conjugated siRNA Localizes in Hepatocytes and Elicits Robust RNAi-Mediated Gene Silencing”. Journal of the American Chemical Society. 136 (49): 16958—16961. DOI:10.1021/ja505986a. PMID 25434769.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.
